Clear Sky Science · zh
用于 AI 驱动细胞分裂分析的亚期标注有丝分裂数据集
为何计数分裂中的细胞至关重要
当医生在显微镜下观察癌症时,他们使用的最重要线索之一就是处于分裂过程中的细胞数量。分裂迅速的肿瘤通常具有更具侵袭性的行为,可能需要不同的治疗策略。然而,发现这些微小的分裂细胞对病理学家来说既费时又令人疲惫,即使是专家之间也常有分歧。本研究提出了一个新的、注释丰富的图像数据集和一种改进的人工智能(AI)方法,旨在帮助计算机在不同癌症类型和医院环境中更可靠地识别和理解这些分裂细胞。
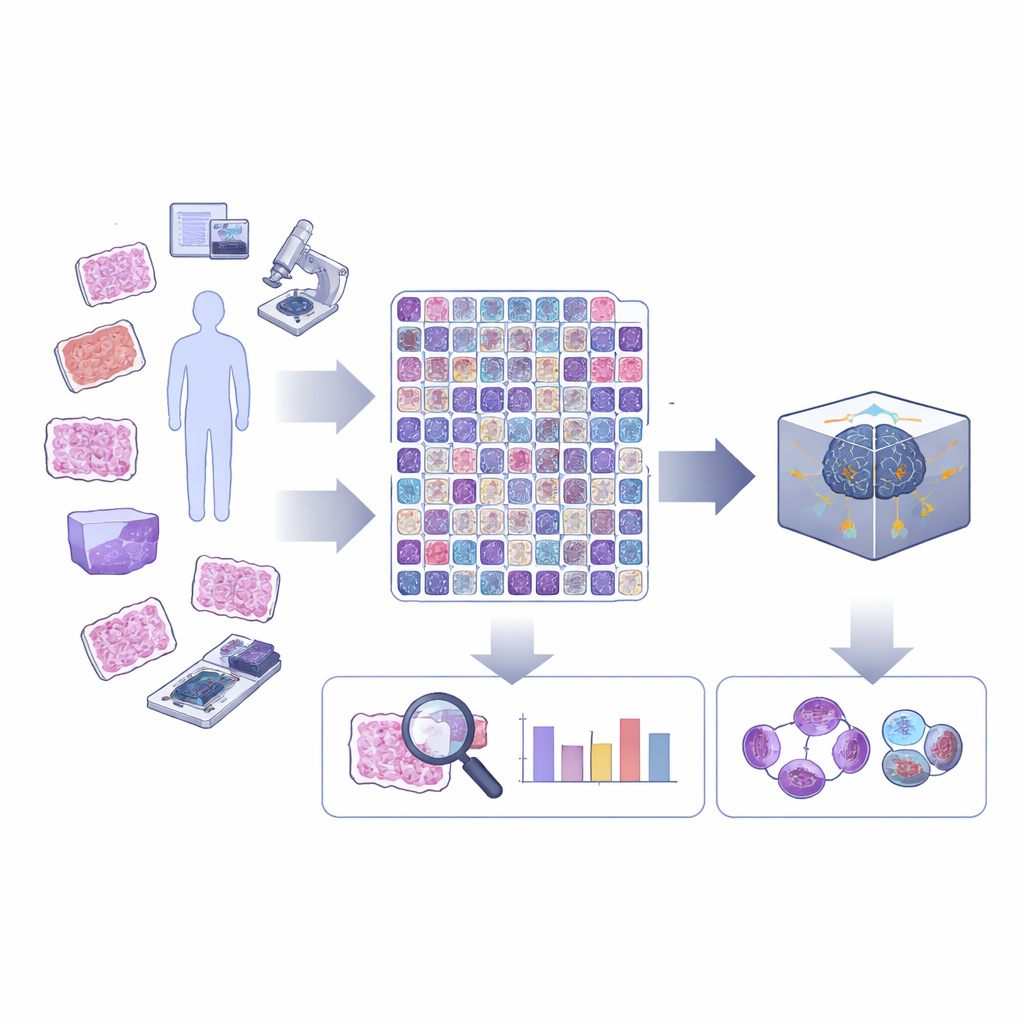
更细致地观察癌组织中的细胞分裂
细胞分裂(即有丝分裂)按一系列阶段展开,细胞的遗传物质在过程中心出复制并被分开。在常规癌症诊断中,大多数计算工具只是将“有丝图像”作为一个单一类别标记,忽略它们所处的阶段或是否呈现异常。然而,异常或“非典型”分裂,以及早期与晚期阶段之间的比例,可能包含关于肿瘤危险性的重要信息。作者认为,只有当 AI 能够识别这些人类专家在显微镜下已经在寻找的更精细差别时,病理学领域的 AI 才能发挥其全部潜力。
构建更丰富的图像库
为了超越对分裂细胞的简单二元判断,团队扩展了已有的大型基准数据集 MIDOG++,该数据集已涵盖多种肿瘤类型、物种和扫描设备。专家标注者重新审查了超过一万例有丝分裂图像,并将每例分配到正常细胞分裂的五个主要阶段之一,另设一类用于非典型有丝分裂。他们还对每个细胞绘制了精确轮廓,而不仅仅是粗略的框。这种细致工作使该数据集成为支持更精确 AI 训练以及未来研究分裂过程中细胞形态和结构的资源。
新增肺癌数据集
鉴于 AI 系统在从一家医院或器官类型迁移到另一处时常会出现性能下降,研究者还创建了来自肺腺癌的新数据集——肺癌中常见且致命的一种类型。他们没有只关注活动最旺盛的“热点”区域,而是选择了每张载玻片上的整个肿瘤区,将其切分为可管理的图像块,并耐心地标注分裂细胞、非典型分裂以及外观相似但未分裂的细胞。该 LUNG‑MITO 数据集为检测算法在面对新的组织和扫描条件时是否仍能保持性能提供了一个严峻的现实世界测试。
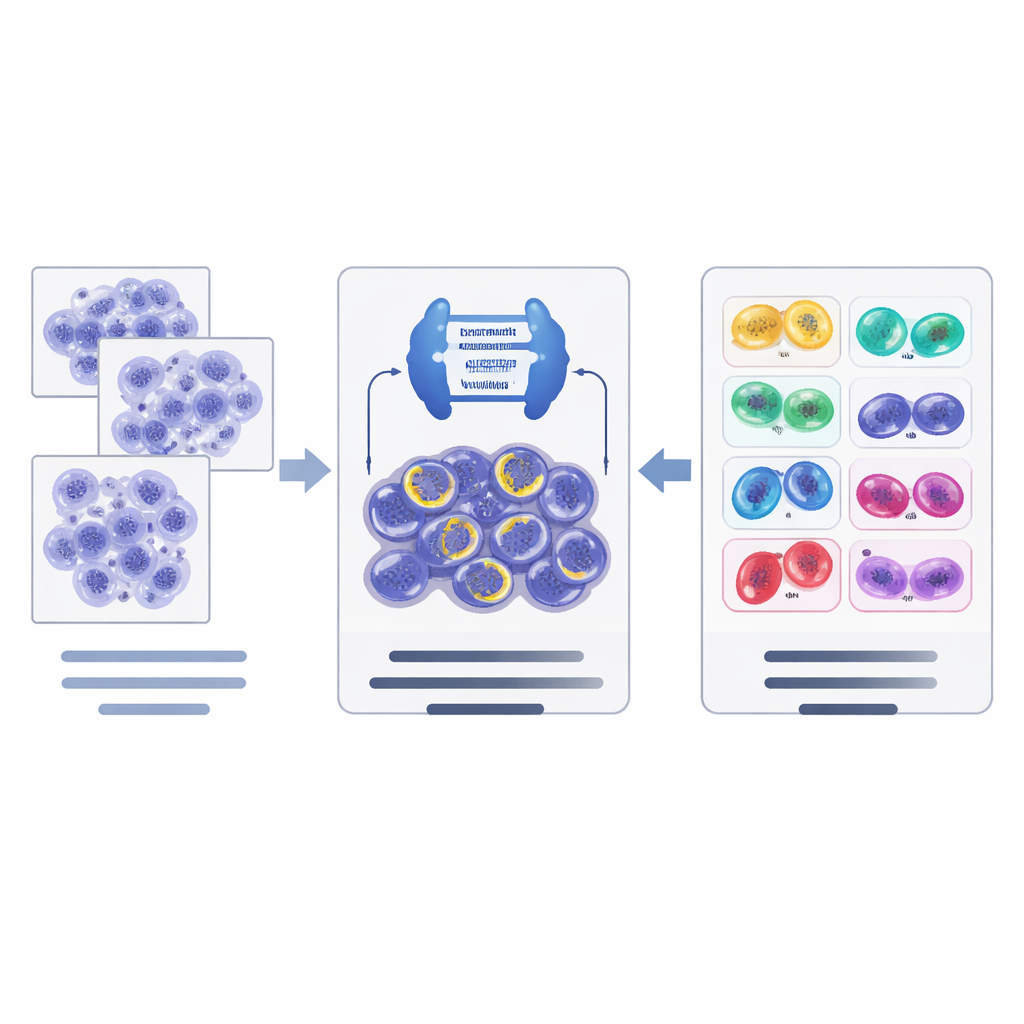
新 AI 流程如何工作
在这些数据资源之上,作者设计了一个两步 AI 流程。首先,一个基于现代架构 ConvNeXt 并结合 Mask R‑CNN 的强大图像分割网络扫描组织切片并提出候选分裂细胞,为每个候选划出轮廓并给出初步的阶段猜测。其次,一个单独的分类网络(EfficientNet)对这些候选对象进行更细致的审查并以分层方式细化判定:它先判断候选是否真正处于分裂或仅为伪影,然后对于确认的有丝分裂,选择最可能的阶段。系统使用针对病理图像设计的数据增强策略,帮助其应对不同实验室在染色和扫描设备上的差异。
在不同设置下测试性能
为公平评估其方法的效果,研究者遵循了先前有丝分裂检测挑战中使用的相同评估规则。他们测量算法预测的细胞在小距离内与专家绘制的细胞匹配的频率,同时考虑漏检和误报情况。训练在扩展后的 MIDOG++ 数据的一部分上进行,而新的 LUNG‑MITO 幻灯片被保留为独立测试集,以探查该方法对肿瘤类型与成像硬件变化的鲁棒性。增强的主干网络和细化步骤明显优于更传统的系统,既提升了整体检测能力,也提高了各类分裂亚型的识别准确性。
这对癌症护理和研究意味着什么
对于非专业读者来说,主要信息是该研究同时提供了详尽的公开数据集和更强大的 AI 模型,用于识别癌细胞如何以及何时分裂。通过训练算法区分不同的有丝分裂阶段并标记非典型分裂,以及展示该能力可以在多样的肿瘤与扫描条件下更可靠地实现,这项工作为未来支持病理学家对肿瘤分级和研究肿瘤生物学的工具奠定了基础。从长远看,这类工具可能有助于提高不同医院之间癌症诊断的一致性,并开辟将分裂细胞外观与其分子行为和患者结局关联的新研究方向。
引用: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
关键词: 数字病理学, 细胞分裂, 有丝分裂检测, 癌症成像, 医学人工智能