Clear Sky Science · ru
Набор данных митотических клеток с пометками субфаз для анализа деления клеток с помощью ИИ
Почему важно подсчитывать делящиеся клетки
Когда врачи изучают рак под микроскопом, одним из важнейших ориентиров является число клеток, находящихся в процессе деления. Быстро делящиеся опухоли часто ведут себя более агрессивно и могут требовать иного подхода к лечению. Тем не менее обнаружение этих крошечных делящихся клеток — медленная и утомительная работа для патологов, и даже эксперты часто расходятся во мнениях. В этом исследовании представлен новый, детально аннотированный набор изображений и улучшенный метод искусственного интеллекта (ИИ), призванный помочь компьютерам более надежно находить и классифицировать делящиеся клетки в различных типах рака и в больницах с разным оборудованием.
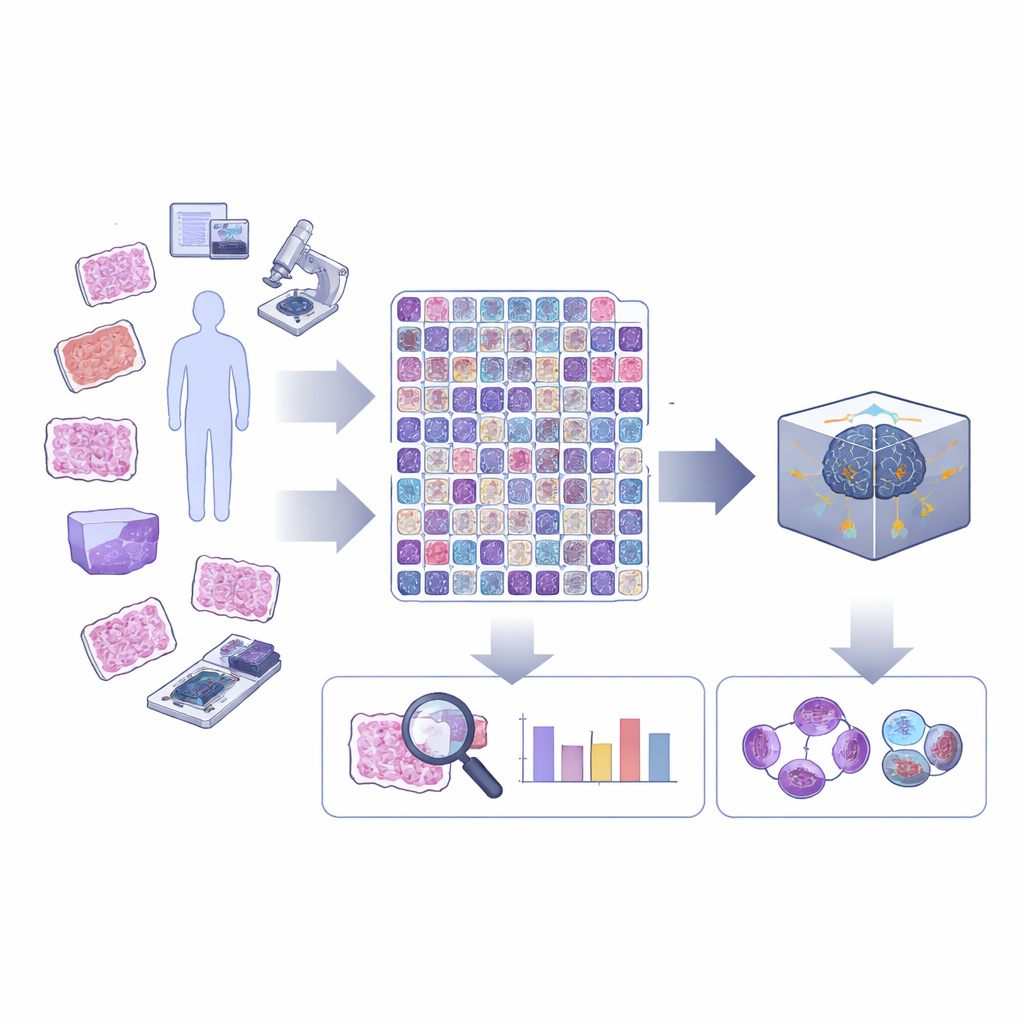
Взгляд поближе на деление клеток в опухолевой ткани
Деление клетки, или митоз, проходит в серии стадий, когда генетический материал удваивается и расходится. В рутинной диагностике большинство компьютерных инструментов помечают «митотические фигуры» как одну категорию, не учитывая, на какой стадии они находятся и выглядят ли они атипично. Между тем необычные или «атипичные» деления и соотношение ранних и поздних стадий могут нести важную информацию о злокачественности опухоли. Авторы утверждают, что ИИ достигнет полного потенциала в патологии лишь тогда, когда сможет распознавать те тонкие различия, на которые человеческие специалисты уже обращают внимание под микроскопом.
Создание более богатой библиотеки изображений
Чтобы выйти за рамки простого ответа «да/нет» для делящихся клеток, команда расширила существующий крупный эталонный набор под названием MIDOG++, который уже охватывал несколько типов опухолей, видов и сканирующих устройств. Экспертные аннотаторы пересмотрели более десяти тысяч митотических фигур и отнесли каждую к одной из пяти основных стадий нормального деления, а также выделили отдельный класс для атипичных митозов. Они также обвели каждую клетку точным контуром, а не только примерно в рамке. Эта тщательная работа превращает набор данных в ресурс, который может поддержать как более точное обучение ИИ, так и будущие исследования формы и структуры клетки во время деления.
Добавление нового набора данных по раку лёгкого
Понимая, что системы ИИ часто ухудшают результаты при переносе в другую больницу или к другому органу, исследователи также создали новый набор данных по аденокарциноме лёгкого, одному из распространённых и смертельно опасных типов рака лёгкого. Вместо того чтобы фокусироваться только на «горячих» областях с наибольшей активностью, они выделили всю область опухоли на каждом слайде, разбили её на удобные для обработки плитки и кропотливо промаркировали делящиеся клетки, атипичные деления и схожие по внешнему виду, но не делящиеся клетки. Этот набор LUNG‑MITO представляет собой жесткое, близкое к реальной практике испытание того, сможет ли алгоритм, обученный на других данных, адекватно работать на новых тканях и со сканерами иного типа.
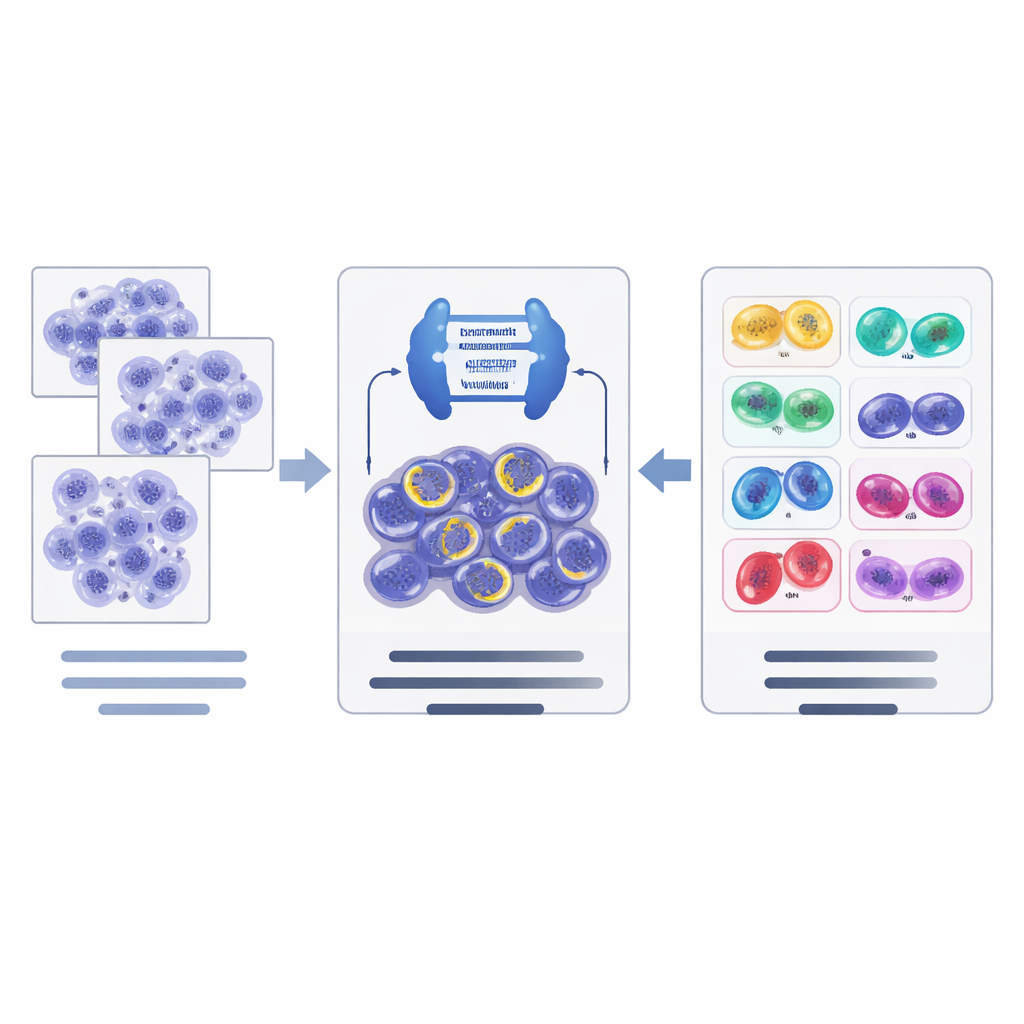
Как работает новый конвейер ИИ
На базе этих данных авторы спроектировали двухэтапный ИИ-конвейер. Сначала мощная сеть сегментации изображений на базе современной архитектуры ConvNeXt в сочетании с Mask R‑CNN просматривает плитки ткани и предлагает кандидатов в делящиеся клетки, обводя каждую и давая первоначальную оценку её стадии. Затем отдельная сеть классификации (EfficientNet) внимательно анализирует эти кандидаты и уточняет решение по иерархическому принципу: сначала она решает, действительно ли кандидат делится или является имитатором, а затем для подтверждённых митозов выбирает наиболее вероятную стадию. Система использует приёмы аугментации данных, адаптированные к патологическим изображениям, чтобы лучше справляться с различиями в окрашивании и сканерах между лабораториями.
Тестирование работы в разных условиях
Чтобы справедливо оценить эффективность подхода, исследователи следовали тем же правилам валидации, что и в предыдущих соревнованиях по обнаружению митозов. Они измеряли, как часто предсказанные алгоритмом клетки совпадают с клетками, обведёнными экспертами, в пределах малого расстояния, учитывая как пропущенные находки, так и ложные срабатывания. Обучение проводилось на части расширенных данных MIDOG++, тогда как слайды из нового LUNG‑MITO были отложены в качестве отдельного теста, чтобы проверить, насколько метод устойчив к изменениям в типе опухоли и оборудовании для сканирования. Усиленная «спина» сети и этап уточнения явно улучшили результаты по сравнению с более традиционной системой, повысив как общую детекцию, так и точность для каждого подтипа митоза.
Что это значит для ухода за больными и исследований
Для неспециалистов главный вывод таков: в работе представлен одновременно подробный открытый набор данных и более мощная модель ИИ для распознавания того, как и когда делятся раковые клетки. Обучая алгоритмы различать стадии митоза и отмечать атипичные деления, а также показывая, что это можно выполнять более надёжно для разных опухолей и сканеров, исследование закладывает основу для будущих инструментов, которые помогут патологам при грейдинге опухолей и изучении их биологии. В долгосрочной перспективе такие инструменты могут сделать диагнозы рака более согласованными между больницами и открыть новые направления исследований, связывающих внешний вид делящихся клеток с их молекулярным поведением и исходами для пациентов.
Цитирование: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Ключевые слова: цифровая патология, деление клеток, обнаружение митоза, изображения рака, медицинский ИИ