Clear Sky Science · sv
En mitos‑dataset märkt efter delningssubfaser för AI‑driven analys av celldelning
Varför det är viktigt att räkna delande celler
När läkare granskar cancer i mikroskop är en av de viktigaste ledtrådarna hur många celler som faktiskt håller på att dela sig. Snabbt delande tumörer beter sig ofta mer aggressivt och kan kräva annan behandling. Att upptäcka dessa små delande celler är dock långsamt och uttröttande arbete för patologer, och även experter kan ofta vara oense. Denna studie presenterar ett nytt, rikligt annoterat bilddataset och en förbättrad artificiell intelligens (AI)-metod som är avsedd att hjälpa datorer att hitta och förstå dessa delande celler mer tillförlitligt över många cancerformer och sjukhus.
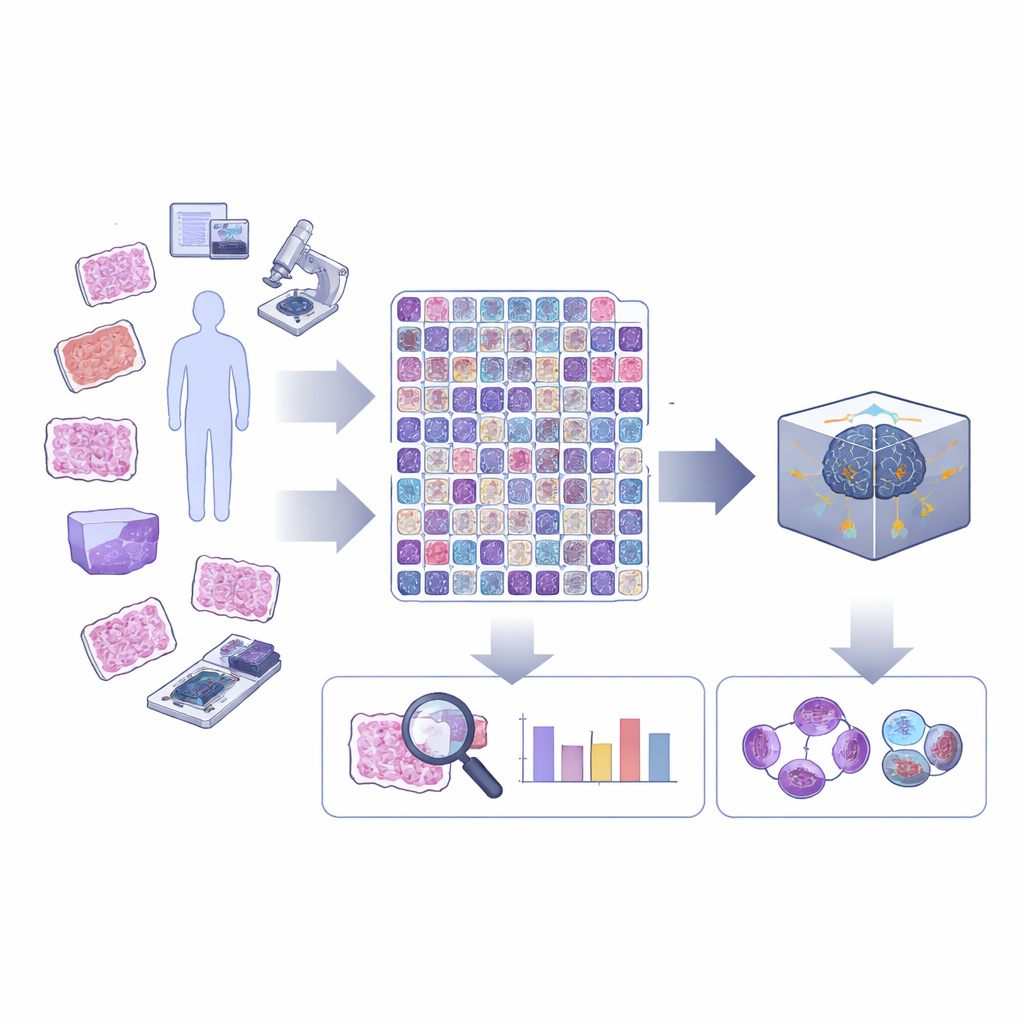
Närmare granskning av celldelning i cancervävnad
Celldelning, eller mitos, sker i flera stadier när cellens genetiska material kopieras och dras isär. I rutinmässig cancerdiagnostik markerar de flesta datorverktyg helt enkelt ”mitotiska figurer” som en enda kategori, utan att ta hänsyn till i vilket stadium de är eller om de ser abnorma ut. Ovanliga eller ”atypiska” delningar, och balansen mellan tidiga och sena stadier, kan dock ge viktig information om hur farlig en tumör är. Författarna hävdar att AI bara når sin fulla potential i patologin om den kan urskilja dessa finare skillnader som mänskliga specialister redan söker efter i mikroskopet.
Bygga ett rikare bildbibliotek
För att gå bortom ett enkelt ja‑/nej‑perspektiv på delande celler utökade teamet en befintlig stor benchmark känd som MIDOG++, som redan täckte flera tumörtyper, arter och skanningsenheter. Expertannotatörer granskade över tiotusen mitotiska figurer och tilldelade varje en till en av de fem huvudfaserna i normal celldelning, plus en separat klass för atypiska mitoser. De ritade också precisa konturer runt varje cell, inte bara grova rutor. Detta noggranna arbete förvandlar datasetet till en resurs som kan stödja både mer exakt AI‑träning och framtida studier av cellform och struktur under delning.
En nytt dataset för lungcancer
Medvetna om att AI‑system ofta havererar när de flyttas från ett sjukhus eller organ till ett annat, skapade forskarna även ett nytt dataset från lungadenokarcinom, en vanlig och dödlig form av lungcancer. Istället för att fokusera endast på de ”varmaste” regionerna med mest aktivitet valde de hela tumörområdet på varje preparat, delade upp det i hanterbara bildflikar och märkte mödosamt upp delande celler, atypiska delningar och liknande men icke‑delande celler. Detta LUNG‑MITO‑dataset ger ett krävande, verklighetsnära test av om en algoritm som tränats annorstädes fortfarande kan prestera väl när den ställs inför ny vävnad och nya skanningsförhållanden.
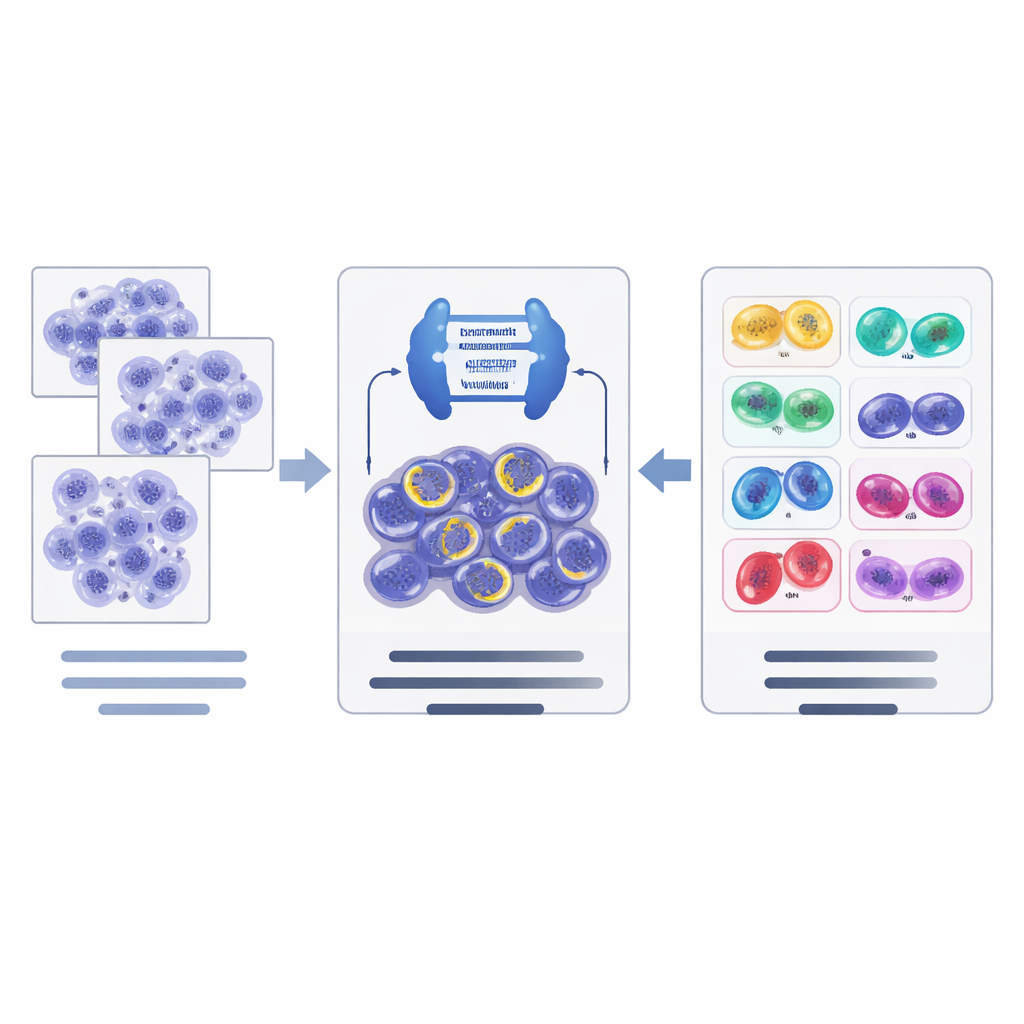
Hur den nya AI‑pipelinjen fungerar
På toppen av dessa dataresurser utvecklade författarna en tvåstegs AI‑pipeline. Först skannar ett kraftfullt bildsegmenteringsnätverk, baserat på en modern arkitektur kallad ConvNeXt kombinerad med Mask R‑CNN, vävnadsflikar och föreslår kandidat‑delande celler, konturerar varje en och ger en initial gissning om dess fas. Sedan granskar ett separat klassificeringsnätverk (EfficientNet) dessa kandidater närmare och förfinar beslutet i en hierarkisk ordning: först bedöms om en kandidat verkligen delar sig eller bara är en bedragare, och sedan, för bekräftade mitoser, väljs det mest sannolika stadiet. Systemet använder dataaugmenteringstrick skräddarsydda för patologibilder för att hjälpa det hantera skillnader i färgning och skannrar mellan laboratorier.
Testa prestanda i olika miljöer
För att rättvist bedöma hur bra deras metod fungerar följde forskarna samma utvärderingsregler som använts i tidigare utmaningar för mitosdetektion. De mätte hur ofta algoritmens förutsagda celler matchade expert‑ritade celler inom ett litet avstånd, vilket tar hänsyn både till missade upptäckter och falsklarm. Träningen gjordes på en del av den utökade MIDOG++‑datan, medan de nya LUNG‑MITO‑preparaten hölls tillbaka som ett separat test för att undersöka hur robust metoden är mot förändringar i tumörtyp och avbildningshårdvara. Den förbättrade ryggraden och förfiningssteget förbättrade tydligt prestandan jämfört med ett mer traditionellt system, och ökade både den övergripande detekteringen och noggrannheten för varje delningssubtyp.
Vad detta betyder för cancerbehandling och forskning
För icke‑specialister är huvudbudskapet att studien levererar både ett detaljerat öppet dataset och en starkare AI‑modell för att känna igen hur och när cancerceller delar sig. Genom att lära algoritmer att skilja mellan olika stadier i mitos och att flagga atypiska delningar, och genom att visa att detta kan göras mer tillförlitligt över olika tumörer och skannrar, lägger arbetet grunden för framtida verktyg som stödjer patologer vid tumörgrading och studier av tumörbiologi. På lång sikt kan sådana verktyg bidra till att göra cancerdiagnoser mer konsekventa mellan sjukhus och öppna nya forskningsvägar som kopplar delande cellers utseende till deras molekylära beteende och patientresultat.
Citering: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Nyckelord: digital patologi, celldelning, mitosdetektion, canceravbildning, medicinsk AI