Clear Sky Science · de
Ein mit Subphasen gekennzeichnetes Mitose‑Datenset für KI‑gestützte Zellteilungsanalyse
Warum das Zählen sich teilender Zellen wichtig ist
Wenn Ärzte Krebs im Mikroskop betrachten, gehört eine der wichtigsten Hinweise dazu, wie viele Zellen sich gerade teilen. Schnell teilende Tumoren verhalten sich oft aggressiver und können andere Behandlungsansätze erfordern. Das Auffinden dieser winzigen teilenden Zellen ist jedoch zeitaufwendig und ermüdend für Pathologinnen und Pathologen, und selbst Expertinnen stimmen häufig nicht überein. Diese Studie stellt ein neues, reich annotiertes Bilddatenset und eine verbesserte künstliche Intelligenz (KI) vor, die Computern helfen soll, diese teilenden Zellen über verschiedene Krebsarten und Krankenhäuser hinweg zuverlässiger zu erkennen und zu verstehen.
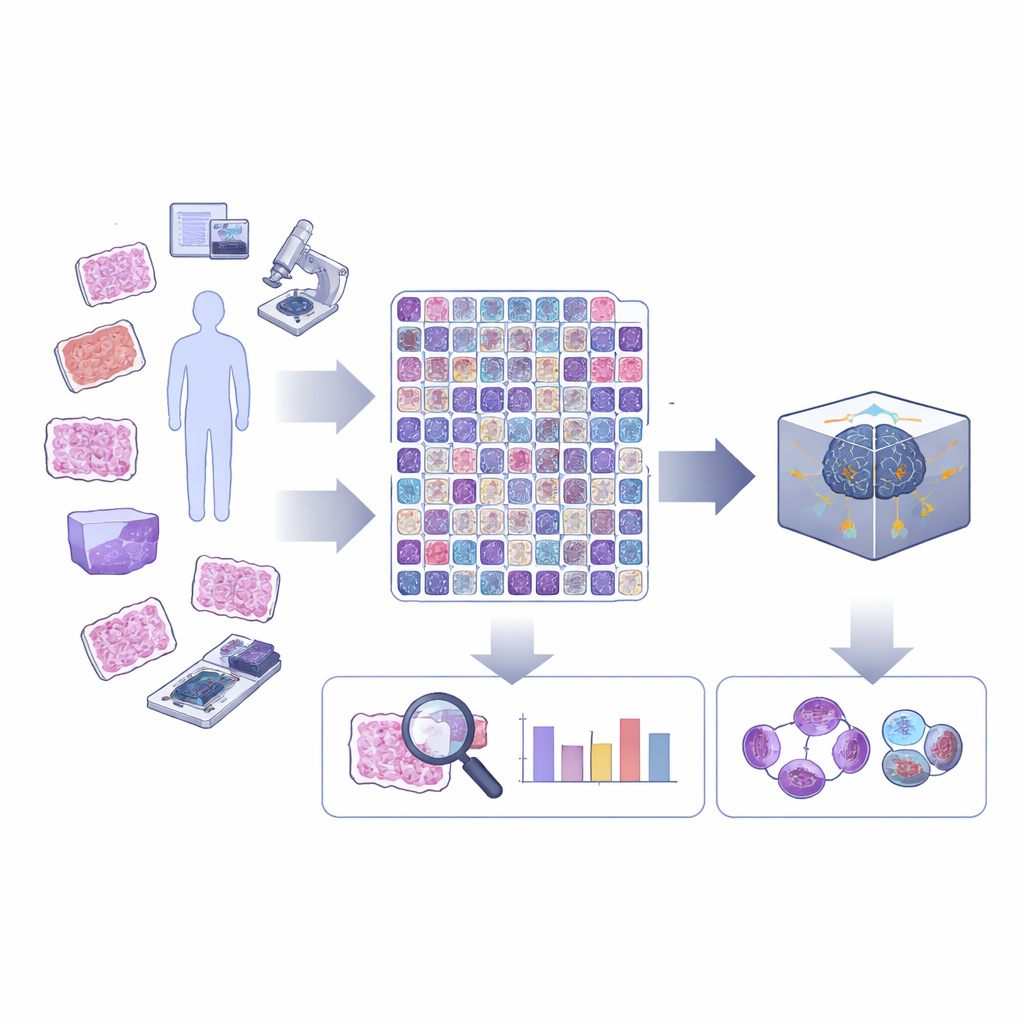
Ein genauerer Blick auf Zellteilung im Tumorgewebe
Zellteilung oder Mitose verläuft in einer Abfolge von Stadien, während das genetische Material der Zelle verdoppelt und getrennt wird. In der routinemäßigen Krebsdiagnostik markieren die meisten Computerwerkzeuge „mitotische Figuren“ einfach als eine einzige Kategorie und ignorieren, in welchem Stadium sie sich befinden oder ob sie ungewöhnlich aussehen. Abnorme oder „atypische“ Teilungen sowie das Verhältnis zwischen frühen und späten Stadien können jedoch wichtige Informationen über die Gefährlichkeit eines Tumors liefern. Die Autoren argumentieren, dass KI ihr volles Potenzial in der Pathologie nur ausschöpfen kann, wenn sie diese feineren Unterscheidungen erkennen kann, auf die menschliche Spezialisten bereits im Mikroskop achten.
Aufbau einer reichhaltigeren Bildbibliothek
Um über eine einfache Ja‑/Nein‑Sicht auf teilende Zellen hinauszukommen, erweiterten die Forschenden ein bestehendes großes Benchmark‑Set namens MIDOG++, das bereits mehrere Tumortypen, Spezies und Scanner abdeckte. Expertinnen und Experten überprüften mehr als zehntausend mitotische Figuren und ordneten jede einer der fünf Hauptphasen normaler Zellteilung zu sowie einer separaten Klasse für atypische Mitosen. Außerdem zogen sie präzise Umrisse um jede Zelle, nicht nur grobe Kästchen. Diese sorgfältige Arbeit verwandelt das Datenset in eine Ressource, die sowohl exakteres KI‑Training als auch künftige Studien zur Zellform und Struktur während der Teilung unterstützt.
Ergänzung durch ein neues Lungenkrebs‑Datenset
Da KI‑Systeme oft Probleme haben, wenn sie von einem Krankenhaus oder Organtyp auf einen anderen übertragen werden, erstellten die Forschenden außerdem ein neues Datenset aus Adenokarzinomen der Lunge, einer häufigen und tödlichen Form von Lungenkrebs. Anstatt sich nur auf die „heißesten“ Regionen mit der höchsten Aktivität zu konzentrieren, wählten sie das gesamte Tumorgebiet auf jedem Objektträger aus, teilten es in handhabbare Bildausschnitte und kennzeichneten mühsam teilende Zellen, atypische Teilungen und täuschend ähnliche, aber nicht teilende Zellen. Dieses LUNG‑MITO‑Datenset stellt einen harten, realitätsnahen Test dar, ob ein anderswo trainierter Algorithmus auch bei neuen Gewebe‑ und Scannerbedingungen noch gute Leistungen erbringt.
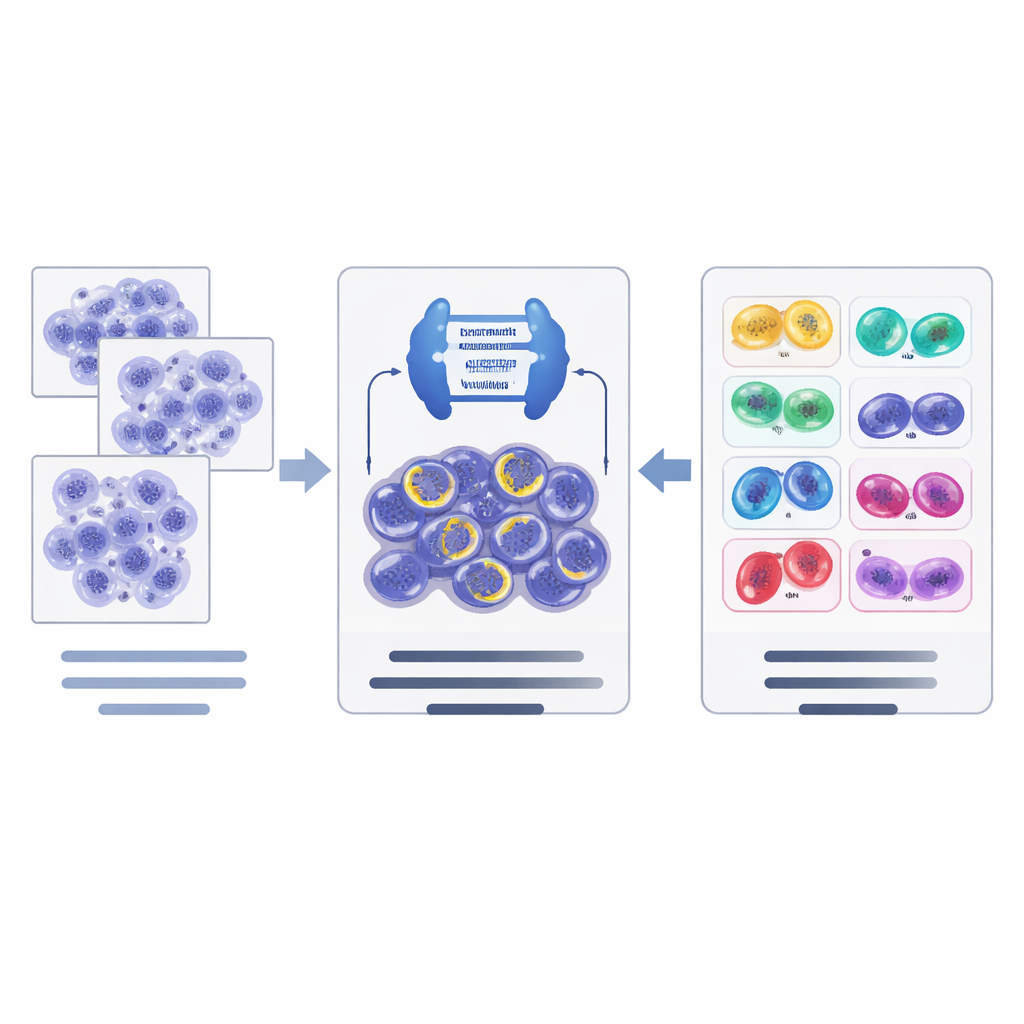
Wie die neue KI‑Pipeline funktioniert
Aufbauend auf diesen Datenressourcen entwarfen die Autoren eine zweistufige KI‑Pipeline. Zuerst durchsucht ein leistungsfähiges Bildsegmentierungsnetzwerk, basierend auf einer modernen Architektur namens ConvNeXt kombiniert mit Mask R‑CNN, Gewebeausschnitte und schlägt Kandidaten für teilende Zellen vor, zeichnet deren Umrisse nach und gibt eine erste Einschätzung ihres Stadiums. Anschließend betrachtet ein separates Klassifikationsnetzwerk (EfficientNet) diese Kandidaten genauer und verfeinert die Entscheidung hierarchisch: Zuerst beurteilt es, ob ein Kandidat tatsächlich teilend ist oder nur ein Täuschungsbild, und dann wählt es für bestätigte Mitosen das wahrscheinlichste Stadium. Das System nutzt Datenaugmentierungs‑Tricks, die auf pathologische Bilder zugeschnitten sind, um mit Unterschieden in Färbung und Scannern zwischen Laboren besser zurechtzukommen.
Leistungsprüfung in unterschiedlichen Settings
Um die Leistung ihres Ansatzes fair zu bewerten, hielten sich die Forschenden an dieselben Bewertungsregeln, die in früheren Mitose‑Erkennungswettbewerben verwendet wurden. Sie maßen, wie oft die vom Algorithmus vorhergesagten Zellen den von Expertinnen und Experten gezeichneten Zellen innerhalb einer kleinen Distanz entsprachen, wobei sowohl verpasste Erkennungen als auch Fehlalarme berücksichtigt wurden. Das Training erfolgte auf einem Teil der erweiterten MIDOG++‑Daten, während die neuen LUNG‑MITO‑Objektträger als separater Test zurückgehalten wurden, um zu prüfen, wie robust die Methode gegenüber Änderungen von Tumortyp und Bildgebungs‑Hardware ist. Der verbesserte Backbone und der Verfeinerungsschritt verbesserten die Leistung deutlich gegenüber einem traditionelleren System und steigerten sowohl die Gesamtentdeckung als auch die Genauigkeit für jeden Subtyp der Zellteilung.
Was das für Krebsversorgung und Forschung bedeutet
Für Nicht‑Fachleute lautet die Hauptbotschaft, dass die Studie sowohl ein detailliertes öffentliches Datenset als auch ein stärkeres KI‑Modell zur Erkennung, wie und wann Krebszellen sich teilen, liefert. Indem Algorithmen beigebracht werden, verschiedene Mitose‑Stadien zu unterscheiden und atypische Teilungen zu markieren — und gezeigt wird, dass dies über unterschiedliche Tumoren und Scanner hinweg zuverlässiger möglich ist —, schafft die Arbeit Grundlagen für künftige Werkzeuge, die Pathologinnen und Pathologen bei der Tumorgrading und der Erforschung ihrer Biologie unterstützen. Langfristig könnten solche Werkzeuge dazu beitragen, Krebsdiagnosen zwischen Krankenhäusern konsistenter zu machen und neue Forschungsrichtungen zu eröffnen, die das Erscheinungsbild teilender Zellen mit ihrem molekularen Verhalten und Patientenergebnissen verknüpfen.
Zitation: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Schlüsselwörter: digitale Pathologie, Zellteilung, Mitose‑Erkennung, Krebsbildgebung, medizinische KI