Clear Sky Science · fr
Un jeu de données mitotique étiqueté par sous‑phase pour l’analyse automatisée de la division cellulaire
Pourquoi compter les cellules en division est important
Quand les médecins examinent un cancer au microscope, l’un des indices les plus importants est le nombre de cellules en train de se diviser. Les tumeurs à division rapide se comportent souvent de façon plus agressive et peuvent nécessiter des traitements différents. Pourtant, repérer ces minuscules cellules en division est un travail lent et fatigant pour les pathologistes, et même les experts sont souvent en désaccord. Cette étude présente un nouveau jeu d’images richement annoté et une méthode d’intelligence artificielle (IA) améliorée conçue pour aider les ordinateurs à repérer et à comprendre ces cellules en division de manière plus fiable à travers de nombreux types de cancers et d’hôpitaux.
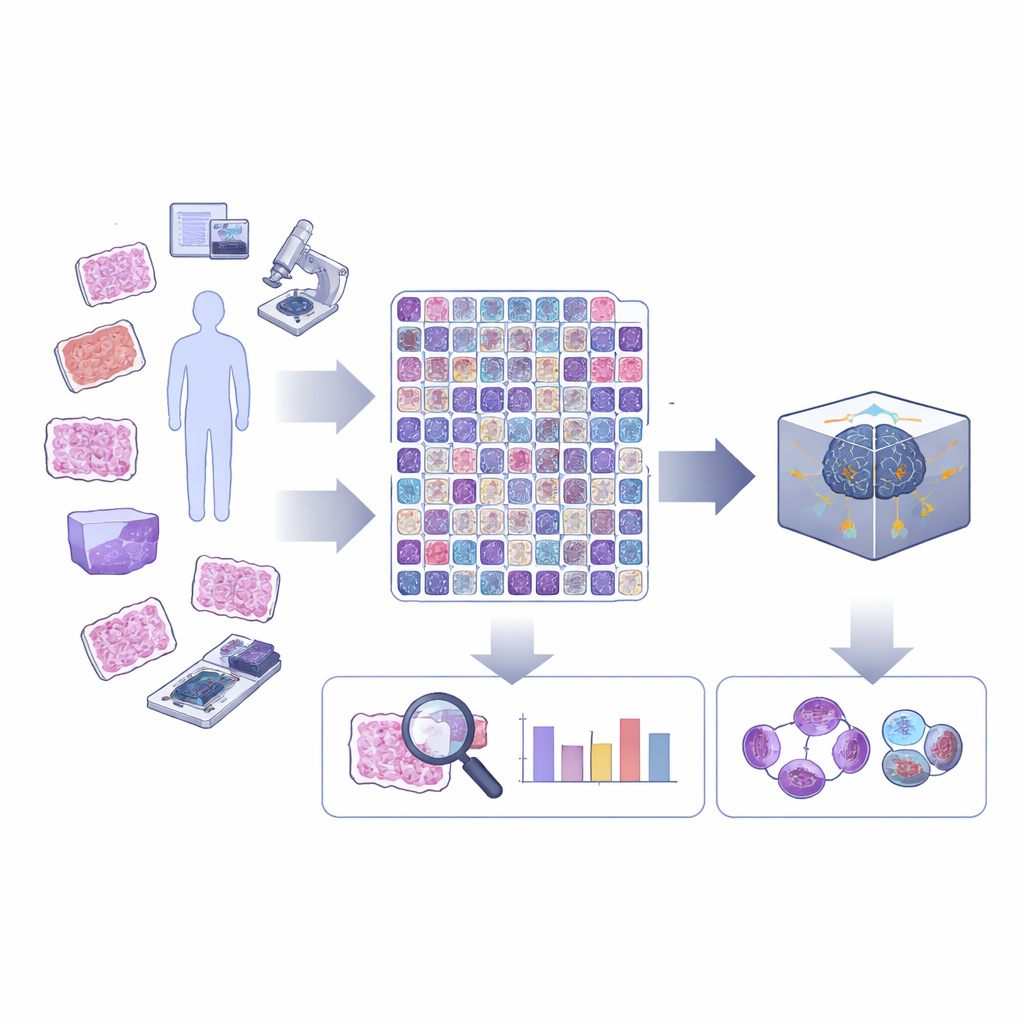
Un regard plus précis sur la division cellulaire dans le tissu cancéreux
La division cellulaire, ou mitose, se déroule en une série d’étapes lorsque le matériel génétique de la cellule est dupliqué et séparé. Dans le diagnostic courant du cancer, la plupart des outils informatiques se contentent de marquer les « figures mitotiques » comme une seule catégorie, sans tenir compte de la phase ni de l’aspect anormal éventuel. Or, les divisions inhabituelles ou « atypiques », ainsi que l’équilibre entre les phases précoces et tardives, peuvent fournir des informations importantes sur le niveau de dangerosité d’une tumeur. Les auteurs soutiennent que l’IA n’atteindra son plein potentiel en pathologie que si elle peut percevoir ces distinctions fines que les spécialistes humains cherchent déjà au microscope.
Construire une bibliothèque d’images plus riche
Pour aller au‑delà d’une vue binaire sur les cellules en division, l’équipe a étendu une référence existante de grande ampleur appelée MIDOG++, qui couvrait déjà plusieurs types de tumeurs, espèces et dispositifs de numérisation. Des annotateurs experts ont réexaminé plus de dix mille figures mitotiques et ont assigné chacune à l’une des cinq principales phases de la mitose normale, plus une classe séparée pour les mitoses atypiques. Ils ont aussi tracé des contours précis autour de chaque cellule, et non de simples boîtes approximatives. Ce travail minutieux transforme le jeu de données en une ressource pouvant soutenir à la fois un entraînement IA plus exact et des études futures sur la forme et la structure des cellules pendant la division.
Ajout d’un nouveau jeu de données sur le cancer du poumon
Conscients que les systèmes d’IA échouent souvent lorsqu’ils sont transférés d’un hôpital ou d’un organe à l’autre, les chercheurs ont également créé un nouveau jeu de données issu d’adénocarcinomes pulmonaires, une forme courante et mortelle de cancer du poumon. Plutôt que de se focaliser uniquement sur les régions « les plus chaudes » où l’activité est maximale, ils ont sélectionné l’intégralité de la zone tumorale sur chaque lame, l’ont découpée en tuiles d’images maniables et ont étiqueté avec soin les cellules en division, les divisions atypiques et les éléments ressemblant à des mitoses mais n’en étant pas. Ce jeu de données LUNG‑MITO offre un test difficile et réaliste pour savoir si un algorithme entraîné ailleurs peut encore bien fonctionner face à de nouveaux tissus et conditions de numérisation.
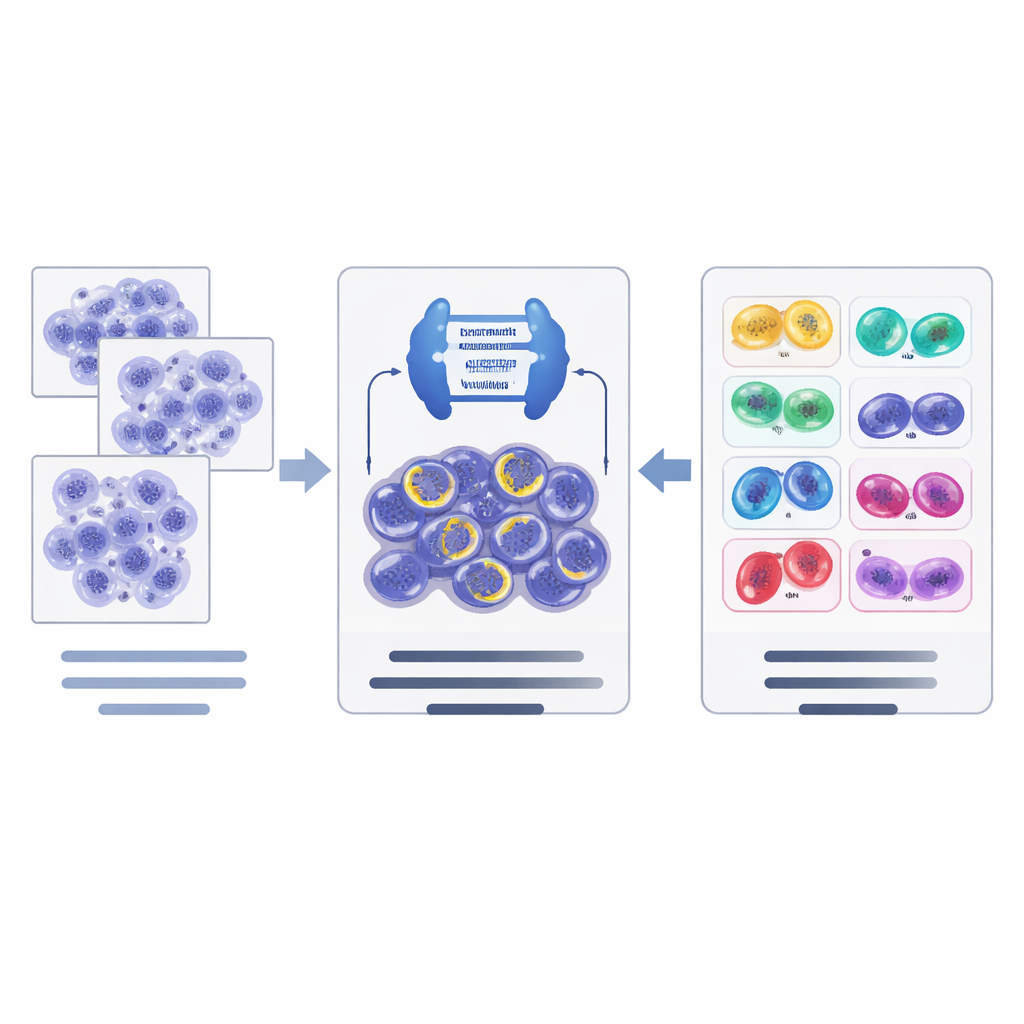
Comment fonctionne la nouvelle chaîne d’IA
Sur la base de ces ressources, les auteurs ont conçu une chaîne d’IA en deux étapes. D’abord, un puissant réseau de segmentation d’images, fondé sur une architecture moderne appelée ConvNeXt combinée à Mask R‑CNN, balaye les tuiles de tissu et propose des candidats cellules en division, en traçant le contour de chacune et en donnant une estimation initiale de sa phase. Ensuite, un réseau de classification séparé (EfficientNet) examine de plus près ces candidats et affine la décision de façon hiérarchique : il juge d’abord si un candidat est vraiment en division ou s’il s’agit d’un leurre, puis, pour les mitoses confirmées, choisit la phase la plus probable. Le système utilise des astuces d’augmentation des données adaptées aux images de pathologie pour l’aider à gérer les différences de coloration et de scanners entre laboratoires.
Évaluer la performance dans différents contextes
Pour juger équitablement de l’efficacité de leur approche, les chercheurs ont suivi les mêmes règles d’évaluation que celles utilisées dans les précédents défis de détection de mitoses. Ils ont mesuré la fréquence à laquelle les cellules prédites par l’algorithme coïncidaient avec les cellules annotées par les experts dans une petite distance, en tenant compte à la fois des détections manquées et des fausses alertes. L’entraînement a été réalisé sur une portion des données étendues MIDOG++, tandis que les lames LUNG‑MITO nouvelles ont été conservées comme jeu de test séparé pour évaluer la robustesse de la méthode face aux changements de type tumoral et de matériel d’imagerie. Le backbone amélioré et l’étape de raffinement ont clairement amélioré les performances par rapport à un système plus traditionnel, augmentant à la fois la détection globale et la précision pour chaque sous‑type de division cellulaire.
Ce que cela signifie pour les soins et la recherche en cancérologie
Pour les non‑spécialistes, le message principal est que l’étude fournit à la fois un jeu de données public détaillé et un modèle d’IA plus performant pour reconnaître comment et quand les cellules cancéreuses se divisent. En apprenant aux algorithmes à distinguer les différentes phases de la mitose et à signaler les divisions atypiques, et en montrant que cela peut être réalisé de façon plus fiable à travers des tumeurs et des scanners variés, le travail prépare le terrain pour des outils futurs qui aideront les pathologistes à graduer les tumeurs et à étudier leur biologie. À plus long terme, de tels outils pourraient contribuer à rendre les diagnostics du cancer plus cohérents d’un hôpital à l’autre et ouvrir de nouvelles pistes de recherche reliant l’apparence des cellules en division à leur comportement moléculaire et aux résultats pour les patients.
Citation: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Mots-clés: pathologie numérique, division cellulaire, détection de mitoses, imagerie du cancer, IA médicale