Clear Sky Science · es
Un conjunto de datos mitóticos etiquetado por subfases para el análisis de la división celular impulsado por IA
Por qué importa contar las células en división
Cuando los médicos examinan el cáncer al microscopio, una de las pistas más importantes que usan es cuántas células están en proceso de dividirse. Los tumores que se dividen rápidamente suelen comportarse con mayor agresividad y pueden requerir tratamientos distintos. Sin embargo, localizar estas pequeñas células en división es un trabajo lento y fatigoso para los patólogos, y hasta los expertos a menudo discrepan. Este estudio presenta un nuevo conjunto de imágenes ricamente anotado y un método de inteligencia artificial (IA) mejorado diseñado para ayudar a los ordenadores a encontrar y comprender estas células en división con mayor fiabilidad en múltiples tipos de cáncer y hospitales.
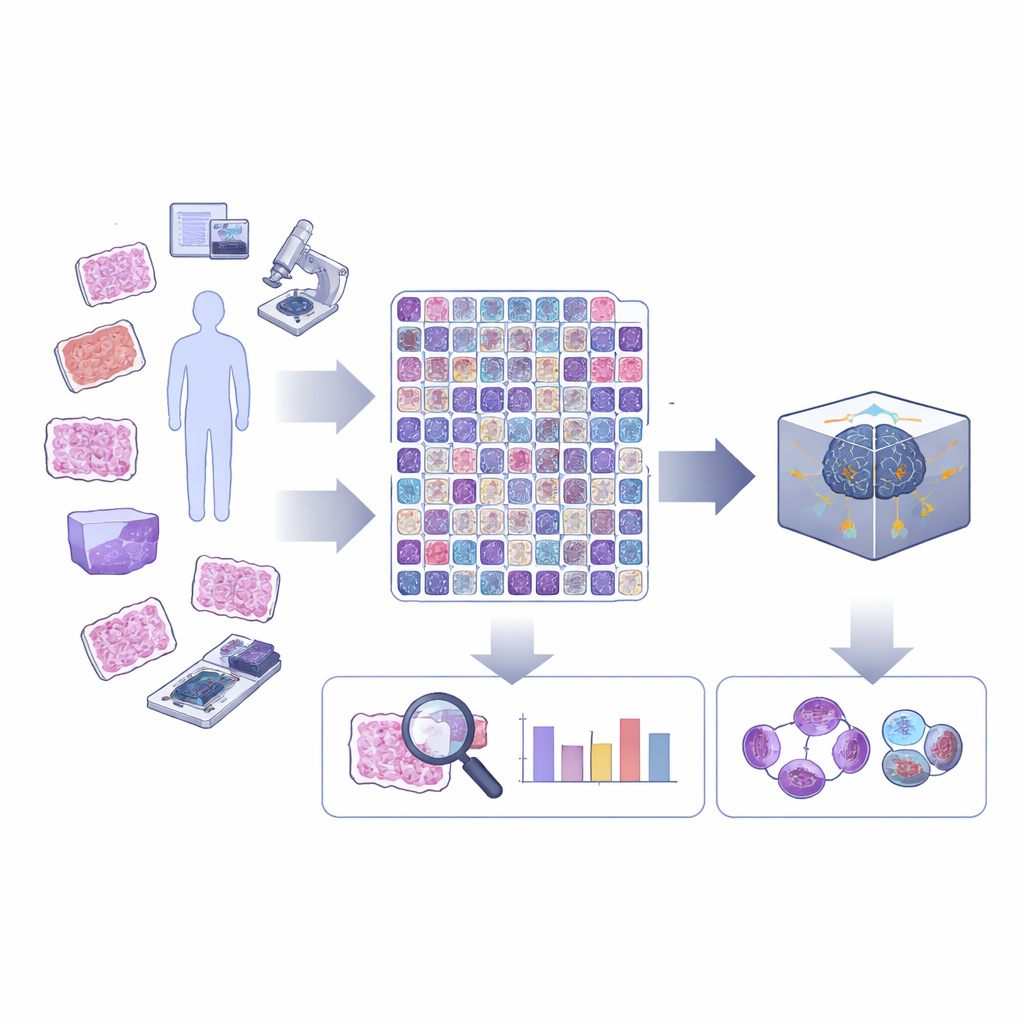
Una mirada más cercana a la división celular en tejido canceroso
La división celular, o mitosis, se desarrolla en una serie de etapas en las que el material genético de la célula se duplica y se separa. En el diagnóstico rutinario del cáncer, la mayoría de las herramientas informáticas simplemente marcan las “figuras mitóticas” como una sola categoría, sin distinguir en qué etapa se encuentran ni si presentan aspecto anómalo. Sin embargo, las divisiones inusuales o “atípicas”, y el equilibrio entre etapas tempranas y tardías, pueden aportar información importante sobre la peligrosidad de un tumor. Los autores sostienen que la IA alcanzará todo su potencial en patología solo si puede detectar estas distinciones más finas que los especialistas humanos ya buscan al microscopio.
Construir una biblioteca de imágenes más rica
Para ir más allá de una visión binaria sobre las células en división, el equipo amplió un gran banco de referencia existente conocido como MIDOG++, que ya abarcaba varios tipos de tumores, especies y dispositivos de escaneado. Anotadores expertos revisaron más de diez mil figuras mitóticas y asignaron cada una a una de las cinco etapas principales de la división celular normal, además de una clase separada para mitosis atípicas. También trazaron contornos precisos alrededor de cada célula, no solo cuadros aproximados. Este trabajo minucioso convierte al conjunto de datos en un recurso capaz de apoyar tanto un entrenamiento de IA más exacto como estudios futuros sobre la forma y la estructura celular durante la división.
Añadiendo un nuevo conjunto de datos de cáncer de pulmón
Reconociendo que los sistemas de IA a menudo fallan cuando se trasladan de un hospital o tipo de órgano a otro, los investigadores también crearon un nuevo conjunto de datos a partir de adenocarcinoma pulmonar, una forma común y letal de cáncer de pulmón. En lugar de centrarse solo en las regiones “más activas” con mayor número de divisiones, seleccionaron toda el área tumoral en cada portaobjetos, la dividieron en parches de imagen manejables y etiquetaron meticulosamente las células en división, las divisiones atípicas y células similares pero que no se están dividiendo. Este conjunto LUNG‑MITO ofrece una prueba difícil y realista de si un algoritmo entrenado en otros datos puede seguir rindiendo bien ante tejidos y condiciones de escáner nuevas.
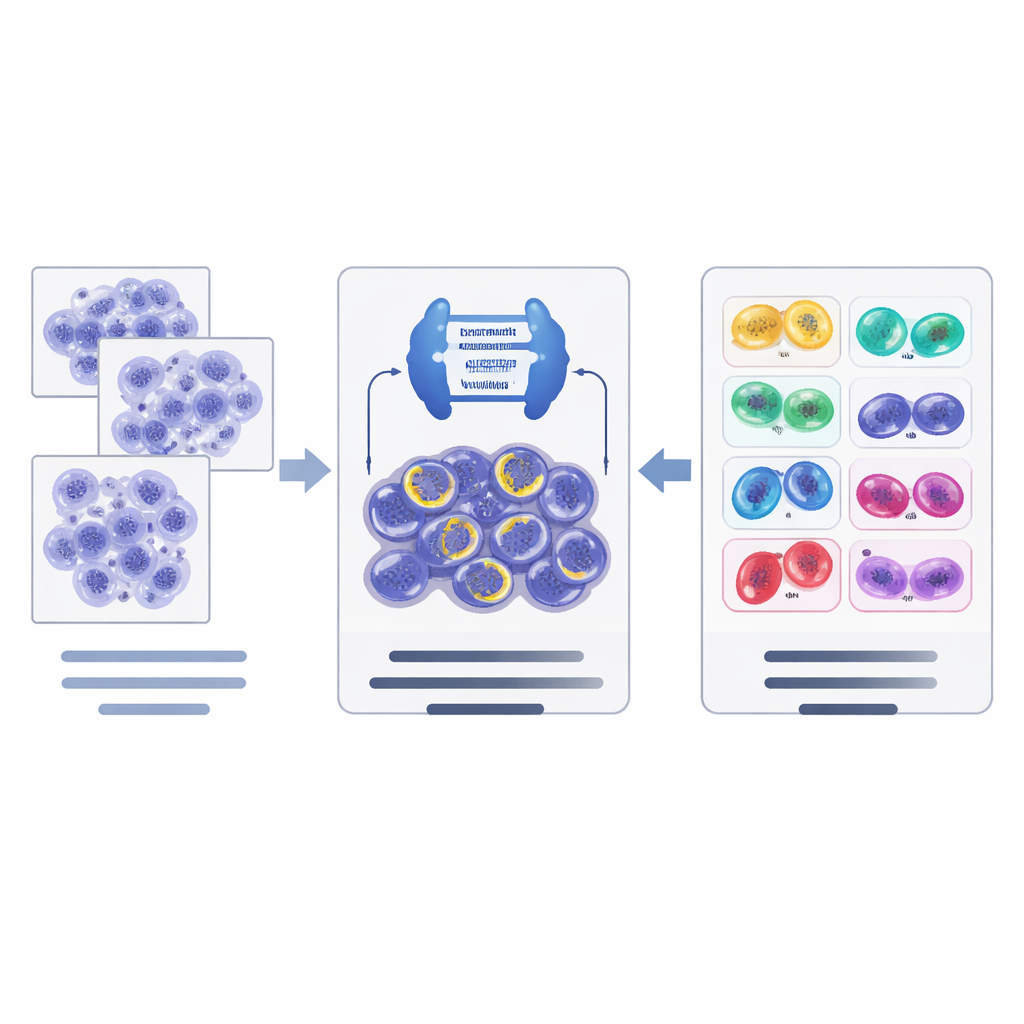
Cómo funciona la nueva canalización de IA
Sobre estos recursos de datos, los autores diseñaron una canalización de IA de dos pasos. Primero, una potente red de segmentación de imágenes, basada en una arquitectura moderna llamada ConvNeXt combinada con Mask R‑CNN, examina los mosaicos de tejido y propone candidatas a células en división, trazando su contorno y dando una estimación inicial de su subfase. Segundo, una red de clasificación separada (EfficientNet) examina con más detalle estas candidatas y refina la decisión de forma jerárquica: primero juzga si una candidata está realmente en división o es un impostor y, luego, para las mitosis confirmadas, selecciona la etapa más probable. El sistema emplea trucos de aumento de datos adaptados a imágenes de patología para ayudar a lidiar con las diferencias en tinción y escáneres entre laboratorios.
Evaluación del rendimiento en distintos entornos
Para juzgar de forma justa qué tan bien funciona su enfoque, los investigadores siguieron las mismas reglas de evaluación usadas en desafíos previos de detección de mitosis. Midieron con qué frecuencia las células predichas por el algoritmo coincidían con las células dibujadas por expertos dentro de una pequeña distancia, teniendo en cuenta tanto las detecciones perdidas como las falsas alarmas. El entrenamiento se realizó con una porción de los datos ampliados de MIDOG++, mientras que las nuevas diapositivas de LUNG‑MITO se reservaron como prueba separada para sondear qué tan robusto es el método ante cambios en el tipo de tumor y el hardware de imagen. La arquitectura mejorada y el paso de refinamiento mejoraron claramente el rendimiento frente a un sistema más tradicional, aumentando tanto la detección global como la precisión para cada subtipo de división celular.
Qué significa esto para la atención e investigación del cáncer
Para los no especialistas, el mensaje principal es que el estudio ofrece tanto un conjunto de datos público detallado como un modelo de IA más potente para reconocer cómo y cuándo se dividen las células cancerosas. Al enseñar a los algoritmos a distinguir entre distintas etapas de mitosis y a señalar divisiones atípicas, y al demostrar que esto puede hacerse con mayor fiabilidad en tumores y escáneres diversos, el trabajo sienta las bases para futuras herramientas que apoyen a los patólogos en la graduación de tumores y en el estudio de su biología. A largo plazo, dichas herramientas podrían ayudar a que los diagnósticos de cáncer sean más consistentes entre hospitales y abrir nuevas líneas de investigación que vinculen la apariencia de las células en división con su comportamiento molecular y los resultados en pacientes.
Cita: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Palabras clave: patología digital, división celular, detección de mitosis, imágenes del cáncer, IA médica