Clear Sky Science · tr
Yapay Zekâ Destekli Hücre Bölünmesi Analizi için Altfaz Etiketli Bir Mitotik Veri Kümesi
Bölen hücreleri saymanın önemi
Doktorlar kanseri mikroskop altında incelerken en önemli ipuçlarından biri, bölünme halinde olan hücre sayısıdır. Hızla bölünen tümörler genellikle daha agresif davranır ve farklı tedavi gerektirebilir. Ancak bu küçük bölünen hücreleri tespit etmek patologlar için yavaş ve yorucu bir iştir ve uzmanlar arasında bile sıklıkla görüş ayrılıkları olur. Bu çalışma, yeni, zengin anotasyonlu bir görüntü veri kümesi ve bilgisayarların bu bölünen hücreleri birçok kanser türü ve hastanede daha güvenilir şekilde bulup yorumlamasına yardımcı olmak üzere geliştirilmiş iyileştirilmiş bir yapay zekâ (YZ) yöntemini sunuyor.
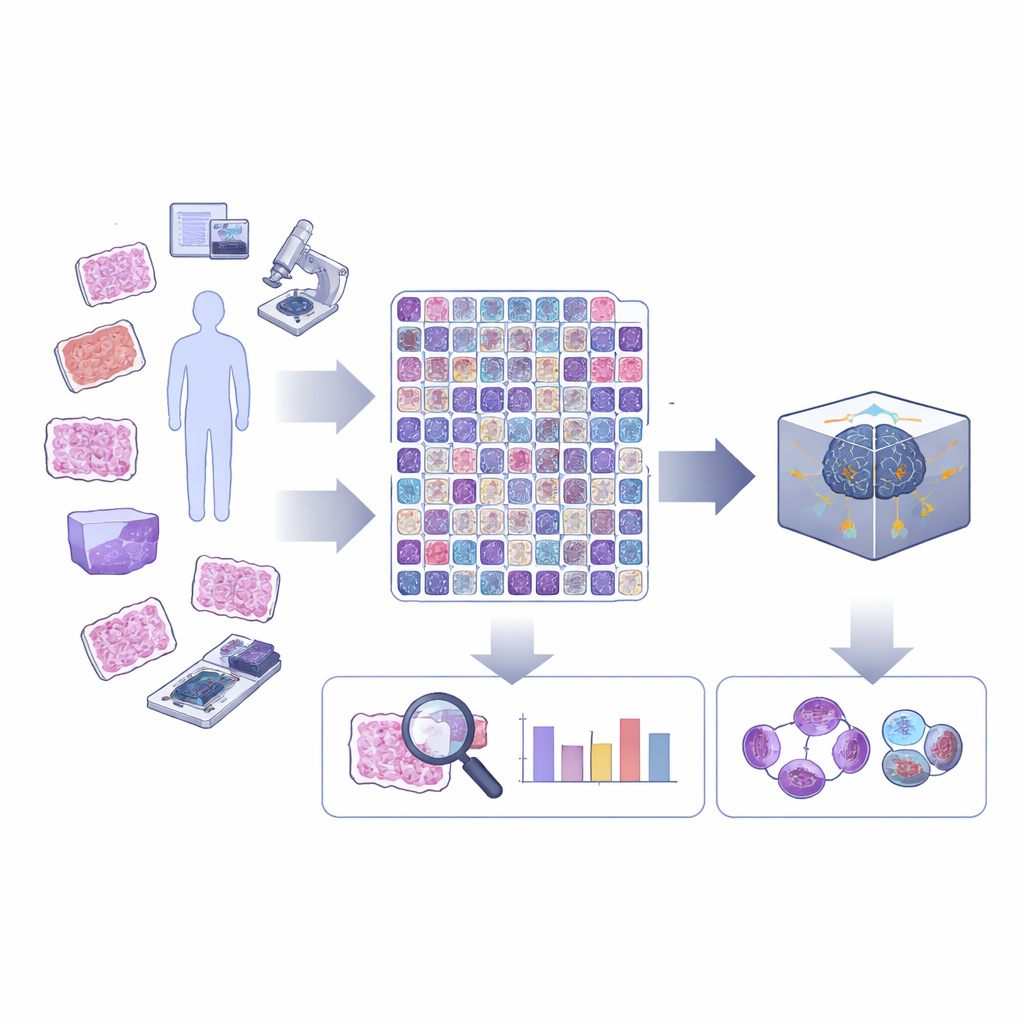
Kanser dokusunda hücre bölünmesine daha yakın bakış
Hücre bölünmesi veya mitoz, hücrenin genetik materyali kopyalanıp ayrılırken bir dizi aşamada gerçekleşir. Rutin kanser tanısında, çoğu bilgisayar aracı “mitotik yapı”ları tek bir kategori olarak işaretler; hangi aşamada oldukları veya anormal görünüp görünmedikleri genellikle göz ardı edilir. Oysa alışılmadık veya “atipik” bölünmeler ve erken ile geç aşamalar arasındaki denge, bir tümörün ne kadar tehlikeli olduğu hakkında önemli bilgiler taşıyabilir. Yazarlar, YZ’nin patolojide tam potansiyeline ulaşabilmesi için, insan uzmanların mikroskopta zaten aradığı bu ince ayrımları görebilmesi gerektiğini savunuyor.
Daha zengin bir görüntü kütüphanesi oluşturmak
Bölünen hücrelere basit bir evet‑hayır yaklaşımının ötesine geçmek için ekip, halihazırda birden çok tümör türünü, türü ve tarayıcı cihazını kapsayan büyük bir kıyaslama seti olan MIDOG++’u genişletti. Uzman anotatörler on binden fazla mitotik yapıyı yeniden gözden geçirerek her birini normal hücre bölünmesinin beş ana aşamasından birine veya ayrı bir atipik mitoz sınıfına atadılar. Ayrıca her hücrenin etrafına kaba kutular yerine hassas konturlar çizdiler. Bu titiz çalışma, veri kümesini hem daha doğru YZ eğitimi hem de bölünme sırasında hücre şekli ve yapısının gelecekteki çalışmaları için destekleyen bir kaynağa dönüştürüyor.
Yeni bir akciğer kanseri veri kümesi eklemek
YZ sistemlerinin bir hastaneden veya organ tipinden diğerine taşındığında sıkça sorun yaşadığını kabul eden araştırmacılar, yaygın ve ölümcül bir akciğer kanseri türü olan akciğer adenokarsinomundan yeni bir veri kümesi de oluşturdular. En çok aktivitenin olduğu “en sıcak” bölgeler yerine, her lam üzerindeki tüm tümör alanını seçtiler, bunu yönetilebilir görüntü yama parçalarına böldüler ve bölünen hücreleri, atipik bölünmeleri ve benzer görünüp bölünmeyen hücreleri titizlikle etiketlediler. Bu LUNG‑MITO veri kümesi, başka yerde eğitilmiş bir algoritmanın yeni doku ve tarayıcı koşullarıyla karşılaştığında hâlâ iyi performans gösterip göstermediğini sınayan zorlu, gerçek dünya testi sunuyor.
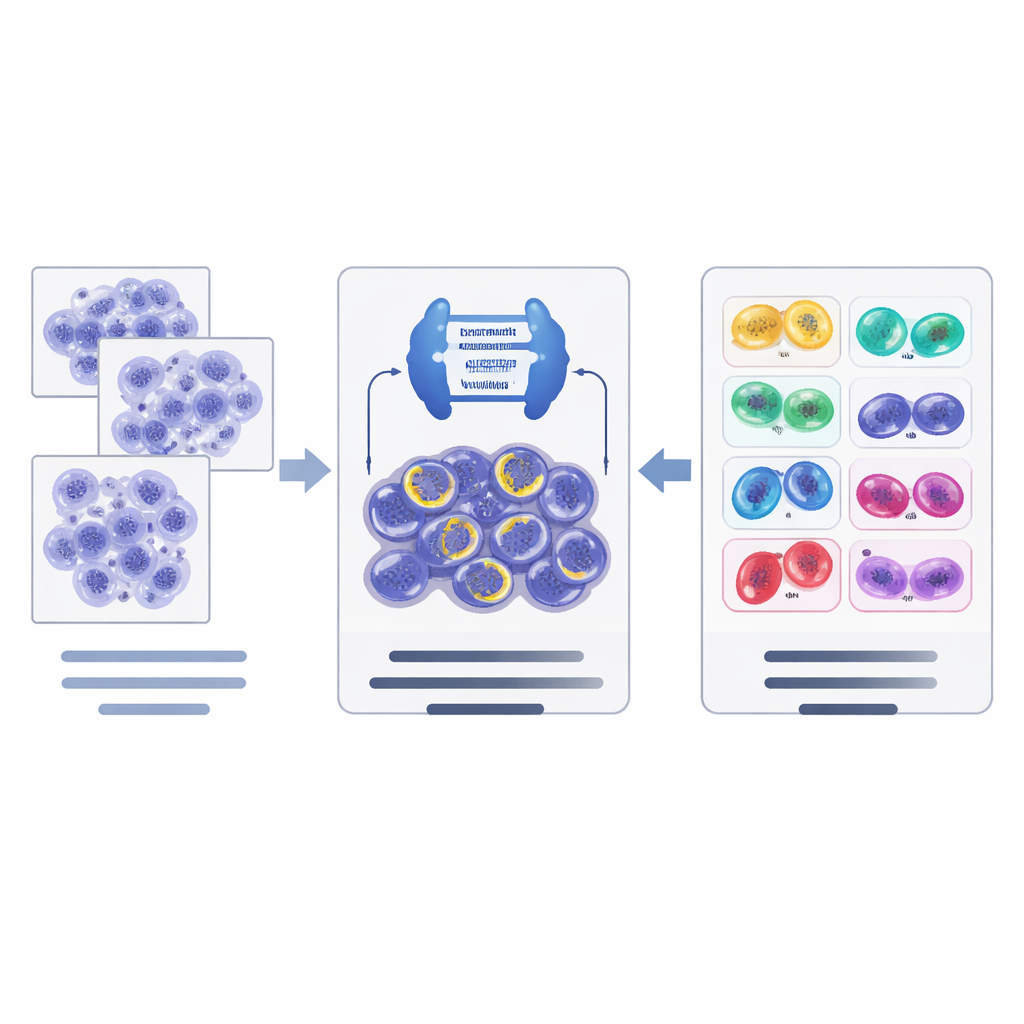
Yeni YZ hattının çalışma biçimi
Bu veri kaynaklarının üzerine yazarlar iki aşamalı bir YZ hattı tasarladılar. İlk olarak, ConvNeXt tabanlı modern bir mimari ile Mask R‑CNN’in birleşimine dayanan güçlü bir görüntü segmentasyon ağı, doku yamalarını tarar ve aday bölünen hücreleri önerir; her birinin çevresini çizer ve başlangıç aşaması hakkında bir tahmin verir. İkinci olarak, ayrı bir sınıflandırma ağı (EfficientNet) bu adaylara daha yakından bakar ve hiyerarşik bir şekilde kararı rafine eder: önce bir adayın gerçekten bölünüp bölünmediğine veya bir taklit olup olmadığına karar verir, ardından teyit edilen mitozlar için en olası aşamayı seçer. Sistem, laboratuvarlar arasındaki boyama ve tarayıcı farklılıklarıyla başa çıkmasına yardımcı olmak için patoloji görüntülerine özgü veri çoğaltma (augmentation) hileleri kullanır.
Farklı ortamlarda performansı test etmek
Yaklaşımlarının ne kadar iyi çalıştığını adil şekilde değerlendirmek için araştırmacılar önceki mitoz tespiti yarışmalarında kullanılan aynı değerlendirme kurallarını izlediler. Algoritmanın tahmin ettiği hücrelerin, uzmanlar tarafından çizilmiş hücrelerle küçük bir mesafe içinde ne sıklıkla eşleştiğini ölçtüler; hem kaçırılan tespitleri hem de yanlış alarmları hesaba kattılar. Eğitim genişletilmiş MIDOG++ verisinin bir bölümünde yapıldı; yeni LUNG‑MITO lamları ise tümör türü ve görüntü donanımındaki değişikliklere karşı yöntemin sağlamlığını test etmek için ayrı bir sınav olarak ayrıldı. Geliştirilmiş omurga (backbone) ve rafine etme adımı, daha geleneksel bir sisteme kıyasla hem genel tespiti hem de her alt tür için doğruluğu açıkça artırdı.
Kanser bakımı ve araştırma için anlamı
Uzman olmayanlar için ana mesaj, çalışmanın hem ayrıntılı bir halka açık veri kümesi hem de kanser hücrelerinin nasıl ve ne zaman bölündüğünü tanımakta daha güçlü bir YZ modeli sunmasıdır. Algoritmaları mitozun farklı aşamalarını ayırt etmeyi ve atipik bölünmeleri işaretlemeyi öğretmek; ayrıca bunun farklı tümörler ve tarayıcılar arasında daha güvenilir şekilde yapılabileceğini göstermek, patologlara tümörleri derecelendirmede ve biyolojilerini incelemede yardımcı olacak gelecekteki araçların temelini atıyor. Uzun vadede, bu tür araçlar kanser tanılarını bir hastaneden diğerine daha tutarlı hale getirmeye yardımcı olabilir ve bölünen hücrelerin görünümünü moleküler davranışları ve hasta sonuçlarıyla ilişkilendiren yeni araştırma yönergelerinin önünü açabilir.
Atıf: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Anahtar kelimeler: dijital patoloji, hücre bölünmesi, mitoz tespiti, kanser görüntüleme, tıbbi yapay zekâ