Clear Sky Science · he
מאגר מידע מתויג לפי תתי‑שלבים של מיטוזה לניתוח חלוקת תאים מונע‑בינה מלאכותית
למה חשוב לספור תאים שמתחלקים
כשמנתחים סרטן תחת המיקרוסקופ, אחד הרמזים החשובים הוא כמה תאים נמצאים בתהליך החלוקה. גידולים שמתחלקים במהירות נוטים להתנהג באגרסיביות רבה יותר ועלולים לדרוש טיפול שונה. יחד עם זאת, זיהוי התאים הקטנים הללו עוסק בעבודה איטית ומתישה עבור פתולוגים, ואף מומחים יכולים לא להסכים ביניהם. המחקר הזה מציג מאגר תמונות חדש, מתויג בקפידה, ושיטה משופרת מבוססת בינה מלאכותית שנועדה לעזור למחשבים לאתר ולהבין תאים מתחלקים בצורה אמינה יותר עבור סוגי סרטן ומוסדות רפואיים שונים.
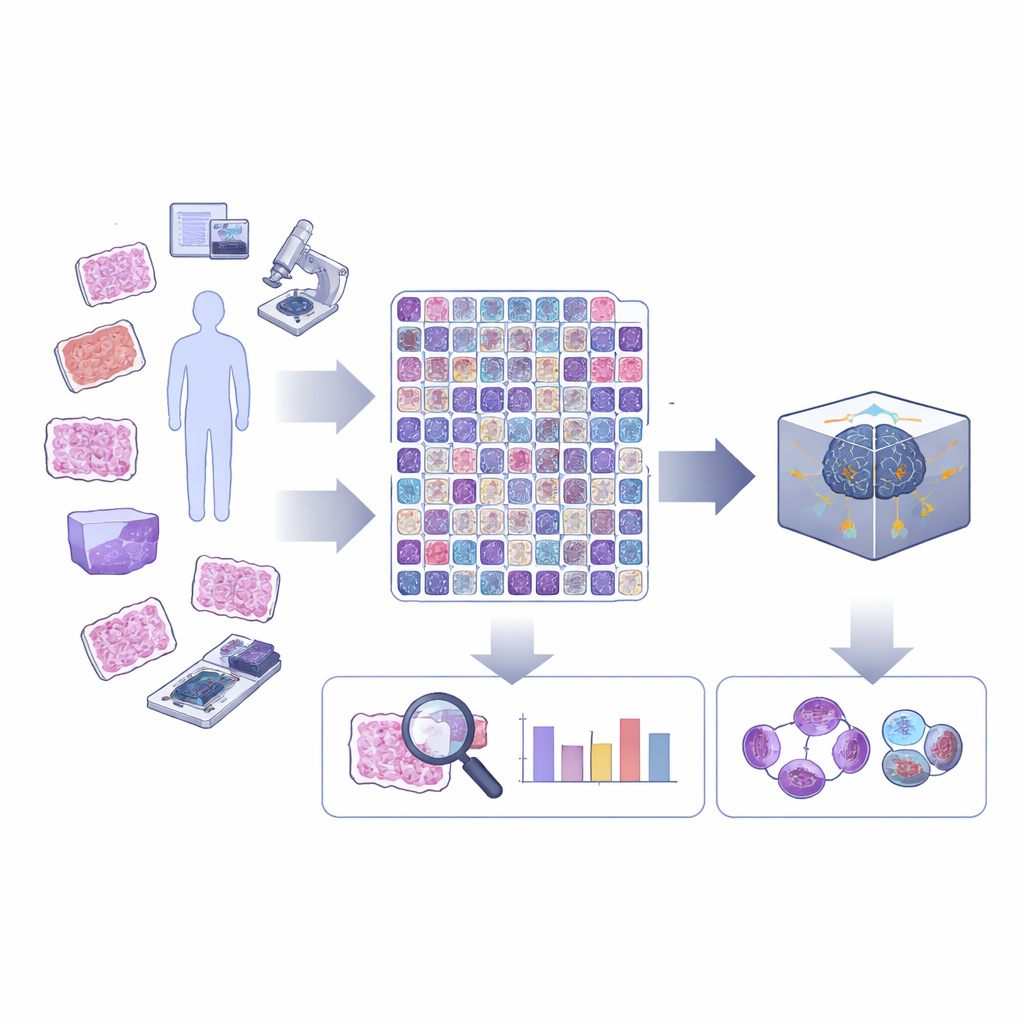
מבט קרוב יותר על חלוקת תאים ברקמת סרטן
חלוקת תאים, או מיטוזה, מתרחשת בסדרה של שלבים שבהם החומר הגנטי מוכפל ומופרד. באבחון השגרתי של סרטן, כלים ממוחשבים רבים מסמנים פשוט "דמויות מיטוטיות" כקטגוריה אחת, בלי להתייחס לאיזה שלב הן שייכות או האם הן נראות חריגות. עם זאת, חלוקות חריגות או "א-טיפיות", והיחס בין שלבים מוקדמים למאוחרים, עשויים לשאת מידע חשוב לגבי מידת הסיכון של הגידול. המחברים טוענים שבינה מלאכותית תגשים את הפוטנציאל שלה בפתולוגיה רק אם תוכל לזהות הבחנות דקות אלה שהמומחים האנושיים כבר מחפשים תחת המיקרוסקופ.
בניית ספרייה עשירה יותר של תמונות
כדי לעבור מעבר לגישה פשוטה של כן‑או‑לא לגבי תאים מתחלקים, הצוות הרחיב מאגר בוחן קיים גדול הידוע כ‑MIDOG++, שכבר כלל כמה סוגי גידולים, מינים ומכשירי סריקה. מציינים מומחים עברו מחדש על יותר מעשרת אלפים דמויות מיטוטיות ולכל אחת ייחסו אחד מחמשת השלבים העיקריים של חלוקה תקינה, בנוסף לקטגוריה נפרדת למיטוזות א‑טיפיות. הם גם שרטטו קווי מתאר מדויקים סביב כל תא, לא רק תיבות גסות. עבודה זהירה זו הופכת את המאגר למשאב שיכול לתמוך גם באימון בינה מלאכותית מדויק יותר וגם במחקרים עתידיים על צורת התא ומבנהו במהלך החלוקה.
הוספת מאגר חדש לסרטן ריאה
בהכרה בכך שמערכות בינה מלאכותית לרוב נתקעות כשהן מועברות מבית חולים או סוג איבר אחד לאחר, החוקרים גם יצרו מאגר חדש מתוך אדנוקרצינומה של הריאה, צורה שכיחה ומסוכנת של סרטן הריאה. במקום להתמקד רק באזורי "החמים" שבהם יש הכי הרבה פעילות, הם בחרו את כל אזור הגידול בכל פרט, חילקו אותו לפעמים לתמונות חפיפת‑גודל נוחות לעיבוד, ותייגו בעמל רב תאים מתחלקים, חלוקות א‑טיפיות ותאים שנראים דומים אבל אינם מתחלקים. מאגר LUNG‑MITO הזה מספק מבחן אמיתי ומאתגר לשאלה האם אלגוריתם שאומן במקום אחר יכול עדיין להציג ביצועים טובים מול רקמות ותנאי סריקה חדשים.
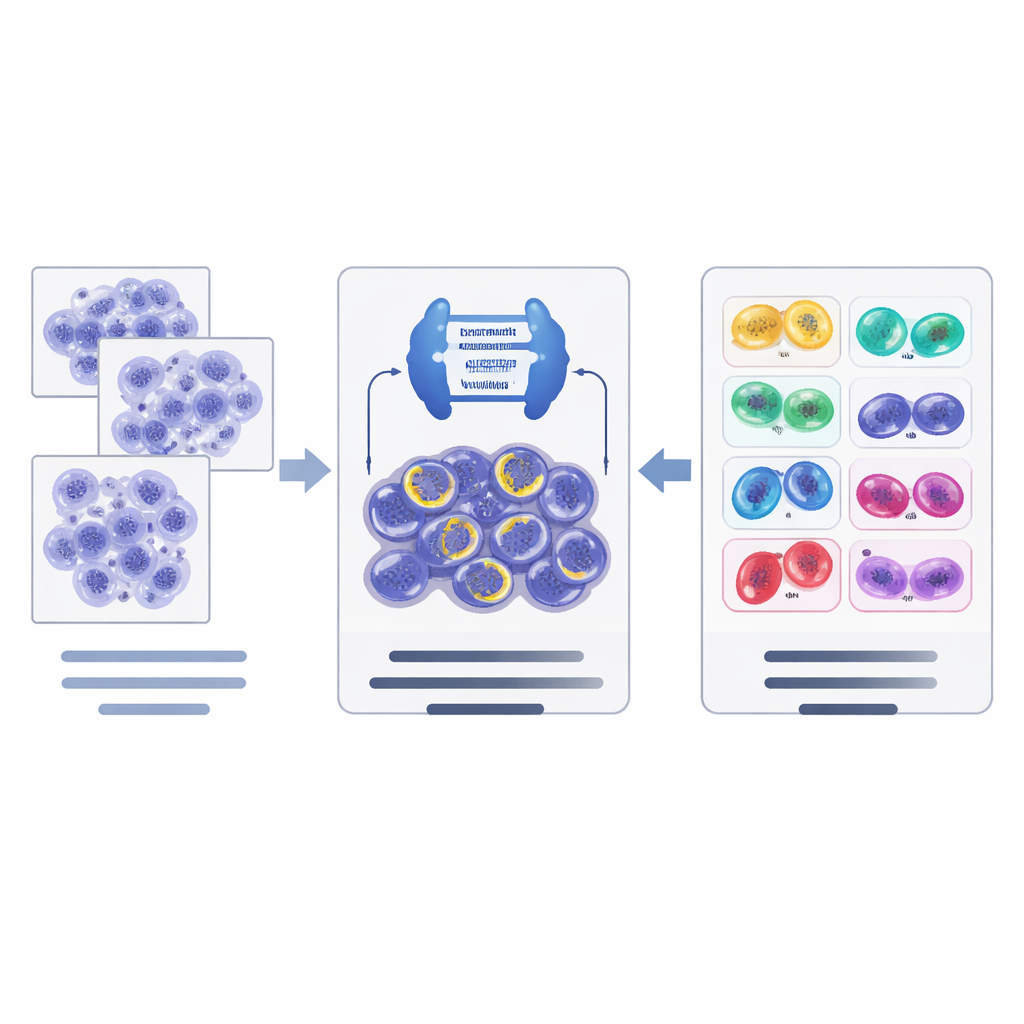
איך צינור הבינה המלאכותית החדש עובד
על בסיס משאבי הנתונים האלה, המחברים תכננו צינור עבודה דו‑שלבי של בינה מלאכותית. ראשית, רשת חיתוך תמונות חזקה, מבוססת ארכיטקטורה מודרנית בשם ConvNeXt בשילוב עם Mask R‑CNN, סורקת אריחי רקמה ומציעה מועמדים לתאים מתחלקים, תוך שרטוט כל אחד ומתן הערכה התחלתית של שלבו. שנית, רשת סיווג נפרדת (EfficientNet) בוחנת מקרוב את המועמדים ומדייקת את ההחלטה באופן היררכי: קודם היא שופטת האם המועמד אכן מתחלק או שמדובר בזיוף, ולאחר מכן, עבור מיטוזות מאושרות, בוחרת את השלב הסביר ביותר. המערכת משתמשת בטריקות הגברה מותאמות לתמונות פתולוגיות כדי להתמודד עם הבדלים בצביעה ובמכשירי הסריקה בין מעבדות.
בדיקת ביצועים בהגדרות שונות
כדי לשפוט באופן הוגן עד כמה הגישה שלהם עובדת, החוקרים עקבו אחרי כללי ההערכה שנעשה בהם שימוש באתגרים קודמים לזיהוי מיטוזה. הם מדדו באיזו תדירות התאים שחזו האלגוריתמים התאימו לתאים שסומנו על‑ידי מומחים בתוך מרחק קטן, תוך התחשבות גם בגילויי החמצה וגם באזעקות שווא. האימון בוצע על חלק מנתוני MIDOG++ המורחב, בעוד שקבצי השקופיות החדשים של LUNG‑MITO הוחזקו כמבחן נפרד כדי לבדוק עד כמה השיטה חסינה לשינויים בסוג הגידול ובחומרת הצילום. החיזוק של המבנה והתוספת של שלב הדייקון שיפרו באופן ברור את הביצועים לעומת מערכת מסורתית יותר, הן בזיהוי הכולל והן בדיוק עבור כל תת‑סוג של חלוקת תאים.
מה המשמעות של זה לטיפול ולמחקר בסרטן
עבור לא‑מומחים, המסר העיקרי הוא שהמחקר מספק גם מאגר ציבורי מפורט יותר וגם מודל בינה מלאכותית משופר לזיהוי איך ומתי תאי סרטן מתחלקים. על‑ידי לימוד האלגוריתמים להבחין בין שלבים שונים של מיטוזה ולסמן חלוקות א‑טיפיות, וכן באמצעות הצגת העובדה שאפשר לעשות זאת בצורה אמינה יותר על פני גידולים וסורקים מגוונים, העבודה מסמנת את היסודות לכלים עתידיים שיתמכו בפתולוגים בדירוג גידולים ובמחקר הביולוגיה שלהם. בטווח הארוך, כלים כאלה עשויים לסייע לעשות אבחנות סרטן עקביות יותר בין בתי חולים ולפתוח כיווני מחקר חדשים המקשרים בין מראה התאים המתחלקים להתנהגותם המולקולרית ותוצאות המטופל.
ציטוט: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
מילות מפתח: פתולוגיה דיגיטלית, חלוקת תאים, זיהוי מיטוזה, דימות סרטן, בינה מלאכותית רפואית