Clear Sky Science · pt
Um conjunto de dados mitótico rotulado por subfases para análise de divisão celular com IA
Por que contar células em divisão é importante
Quando médicos examinam câncer ao microscópio, uma das pistas mais importantes é quantas células estão em processo de divisão. Tumores que se dividem rapidamente costumam se comportar de forma mais agressiva e podem exigir tratamentos diferentes. Ainda assim, identificar essas minúsculas células em divisão é um trabalho lento e cansativo para patologistas, e até especialistas frequentemente discordam. Este estudo apresenta um novo conjunto de imagens ricamente anotado e um método de inteligência artificial (IA) aprimorado, projetado para ajudar computadores a localizar e compreender essas células em divisão de forma mais confiável em vários tipos de câncer e hospitais.
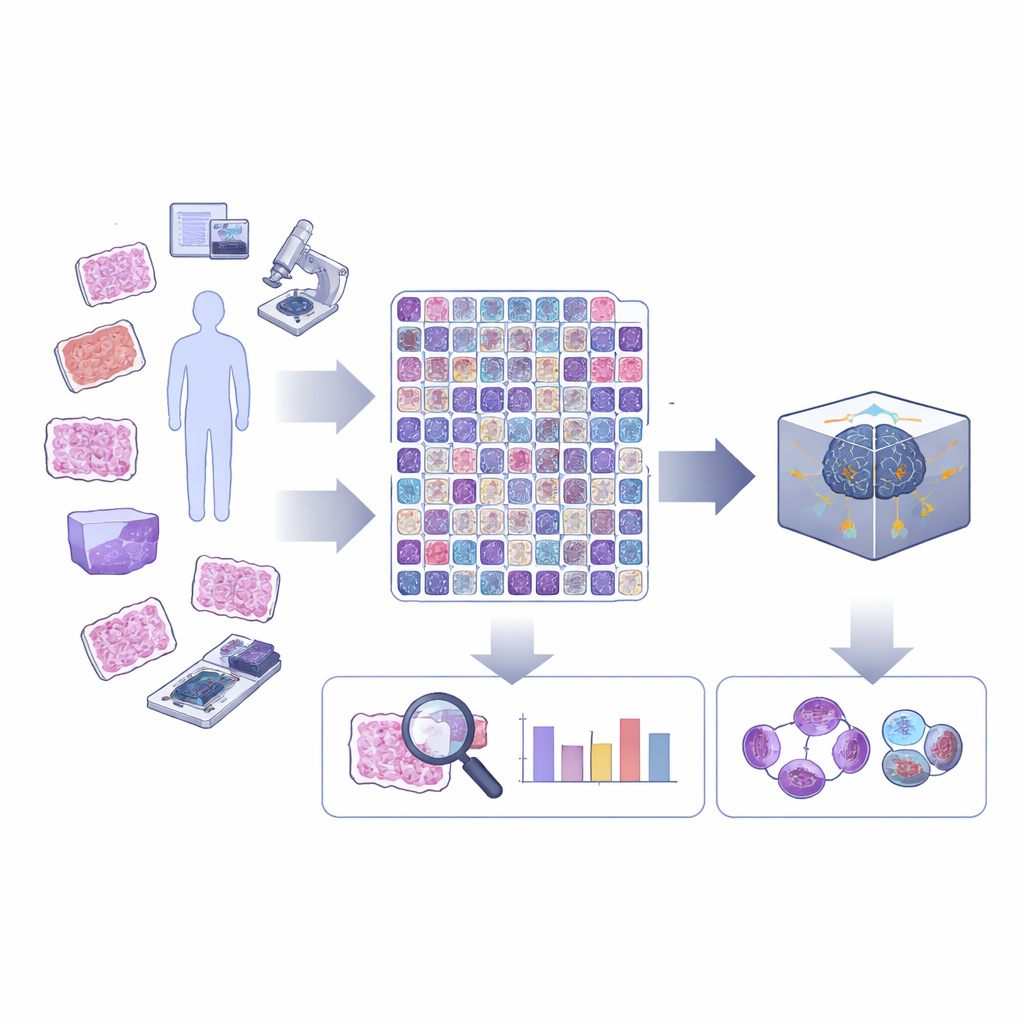
Um olhar mais atento sobre a divisão celular em tecido canceroso
A divisão celular, ou mitose, desenrola‑se em uma série de estágios enquanto o material genético da célula é duplicado e separado. No diagnóstico de rotina do câncer, a maioria das ferramentas computacionais simplesmente marca “figuras mitóticas” como uma única categoria, sem distinguir em que estágio estão ou se parecem anormais. Contudo, divisões incomuns ou “atípicas”, e o equilíbrio entre estágios iniciais e tardios, podem trazer informações importantes sobre o quão perigoso é um tumor. Os autores defendem que a IA só alcançará todo seu potencial na patologia se puder discernir essas distinções mais sutis que especialistas humanos já procuram ao microscópio.
Construindo uma biblioteca de imagens mais rica
Para ir além de uma visão binária das células em divisão, a equipe estendeu um grande benchmark existente conhecido como MIDOG++, que já cobria múltiplos tipos tumorais, espécies e dispositivos de digitalização. Anotadores especialistas revisitaram mais de dez mil figuras mitóticas e atribuíram cada uma a uma das cinco principais fases da divisão celular normal, além de uma classe separada para mitoses atípicas. Eles também desenharam contornos precisos ao redor de cada célula, não apenas caixas genéricas. Esse trabalho cuidadoso transforma o conjunto de dados em um recurso que pode suportar tanto um treinamento de IA mais exato quanto estudos futuros sobre forma e estrutura celulares durante a divisão.
Adicionando um novo conjunto de dados de câncer de pulmão
Reconhecendo que sistemas de IA frequentemente falham quando transferidos de um hospital ou órgão para outro, os pesquisadores também criaram um novo conjunto de dados a partir de adenocarcinoma pulmonar, uma forma comum e letal de câncer de pulmão. Em vez de focar apenas nas regiões mais ativas, eles selecionaram toda a área tumoral em cada lâmina, dividiram‑na em blocos de imagem manejáveis e rotularam meticulosamente células em divisão, mitoses atípicas e células semelhantes mas não em divisão. Este conjunto LUNG‑MITO fornece um teste difícil e realista para verificar se um algoritmo treinado em outros contextos ainda tem bom desempenho ao lidar com novo tecido e condições de digitalização.
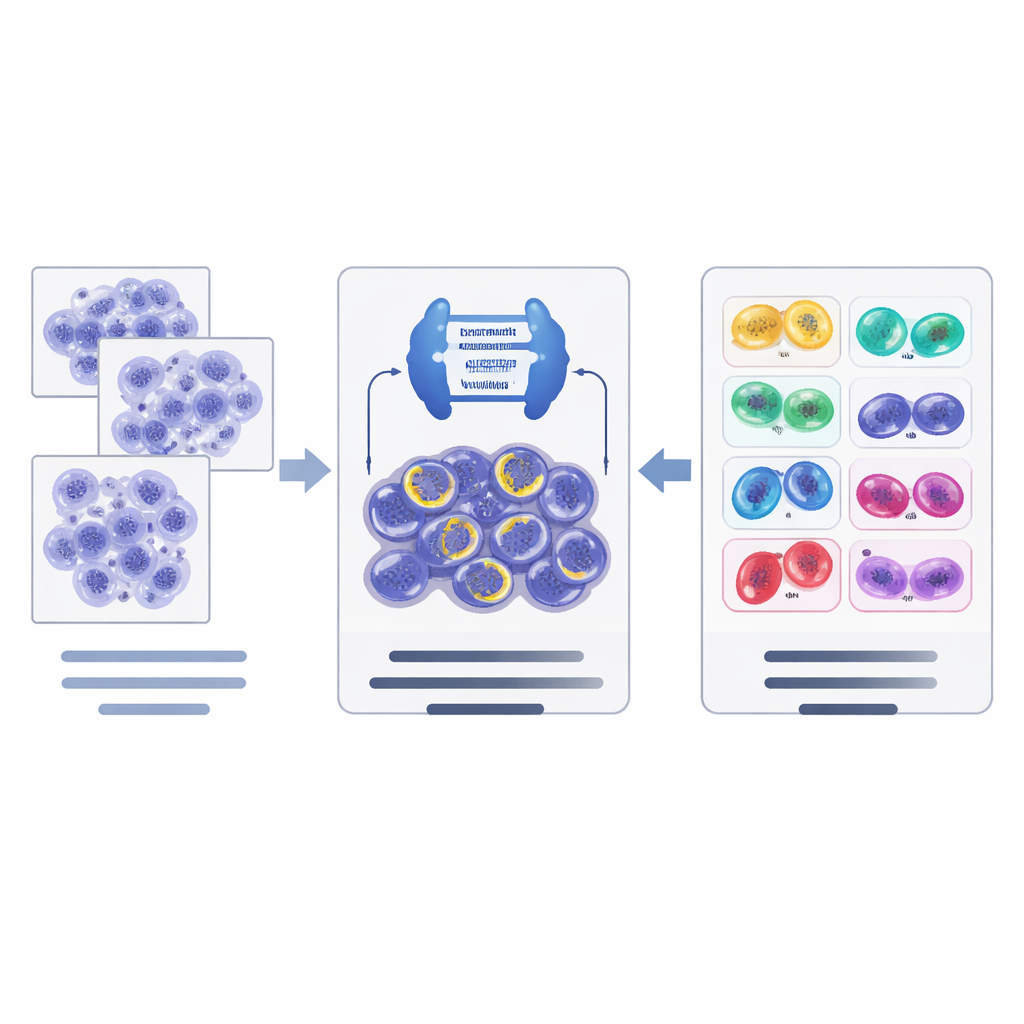
Como o novo pipeline de IA funciona
Com base nesses recursos de dados, os autores desenharam um pipeline de IA em duas etapas. Primeiro, uma poderosa rede de segmentação de imagem, baseada em uma arquitetura moderna chamada ConvNeXt combinada com Mask R‑CNN, escaneia os blocos de tecido e propõe candidatos a células em divisão, contornando cada uma e fornecendo uma estimativa inicial de seu estágio. Em segundo lugar, uma rede de classificação separada (EfficientNet) analisa mais a fundo esses candidatos e refina a decisão de forma hierárquica: primeiro julga se um candidato está realmente em divisão ou é um impostor e, em seguida, para mitoses confirmadas, escolhe o estágio mais provável. O sistema usa truques de aumento de dados adaptados a imagens de patologia para ajudá‑lo a lidar com diferenças de coloração e digitalizadores entre laboratórios.
Testando desempenho em diferentes cenários
Para avaliar com justiça quão bem a abordagem funciona, os pesquisadores seguiram as mesmas regras de avaliação usadas em desafios anteriores de detecção de mitose. Mediram com que frequência as células previstas pelo algoritmo correspondiam às células desenhadas por especialistas dentro de uma pequena distância, levando em conta tanto detecções perdidas quanto alarmes falsos. O treinamento foi feito em uma parte dos dados estendidos do MIDOG++, enquanto as novas lâminas LUNG‑MITO foram reservadas como um teste separado para sondar quão robusto o método é a mudanças no tipo tumoral e no hardware de imagem. A espinha dorsal aprimorada e a etapa de refinamento mostraram claramente melhora de desempenho sobre um sistema mais tradicional, elevando tanto a detecção geral quanto a precisão para cada subtipo de divisão celular.
O que isso significa para o cuidado e a pesquisa do câncer
Para não‑especialistas, a mensagem principal é que o estudo oferece tanto um conjunto de dados público detalhado quanto um modelo de IA mais robusto para reconhecer como e quando células cancerosas se dividem. Ao ensinar algoritmos a distinguir diferentes estágios da mitose e a sinalizar divisões atípicas, e ao mostrar que isso pode ser feito de forma mais confiável em diversos tumores e digitalizadores, o trabalho estabelece a base para futuras ferramentas que apoiem patologistas na graduação de tumores e no estudo de sua biologia. A longo prazo, tais ferramentas poderiam ajudar a tornar diagnósticos de câncer mais consistentes entre hospitais e abrir novas direções de pesquisa que relacionem a aparência de células em divisão a seu comportamento molecular e aos desfechos dos pacientes.
Citação: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Palavras-chave: patologia digital, divisão celular, detecção de mitose, imagens de câncer, IA médica