Clear Sky Science · it
Un dataset mitotico etichettato per sottofasi per l’analisi della divisione cellulare con l’IA
Perché conta contare le cellule in divisione
Quando i medici osservano il cancro al microscopio, uno degli indizi più importanti è quante cellule sono nel mezzo della divisione. I tumori che si dividono rapidamente tendono a comportarsi in modo più aggressivo e possono richiedere trattamenti diversi. Tuttavia individuare queste minuscole cellule in divisione è un lavoro lento e faticoso per i patologi e anche gli esperti spesso non sono d’accordo. Questo studio presenta un nuovo dataset di immagini riccamente annotato e un metodo di intelligenza artificiale (IA) migliorato pensato per aiutare i computer a trovare e comprendere queste cellule in divisione in modo più affidabile su molti tipi di tumore e strutture ospedaliere.
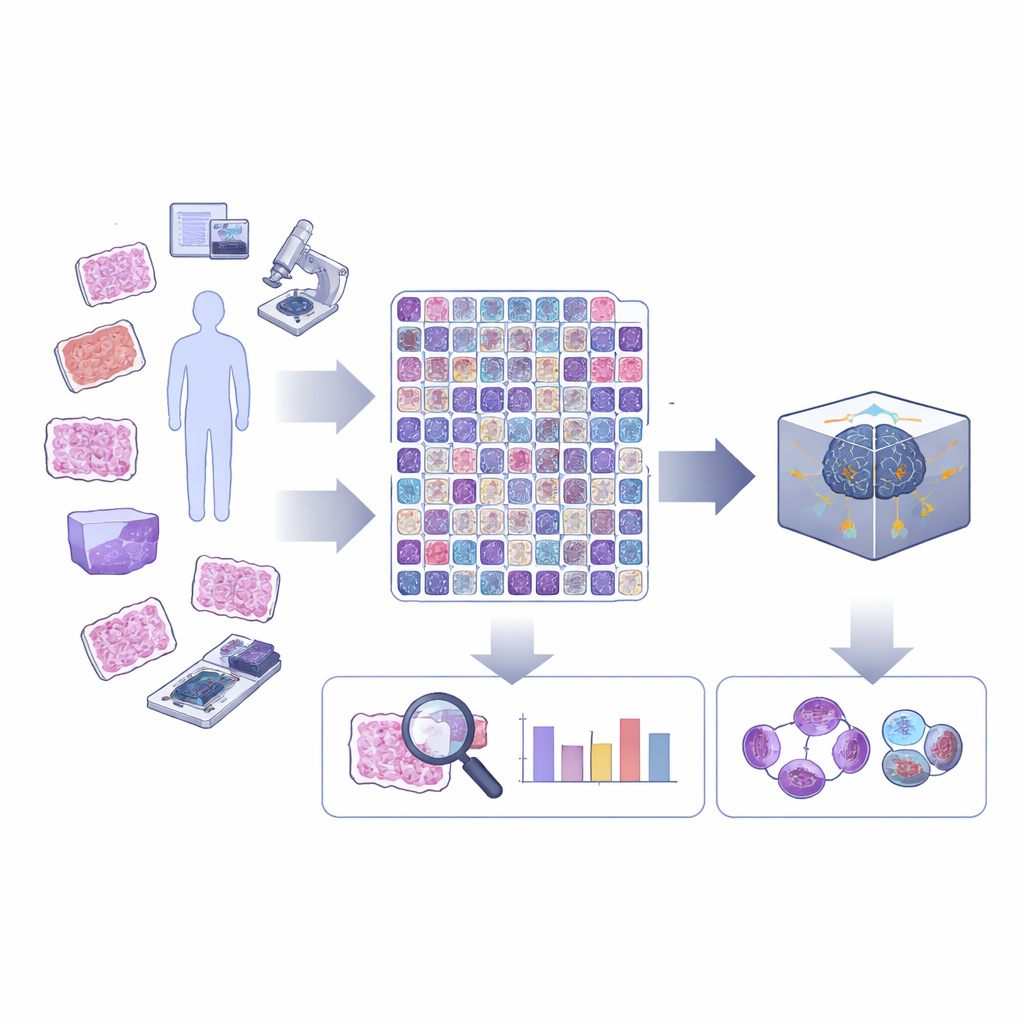
Uno sguardo più ravvicinato alla divisione cellulare nel tessuto tumorale
La divisione cellulare, o mitosi, si svolge in una serie di fasi mentre il materiale genetico della cellula viene duplicato e separato. Nella diagnostica oncologica di routine, la maggior parte degli strumenti informatici limita le “figure mitotiche” a un’unica categoria, ignorando in quale fase si trovino o se appaiano anomale. Tuttavia le divisioni insolite o “atipiche”, e l’equilibrio tra fasi precoci e tardive, possono fornire informazioni importanti sul grado di pericolosità di un tumore. Gli autori sostengono che l’IA raggiungerà il suo pieno potenziale in patologia solo se riuscirà a riconoscere queste distinzioni più fini che gli specialisti umani già cercano al microscopio.
Costruire una libreria di immagini più ricca
Per andare oltre una semplice visione binaria delle cellule in divisione, il team ha esteso un grande benchmark esistente noto come MIDOG++, che già includeva diversi tipi di tumore, specie e scanner. Annotatori esperti hanno rivisto più di diecimila figure mitotiche assegnando a ciascuna una delle cinque fasi principali della mitosi normale, oltre a una classe separata per le mitosi atipiche. Hanno inoltre tracciato contorni precisi attorno a ogni cellula, non solo rettangoli approssimativi. Questo lavoro accurato trasforma il dataset in una risorsa che può supportare sia l’addestramento di IA più preciso sia studi futuri sulla forma e sulla struttura delle cellule durante la divisione.
Aggiunta di un nuovo dataset sul cancro polmonare
Consapevoli che i sistemi di IA spesso peggiorano quando vengono trasferiti da un ospedale o da un organo a un altro, i ricercatori hanno creato anche un nuovo dataset da adenocarcinomi polmonari, una forma comune e letale di cancro al polmone. Invece di concentrarsi solo sulle regioni “più attive”, hanno selezionato l’intera area tumorale su ciascuna lastra, l’hanno suddivisa in tasselli d’immagine gestibili e hanno accuratamente etichettato le cellule in divisione, le divisioni atipiche e le strutture simili ma non in divisione. Questo dataset LUNG‑MITO offre un test difficile e realistico per verificare se un algoritmo addestrato altrove può comunque performare bene di fronte a nuovi tessuti e condizioni di scansione.
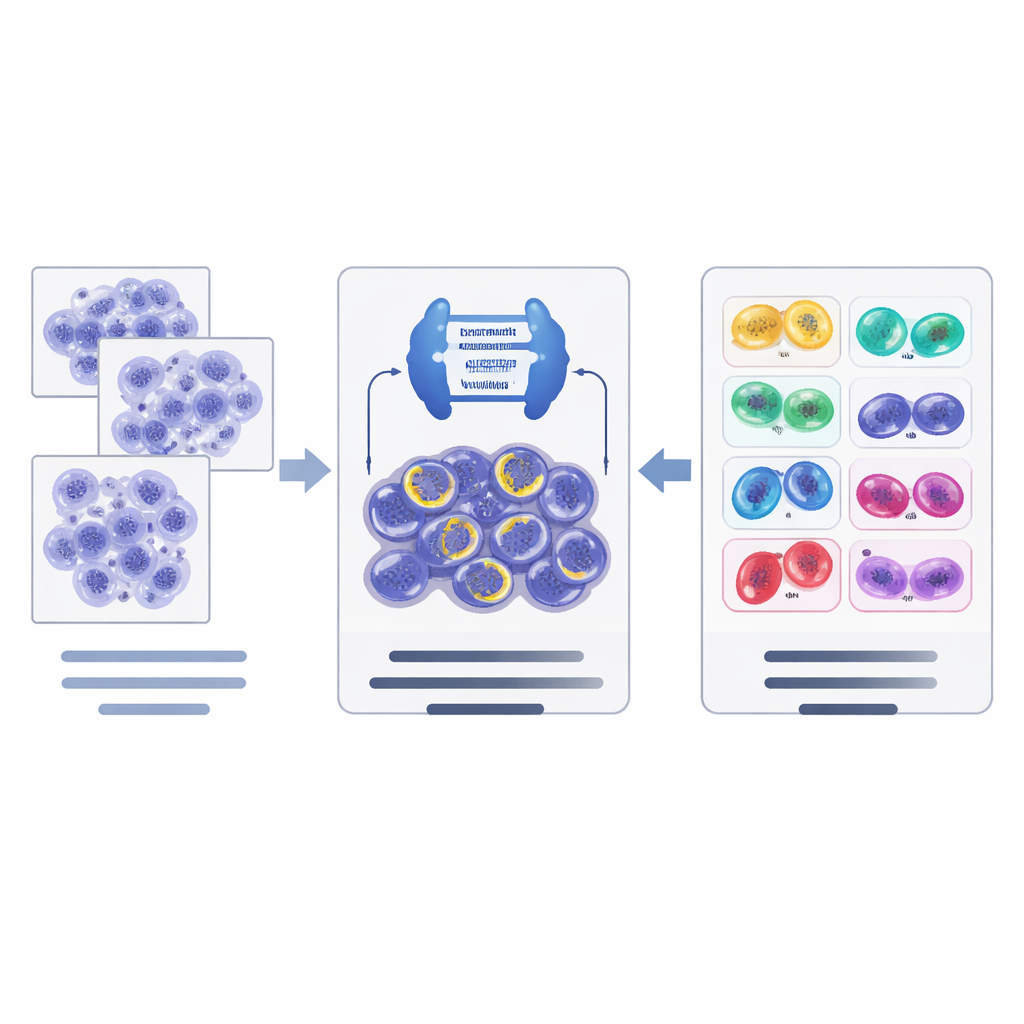
Come funziona la nuova pipeline IA
Sopra a queste risorse di dati, gli autori hanno progettato una pipeline IA in due fasi. Per prima cosa, una potente rete di segmentazione d’immagine, basata su un’architettura moderna chiamata ConvNeXt combinata con Mask R‑CNN, analizza i tasselli di tessuto e propone candidati a cellule in divisione, tracciandone il contorno e fornendo una stima iniziale della fase. In secondo luogo, una rete di classificazione separata (EfficientNet) esamina più in dettaglio questi candidati e affina la decisione in modo gerarchico: valuta prima se un candidato è davvero in divisione o è un falso positivo, e poi, per le mitosi confermate, sceglie la fase più probabile. Il sistema impiega tecniche di data augmentation adattate alle immagini di patologia per aiutarlo a gestire le differenze di colorazione e di scanner tra i laboratori.
Valutare le prestazioni in contesti diversi
Per giudicare in modo equo l’efficacia del loro approccio, i ricercatori hanno seguito le stesse regole di valutazione usate nelle precedenti challenge di rilevamento della mitosi. Hanno misurato quanto spesso le cellule predette dall’algoritmo corrispondessero a quelle disegnate dagli esperti entro una piccola distanza, tenendo conto sia delle omissioni sia dei falsi positivi. L’addestramento è stato svolto su una porzione dei dati estesi di MIDOG++, mentre le nuove lastre LUNG‑MITO sono state tenute separate come test per sondare la robustezza del metodo rispetto ai cambiamenti di tipo tumorale e di hardware di imaging. Il backbone migliorato e il passaggio di raffinamento hanno chiaramente aumentato le prestazioni rispetto a un sistema più tradizionale, migliorando sia il rilevamento complessivo sia la precisione per ogni sottotipo di divisione cellulare.
Cosa significa per la cura e la ricerca del cancro
Per i non specialisti, il messaggio principale è che lo studio fornisce sia un dataset pubblico dettagliato sia un modello IA più solido per riconoscere come e quando le cellule tumorali si dividono. Insegnando agli algoritmi a distinguere le diverse fasi della mitosi e a segnalare le divisioni atipiche, e dimostrando che ciò può essere fatto in modo più affidabile attraverso tumori e scanner diversi, il lavoro pone le basi per futuri strumenti di supporto ai patologi nella stadiazione dei tumori e nello studio della loro biologia. A lungo termine, tali strumenti potrebbero contribuire a rendere le diagnosi oncologiche più coerenti tra diversi ospedali e aprire nuove direzioni di ricerca che colleghino l’aspetto delle cellule in divisione al loro comportamento molecolare e agli esiti dei pazienti.
Citazione: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Parole chiave: patologia digitale, divisione cellulare, rilevamento della mitosi, imaging oncologico, IA medica