Clear Sky Science · pl
Zbiór danych mitotycznych oznaczony podfazami do analizy podziału komórek wspomaganej przez AI
Dlaczego liczenie dzielących się komórek ma znaczenie
Kiedy lekarze oglądają nowotwór pod mikroskopem, jednym z najważniejszych wskazówek jest liczba komórek będących w trakcie podziału. Guzy szybko dzielące się często zachowują się bardziej agresywnie i mogą wymagać innego leczenia. Jednak wykrywanie tych maleńkich komórek w mitozie jest pracochłonne i męczące dla patologów, a nawet eksperci często się nie zgadzają. W tym badaniu przedstawiono nowy, bogato adnotowany zestaw obrazów oraz udoskonaloną metodę sztucznej inteligencji (AI), zaprojektowaną, by pomagać komputerom w bardziej niezawodnym wykrywaniu i rozumieniu tych komórek w różnych typach nowotworów i w wielu szpitalach.
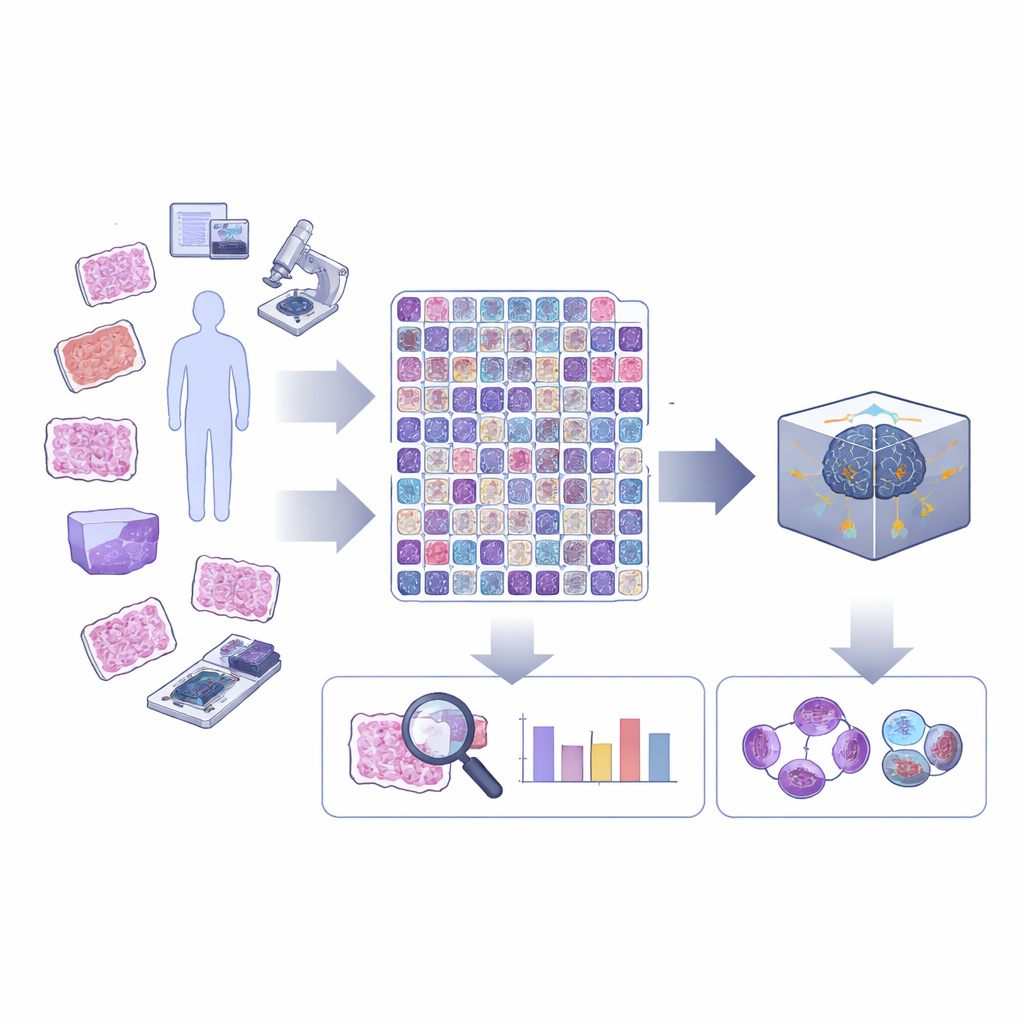
Bliższe spojrzenie na podział komórek w tkance nowotworowej
Podział komórkowy, czyli mitoza, przebiega w szeregu etapów, podczas których materiał genetyczny komórki jest kopiowany i rozdzielany. W rutynowej diagnostyce onkologicznej większość narzędzi komputerowych zaznacza „figury mitotyczne” jako jedną kategorię, pomijając, na jakim etapie się znajdują lub czy wyglądają nieprawidłowo. Tymczasem nietypowe podziały oraz proporcje między wczesnymi a późnymi fazami mogą dostarczać ważnych informacji o złośliwości guza. Autorzy argumentują, że AI osiągnie pełny potencjał w patologii tylko wtedy, gdy będzie widziała te drobne rozróżnienia, na które specjaliści zwracają uwagę pod mikroskopem.
Budowanie bogatszej biblioteki obrazów
Aby wyjść poza prostą ocenę tak/nie dla komórek w mitozie, zespół rozszerzył istniejący duży benchmark znany jako MIDOG++, który już obejmował wiele typów nowotworów, gatunków i urządzeń skanujących. Eksperci-annotatorzy ponownie przejrzeli ponad dziesięć tysięcy figur mitotycznych i przypisali każdą z nich do jednej z pięciu głównych faz prawidłowego podziału komórkowego oraz do oddzielnej klasy dla mitoz atypowych. Dodatkowo narysowali precyzyjne obrysy każdej komórki, a nie tylko przybliżone ramki. Ta staranna praca przekształca zbiór danych w zasób, który może wspierać zarówno dokładniejsze trenowanie AI, jak i przyszłe badania nad kształtem i strukturą komórek podczas podziału.
Dodanie nowego zbioru danych dotyczącego raka płuca
Kiedy AI przenosi się z jednego szpitala lub typu narządu do innego, często napotyka trudności — mając to na uwadze, badacze stworzyli także nowy zbiór danych z przyswającego się raka płuc (adenocarcinoma płuca), powszechnego i groźnego typu raka. Zamiast koncentrować się wyłącznie na „najgorętszych” obszarach z największą aktywnością, wybrali cały obszar guza na każdej szkiełce, podzielili go na łatwe do przetwarzania fragmenty obrazu i żmudnie oznaczyli komórki w mitozie, podziały atypowe oraz struktury podobne wyglądem, lecz niewykonujące podziału. Zbiór danych LUNG-MITO stanowi trudny, realistyczny test tego, czy algorytm trenowany gdzie indziej nadal radzi sobie dobrze w obliczu nowych tkanek i warunków skanowania.
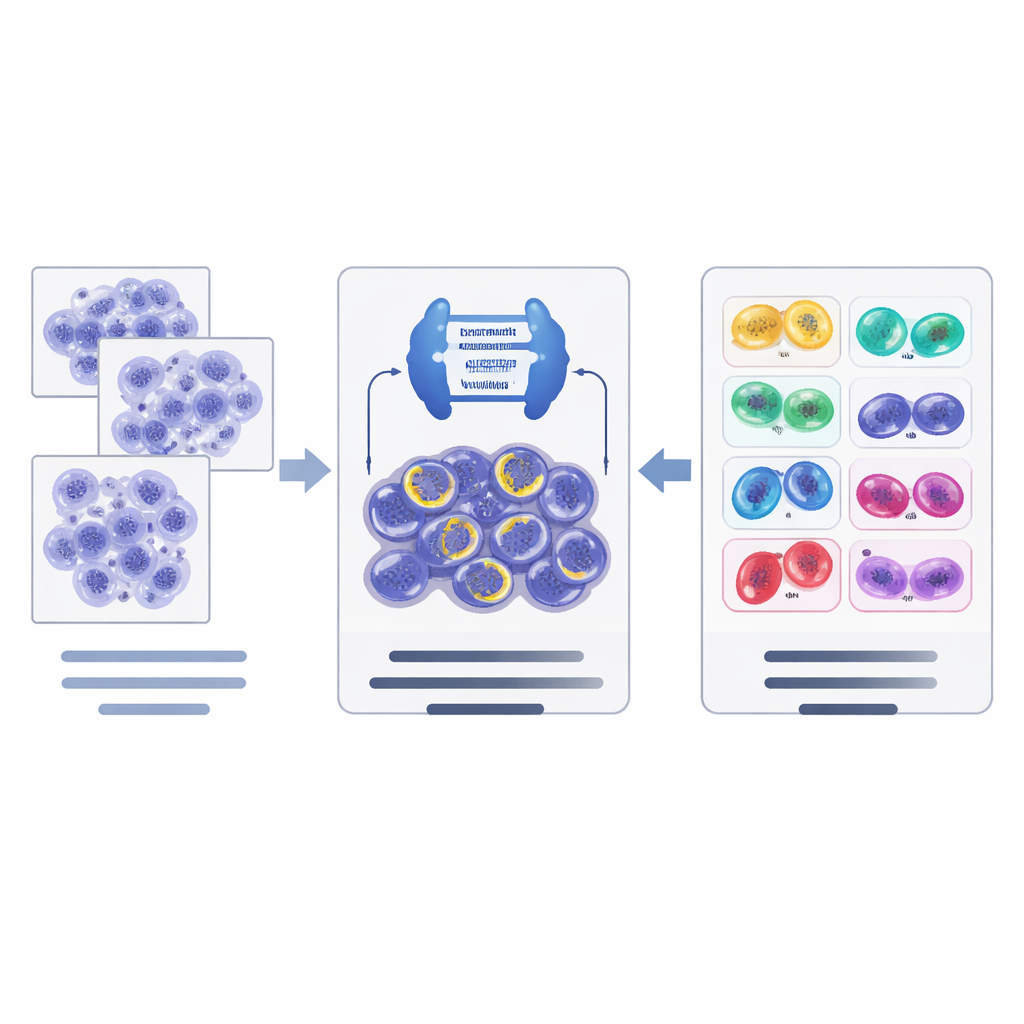
Jak działa nowy pipeline AI
W oparciu o te zasoby danych autorzy zaprojektowali dwuetapowy pipeline AI. Najpierw potężna sieć segmentacyjna obrazu, oparta na nowoczesnej architekturze ConvNeXt połączonej z Mask R‑CNN, skanuje fragmenty tkanki i proponuje kandydatów na komórki dzielące się, obrysowując każdą z nich i podając wstępne oszacowanie fazy. Następnie oddzielna sieć klasyfikacyjna (EfficientNet) przygląda się bliżej tym kandydatom i doprecyzowuje decyzję w sposób hierarchiczny: najpierw ocenia, czy kandydat rzeczywiście dzieli się, czy jest fałszywym tropem, a potem, dla potwierdzonych mitoz, wybiera najbardziej prawdopodobną fazę. System wykorzystuje techniki augmentacji danych dostosowane do obrazów patologicznych, by lepiej radzić sobie z różnicami w barwieniu i sprzęcie skanującym między laboratoriami.
Testowanie wydajności w różnych warunkach
Aby sprawiedliwie ocenić skuteczność podejścia, badacze zastosowali te same zasady ewaluacji, które obowiązywały w poprzednich wyzwaniach wykrywania mitoz. Mierzyli, jak często przewidywane przez algorytm komórki pokrywają się z komórkami narysowanymi przez ekspertów w niewielkiej odległości, uwzględniając zarówno pominięcia, jak i fałszywe alarmy. Trening przeprowadzono na części rozszerzonych danych MIDOG++, podczas gdy nowe preparaty LUNG‑MITO odłożono jako oddzielny test, by zbadać odporność metody na zmiany typu guza i sprzętu obrazującego. Ulepszony fundament sieciowy i etap doprecyzowania wyraźnie poprawiły wyniki w porównaniu z bardziej tradycyjnym systemem, zwiększając zarówno wykrywalność, jak i dokładność dla poszczególnych podtypów podziału komórkowego.
Co to oznacza dla opieki onkologicznej i badań
Dla osób spoza specjalności główny przekaz jest taki, że badanie dostarcza zarówno szczegółowy publiczny zbiór danych, jak i silniejszy model AI do rozpoznawania, jak i kiedy komórki nowotworowe się dzielą. Uczenie algorytmów rozróżniania faz mitozy i oznaczania podziałów atypowych oraz udowodnienie, że można to robić bardziej niezawodnie w różnych rodzajach nowotworów i na różnych skanerach, tworzy podstawy dla przyszłych narzędzi wspierających patologów przy ocenie stopnia zaawansowania guza i badaniu jego biologii. W dłuższej perspektywie takie narzędzia mogą przyczynić się do większej spójności diagnoz onkologicznych między szpitalami oraz otworzyć nowe kierunki badań łączących wygląd dzielących się komórek z ich zachowaniami molekularnymi i wynikami leczenia pacjentów.
Cytowanie: Ivan, Z.Z., Hirling, D., Grexa, I. et al. A Subphase-Labeled Mitotic Dataset for AI-powered Cell Division Analysis. Sci Data 13, 680 (2026). https://doi.org/10.1038/s41597-026-07007-7
Słowa kluczowe: patologia cyfrowa, podział komórkowy, wykrywanie mitozy, obrazowanie nowotworowe, medyczne AI