Clear Sky Science · zh
在Aβ暴露下的人类神经元分化:单细胞转录组与表观基因组数据集
这项脑细胞研究为何重要
阿尔茨海默病会逐步剥夺人们的记忆和思维能力,但我们仍未完全弄清楚在疾病进展过程中新生脑细胞会发生什么。该研究在体外构建了一个详尽的“图谱”,展示人类神经细胞在暴露于淀粉样‑β(amyloid‑beta)时的发育过程——这种小蛋白片段会在阿尔茨海默病患者的大脑中累积。通过对数千个细胞逐一追踪,并同时考察哪些基因被激活以及DNA如何被包装,研究者提供了一个丰富的参考地图,供其他科学家探究与痴呆相关的早期改变。
在培养皿中构建脑细胞
为了在可控条件下研究早期神经元发育,团队使用了人源诱导多能干细胞(iPSC),这些细胞可以被引导分化为神经祖细胞——许多脑细胞类型的起始材料。将这些祖细胞培养在培养皿中,随后转入一种促进其在20天内进一步成熟为神经元的特定培养基。有些培养皿按正常条件处理,另一些从一开始就暴露于淀粉样‑β1–42——该肽段是阿尔茨海默病中斑块的组成成分。两组细胞在四个关键时间点采集——改变前(第0天)以及分化过程中(第7、13和20天)——以捕捉其发育路径逐步展开的过程。 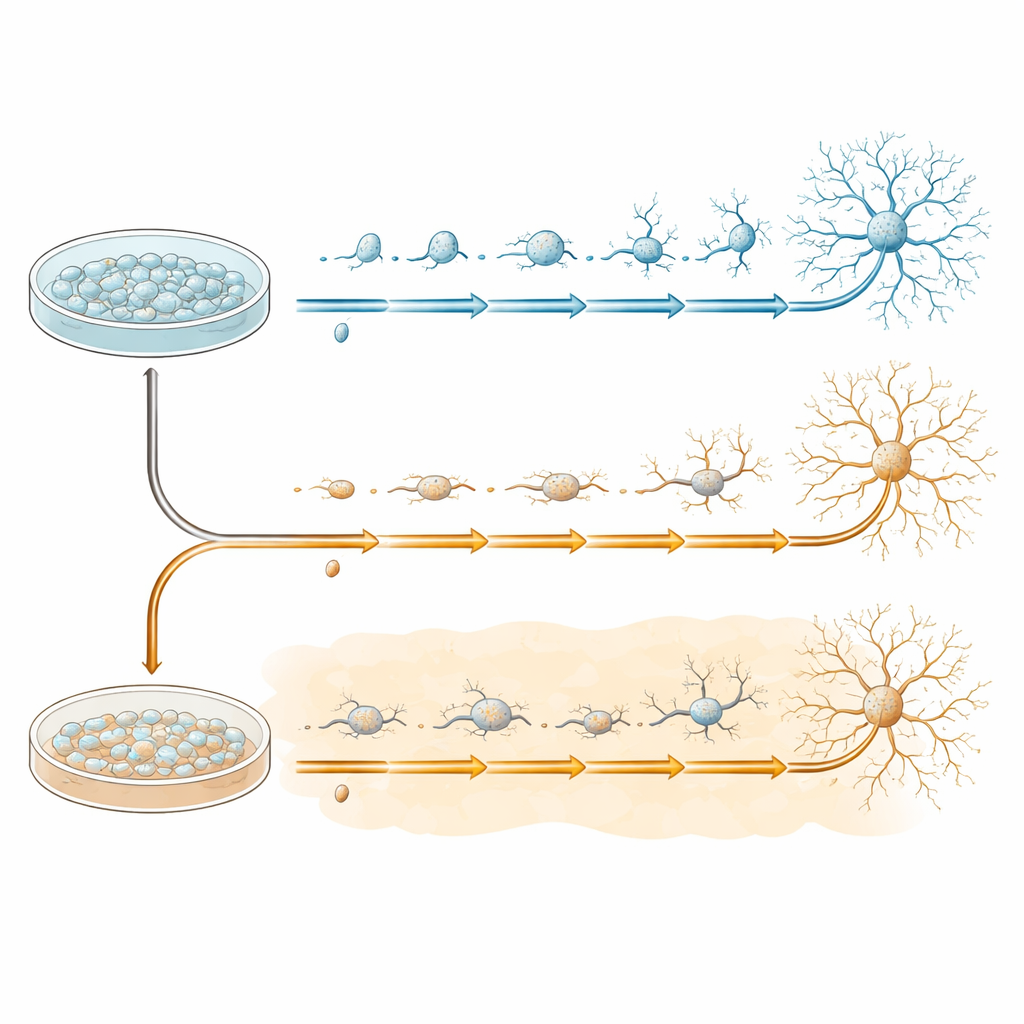
倾听基因并打开基因组
这项工作的突出之处在于每个细胞都以两种互补的方式被检测。首先,研究者使用单细胞RNA测序来测量超过42,000个细胞中哪些基因被激活。其次,他们在超过30,000个细胞中应用了单细胞ATAC测序,以查看DNA哪些区域是可及的——这是这些区域可作为控制基因开关的一个标志。通过复杂的计算方法,研究者将细胞分成不同簇并沿发育“轨迹”排列,从祖细胞到更成熟的神经元和类星形胶质细胞,并将基因表达模式与染色质(包装基因的DNA‑蛋白质物质)变化联系起来。
从干细胞到神经元的追踪旅程
在发育中的神经细胞中,团队识别出一系列五个宽泛阶段,标记为A到E,反映出从分裂的类干细胞向具有复杂树突的成熟神经元的逐步转变。早期和后期神经状态的经典标志基因沿这一路径有序变化,独立的“伪时间”分析也证实了相同的顺序。在后期阶段,他们进一步细分并发现更成熟细胞中存在子路径,显示某些细胞在明确其身份时会沿略微不同的路线发展。贯穿这些步骤,科学家编目了共同变化的基因、在淀粉样‑β存在时反应不同的基因,以及似乎仅在淀粉样‑β暴露下发生改变的基因集合。
淀粉样‑β改变了什么——又保留了什么
尽管有无淀粉样‑β时发育路径的总体结构相似,团队在肽存在的特定阶段仍检测到某些基因活性明显上调或下调的独特变化。许多这些基因参与神经细胞间的通讯、轴突和树突生长以及对健康脑回路至关重要的其他功能。研究者还将基因活性与染色质数据结合,构建了将关键调控蛋白(称为转录因子)与其靶基因集合连接起来的网络。他们发现了数千个此类“调控子(regulon)”,并展示了其中一些在正常与淀粉样‑β条件下的行为不同,尽管大规模的DNA可及性变化仍然较为有限。 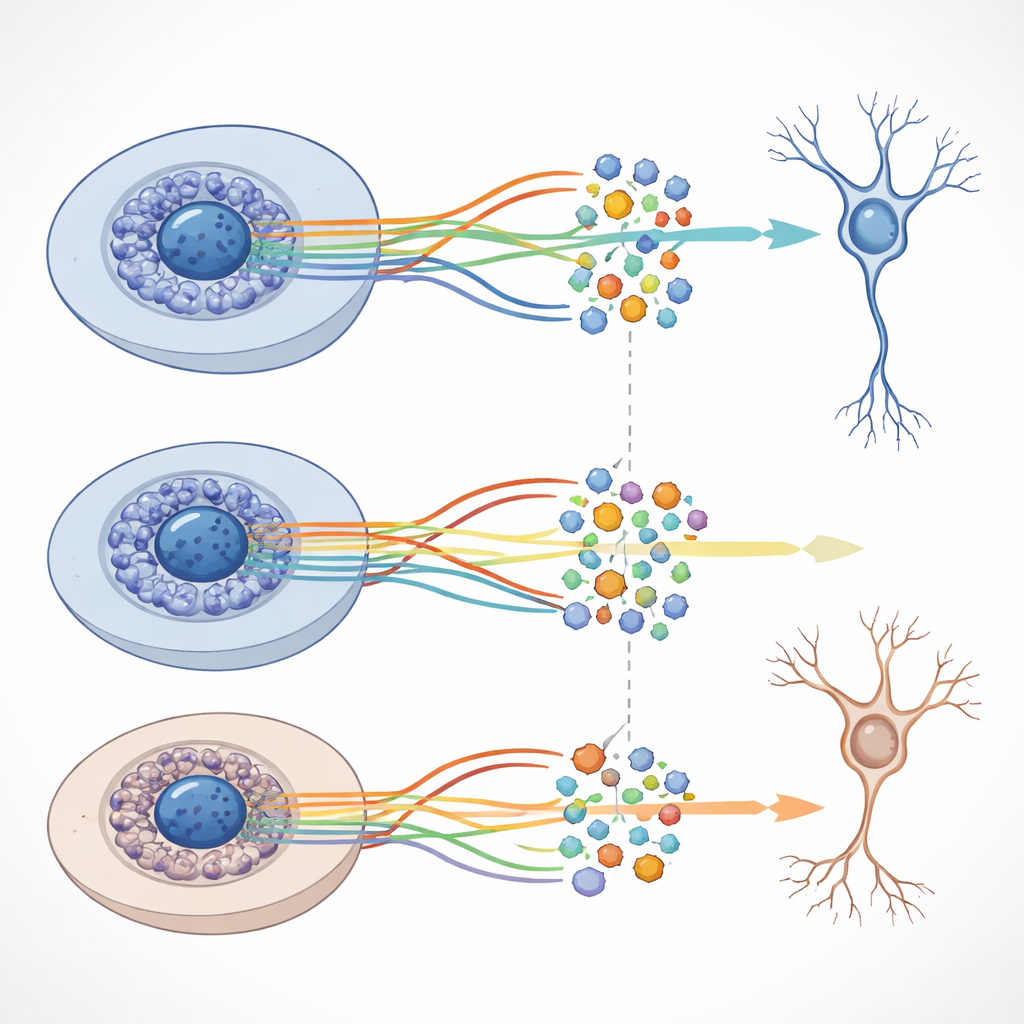
将实验室发现与人类阿尔茨海默病大脑连接起来
为评估其细胞培养系统与真实疾病的相关性,作者将他们的基因列表与一份来自阿尔茨海默病患者与对照者的大脑组织现有数据集进行了比较。若干在正常与淀粉样‑β处理细胞间差异显著的基因,在对照与阿尔茨海默病大脑间也呈现差异。当他们将不同发育阶段特异的基因组合作为“签名”来处理时,这些签名在患者海马样本的变化中富集,尤其是与神经元通讯和结构相关的基因。这表明该体外模型捕捉到了老化大脑中易损记忆中枢发生的有意义的生物学片段。
该资源为未来提供了什么
这项工作的主要产出不是单一的轰动性结论,而是一个公开、可重复使用的数据集。所有原始和处理后的信息,以及分析代码和一个交互式网络浏览器,都可供其他科学家自由访问。研究者可以使用这张地图来基准测试新的计算工具、探索不同实验室方案如何影响神经元发育,或检验关于阿尔茨海默病相关过程如何扰乱脑细胞出生与成熟的新假设。简单来说,该研究提供了一个详细的“连线图”,描述年轻人类脑细胞在有无关键阿尔茨海默病相关胁迫下如何生长——这将帮助该领域分解问题发生的时间与地点。
引用: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
关键词: 阿尔茨海默病, 神经发生, 单细胞测序, 淀粉样β肽, 神经元分化