Clear Sky Science · fr
Différenciation neurale humaine sous exposition à l’Aβ : un jeu de données transcriptomique et épigénomique monocellulaire
Pourquoi cette étude des cellules cérébrales est importante
La maladie d’Alzheimer dépouille lentement les personnes de leur mémoire et de leurs capacités de réflexion, mais nous ne comprenons pas encore complètement ce qui arrive aux nouveaux neurones au fur et à mesure de l’évolution de la maladie. Cette étude établit un « atlas » détaillé du développement des cellules nerveuses humaines en culture lorsqu’elles sont exposées à l’amyloïde‑bêta, un petit fragment protéique qui s’accumule dans les cerveaux des malades d’Alzheimer. En suivant des milliers de cellules individuellement et en regardant non seulement quels gènes sont actifs mais aussi la manière dont l’ADN est empaqueté, les chercheurs proposent une carte de référence riche que d’autres scientifiques peuvent utiliser pour explorer les changements précoces liés à la démence.
Construire des cellules cérébrales en éprouvette
Pour étudier de façon contrôlée le développement précoce des neurones, l’équipe a utilisé des cellules souches pluripotentes induites humaines, qui peuvent être orientées pour devenir des cellules progénitrices neurales — la matière de départ de nombreux types cellulaires du cerveau. Ces progéniteurs ont été cultivés en plaque puis placés dans un milieu spécial qui favorise leur transformation en neurones plus matures sur 20 jours. Certaines plaques ont suivi ce protocole dans des conditions normales, tandis que d’autres ont été exposées dès le départ à l’amyloïde‑bêta 1–42, le même peptide qui forme des plaques dans la maladie d’Alzheimer. Des cellules des deux groupes ont été prélevées à quatre moments clés — avant le changement (jour 0) et pendant la transformation (jours 7, 13 et 20) — afin de capturer pas à pas le déroulement de leurs trajectoires développementales. 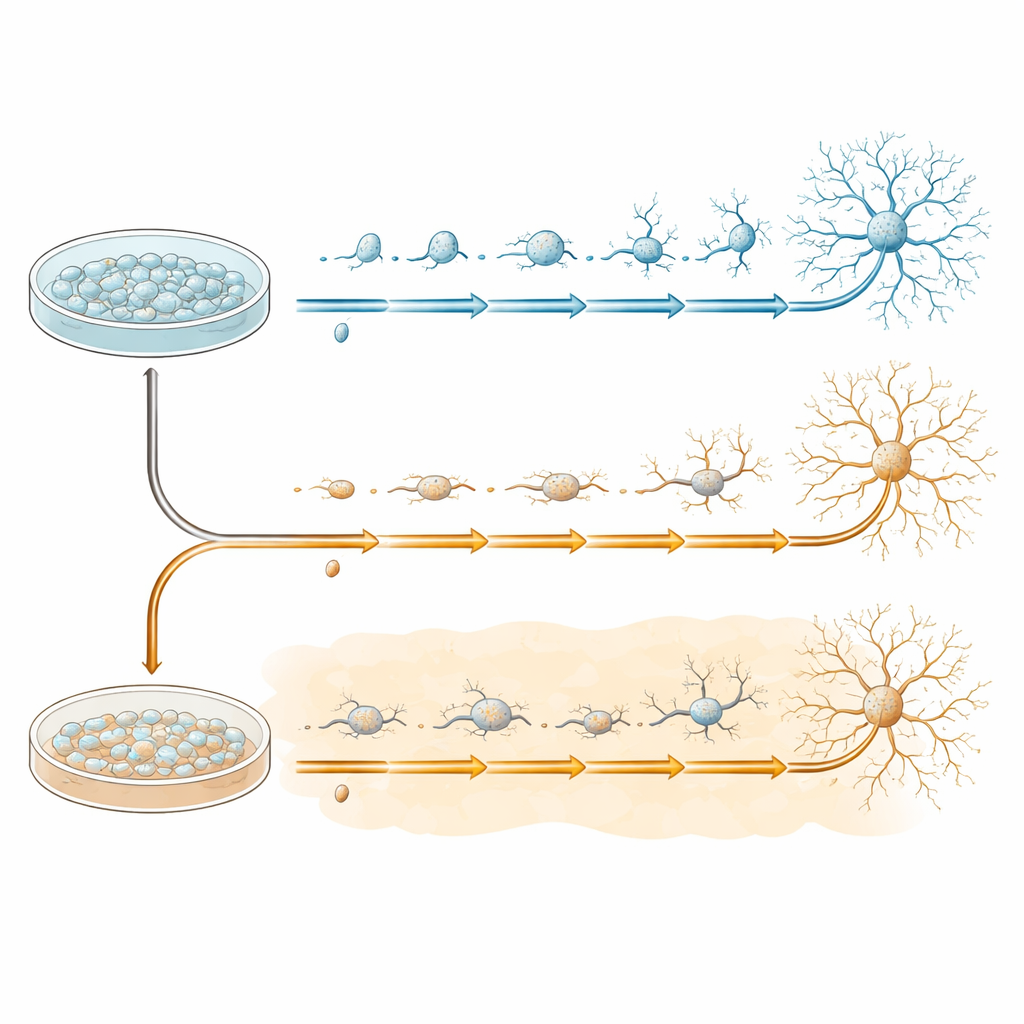
Écouter les gènes et ouvrir le génome
Ce qui distingue ce travail, c’est que chaque cellule a été examinée de deux manières complémentaires. D’une part, les chercheurs ont utilisé le séquençage ARN monocellulaire pour mesurer quels gènes étaient activés dans plus de 42 000 cellules. D’autre part, ils ont employé le séquençage ATAC monocellulaire sur plus de 30 000 cellules pour voir quelles régions de l’ADN étaient physiquement accessibles, indice que ces régions peuvent servir d’interrupteurs régulateurs des gènes. Des méthodes informatiques sophistiquées ont groupé les cellules en amas, les ont ordonnées le long de « trajectoires » développementales allant des progéniteurs vers des neurones plus matures et des cellules de type astrocytaire, et ont relié les motifs d’activité génique aux changements de la chromatine, le complexe ADN‑protéine qui emballe nos gènes.
Tracer le parcours des cellules souches aux neurones
Au sein des cellules neuronales en développement, l’équipe a identifié une série de cinq grands stades, étiquetés de A à E, qui reflètent un passage progressif de cellules à division de type souche vers des neurones en maturation aux ramifications complexes. Les gènes marqueurs classiques des états neuronaux précoces et tardifs ont évolué de manière ordonnée le long de ce parcours, et une analyse indépendante de « pseudotemps » a confirmé la même séquence. À des stades plus avancés, ils ont affiné l’analyse et trouvé des sous‑itinéraires parmi les cellules plus matures, montrant que certaines cellules empruntent des voies légèrement différentes en affinant leur identité. À travers ces étapes, les scientifiques ont catalogué des gènes qui changent de concert, des gènes qui répondent différemment en présence d’amyloïde‑bêta, et des ensembles de gènes qui semblent modifiés uniquement sous exposition à l’amyloïde‑bêta.
Ce que modifie l’amyloïde‑bêta — et ce qu’elle laisse intact
Bien que la structure globale des trajectoires développementales soit similaire avec et sans amyloïde‑bêta, l’équipe a détecté des décalages distincts dans l’activité de certains gènes à des stades particuliers lorsque le peptide était présent. Nombre de ces gènes sont impliqués dans la communication neuronale, la croissance des axones et des dendrites, et d’autres fonctions essentielles aux circuits cérébraux sains. Les chercheurs ont également combiné les données d’activité génique et de chromatine pour construire des réseaux reliant des protéines de contrôle clés, appelées facteurs de transcription, à des ensembles de gènes cibles. Ils ont découvert des milliers de ces « régulons » et montré que certains se comportent différemment entre les conditions normales et sous amyloïde‑bêta, même si les changements à grande échelle d’accessibilité de l’ADN restent modestes. 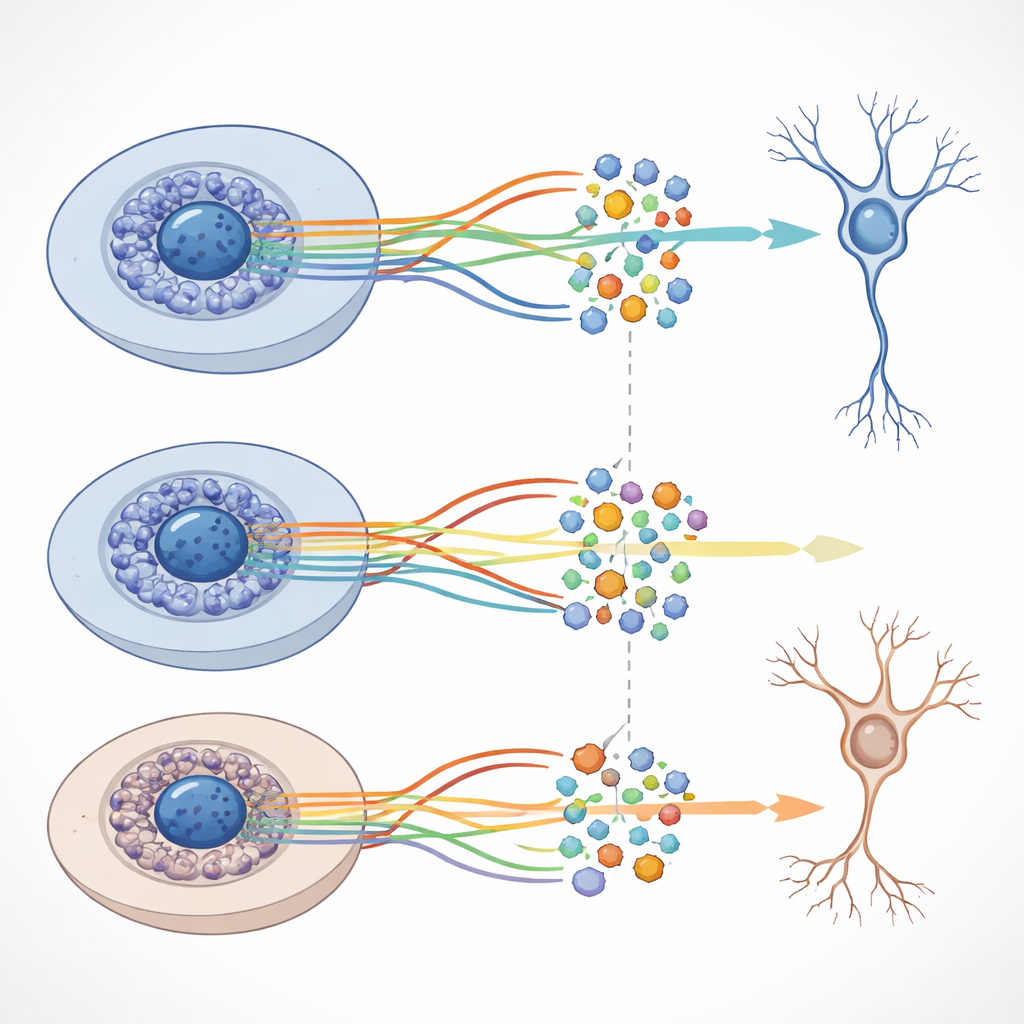
Relier les résultats de laboratoire aux cerveaux humains atteints d’Alzheimer
Pour évaluer la pertinence de leur système en culture par rapport à la maladie réelle, les auteurs ont comparé leurs listes de gènes à un jeu de données existant de tissus cérébraux de personnes avec et sans Alzheimer. Plusieurs des mêmes gènes qui différaient entre cellules traitées ou non par l’amyloïde‑bêta différaient aussi entre cerveaux témoins et cerveaux Alzheimer. Lorsqu’ils ont traité des groupes de gènes spécifiques à des stades de développement comme des « signatures », ces signatures étaient enrichies parmi les changements observés dans des échantillons d’hippocampe de patients, en particulier pour des gènes liés à la communication et à la structure neuronales. Cela suggère que le modèle in vitro capture des éléments significatifs de la biologie se produisant dans les centres de la mémoire vulnérables du cerveau vieillissant.
Ce que cette ressource offre pour l’avenir
Le principal produit de ce travail n’est pas un unique résultat médiatique mais un jeu de données public et réutilisable. Toutes les informations brutes et traitées, ainsi que le code d’analyse et un navigateur web interactif, sont librement disponibles pour d’autres chercheurs. Ces derniers peuvent utiliser cette carte pour évaluer de nouveaux outils informatiques, explorer comment différents protocoles de laboratoire influent sur le développement neuronal, ou tester de nouvelles hypothèses sur la manière dont les processus liés à Alzheimer perturbent la naissance et la maturation des cellules cérébrales. En termes simples, l’étude fournit un « schéma de câblage » détaillé de la croissance des jeunes cellules cérébrales humaines — avec et sans un stresseur clé associé à Alzheimer — qui aidera le domaine à disséquer quand et où les choses tournent mal.
Citation: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Mots-clés: maladie d’Alzheimer, neurogénèse, séquençage monocellulaire, amyloïde bêta, différenciation neuronale