Clear Sky Science · sv
Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset
Varför denna studie av hjärnceller är viktig
Alzheimers sjukdom berövar människor minne och tänkande gradvis, men vi förstår fortfarande inte fullt ut vad som händer med nyfödda hjärnceller när sjukdomen utvecklas. Denna studie skapar ett detaljerat ”atlas” över hur mänskliga nervceller utvecklas i laboratoriet när de utsätts för amyloid‑beta, ett litet proteinfragment som ansamlas i Alzheimers hjärnor. Genom att följa tusentals celler en och en, och inte bara undersöka vilka gener som är aktiva utan också hur DNA är paketerat, erbjuder forskarna en rik referenskarta som andra forskare kan använda för att undersöka tidiga förändringar kopplade till demens.
Att bygga hjärnceller i en skål
För att studera tidig nervcellsutveckling på ett kontrollerat sätt använde teamet mänskliga inducerade pluripotenta stamceller, som kan fås att bli neurala progenitorceller—startmaterialet för många hjärncellstyper. Dessa progenitorer odlades i skålar och byttes sedan över i ett särskilt medium som uppmuntrar dem att bli mer mogna neuroner över 20 dagar. Vissa skålar följde detta program under normala förhållanden, medan andra från början exponerades för amyloid‑beta 1–42, samma peptid som bildar plack vid Alzheimers sjukdom. Celler från båda grupper samlades vid fyra viktiga tidpunkter—före bytet (dag 0) och under omvandlingen (dagar 7, 13 och 20)—för att fånga det steg‑för‑steg som utvecklingsvägarna vecklas ut. 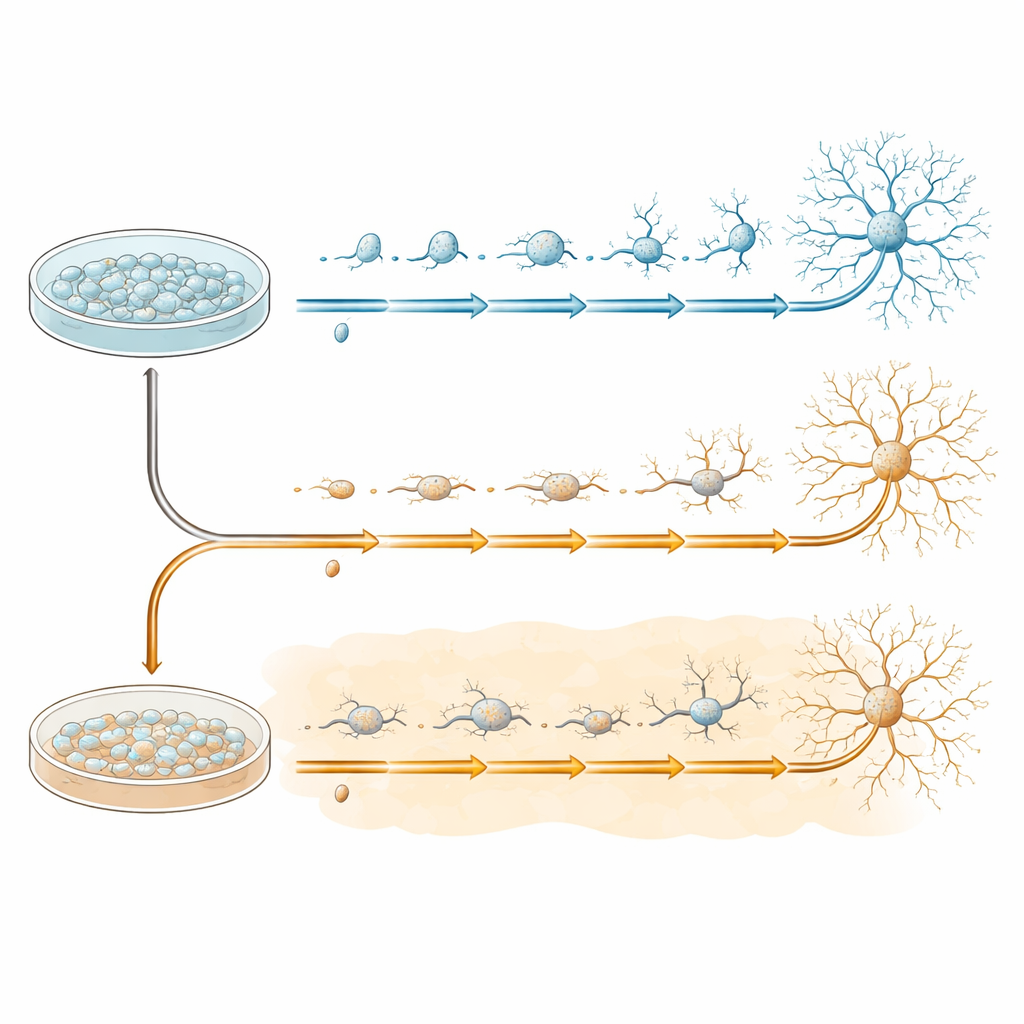
Att lyssna på generna och öppna genomet
Det som gör detta arbete särskilt är att varje cell undersöktes på två kompletterande sätt. Först använde forskarna enkelcells‑RNA‑sekvensering för att mäta vilka gener som var aktiva i mer än 42 000 celler. För det andra använde de enkelcells‑ATAC‑sekvensering i över 30 000 celler för att se vilka delar av DNA som var fysiskt tillgängliga, ett tecken på att dessa regioner kan fungera som strömbrytare för genreglering. Sofistikerade beräkningsmetoder grupperade cellerna i kluster, ordnade dem längs utvecklings"trajektorier" från progenitorer till mer mogna neuroner och astrocyt‑liknande celler, och kopplade mönster av genaktivitet till förändringar i kromatin, det DNA‑proteinmaterial som paketerar våra gener.
Att spåra resan från stamceller till neuroner
Inom de utvecklande neuronala cellerna identifierade teamet en serie av fem breda stadier, märkta A till E, som återspeglar en gradvis förskjutning från delande stamliknande celler mot mognande neuroner med komplexa förgreningar. Klassiska markörgener för tidiga och sena neuronala tillstånd ändrades i en ordnad följd längs denna väg, och en oberoende ”pseudotids”‑analys bekräftade samma sekvens. I senare stadier zoomade de in ytterligare och fann under‑vägar bland mer mogna celler, vilket visar att vissa celler följer något olika banor när de finslipar sin identitet. Över dessa steg katalogiserade forskarna gener som förändras tillsammans, gener som reagerar olika när amyloid‑beta är närvarande, och uppsättningar gener som verkar förändras endast under amyloid‑beta‑exponering.
Vad amyloid‑beta förändrar — och vad det lämnar intakt
Även om den övergripande strukturen av utvecklingsvägarna var likartad med och utan amyloid‑beta, upptäckte teamet tydliga förskjutningar i vilka gener som var mer eller mindre aktiva i särskilda stadier när peptiden var närvarande. Många av dessa gener är involverade i nervcellskommunikation, tillväxt av axoner och dendriter och andra funktioner som är avgörande för hälsosamma hjärnkretsar. Forskarna kombinerade också genaktivitets‑ och kromatindata för att bygga nätverk som länkar nyckelkontrollproteiner, så kallade transkriptionsfaktorer, till uppsättningar målgener. De upptäckte tusentals sådana ”reguloner” och visade att några av dem beter sig olika mellan de normala och amyloid‑beta‑förhållandena, även om storskaliga förändringar i DNA‑tillgänglighet förblev beskedliga. 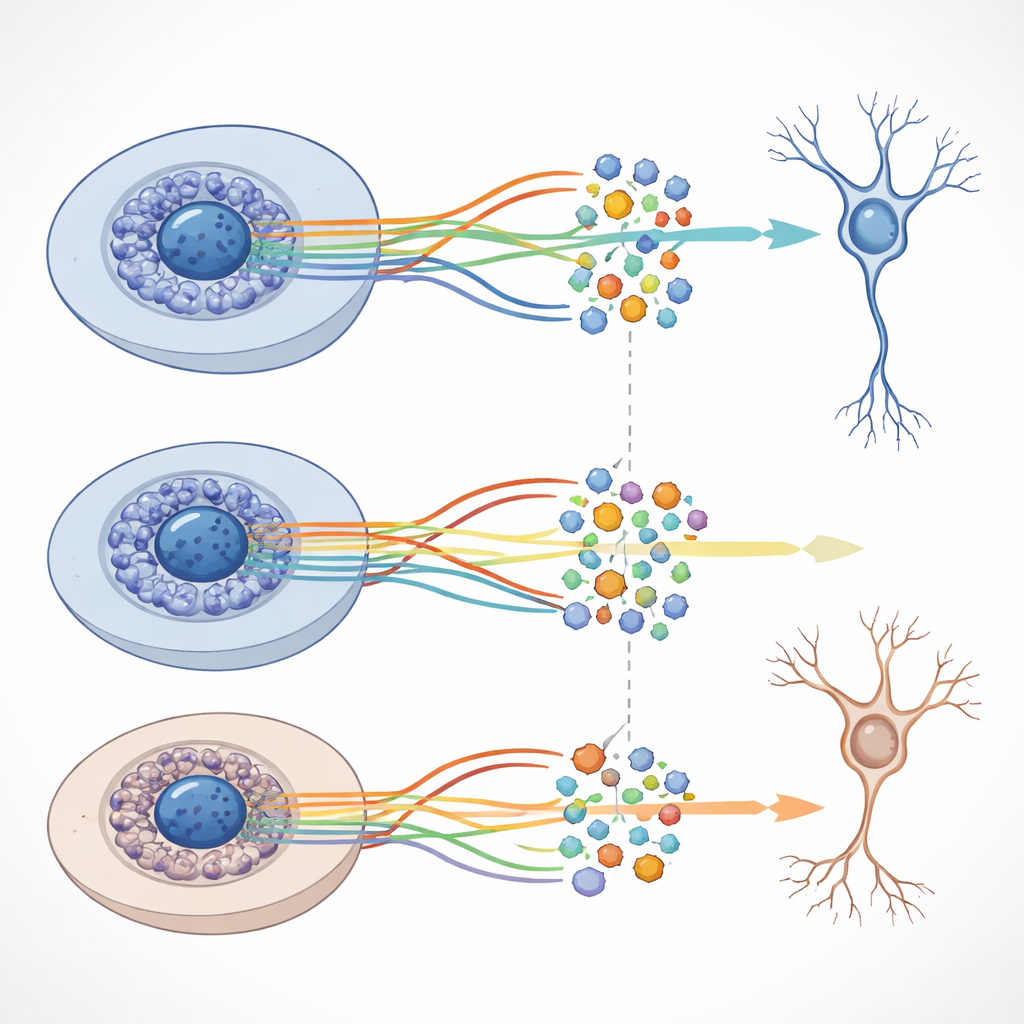
Att koppla laboratoriefynd till mänskliga Alzheimers‑hjärnor
För att se hur relevanta deras cellkultursystem är för verklig sjukdom jämförde författarna sina genträd med en befintlig dataset från hjärnvävnad hos personer med och utan Alzheimers. Flera av samma gener som skilde mellan normala och amyloid‑beta‑behandlade celler skilde sig också mellan kontroll- och Alzheimershjärnor. När de behandlade grupper av utvecklingsstadiespecifika gener som ”signaturer” var dessa signaturer berikade bland förändringarna som sågs i patienternas hippocampusprover, särskilt för gener kopplade till neuronal kommunikation och struktur. Detta tyder på att in vitro‑modellen fångar meningsfulla delar av biologin som sker i de sårbara minnescentra i den åldrande hjärnan.
Vad denna resurs erbjuder för framtiden
Huvudprodukten av detta arbete är inte ett enskilt rubrikresultat utan en offentlig, återanvändbar dataset. All rå och bearbetad information, tillsammans med analyskod och en interaktiv webbläsare, är fritt tillgänglig för andra forskare. Forskare kan använda denna karta för att benchmarka nya beräkningsverktyg, utforska hur olika laboratorieprotokoll påverkar neuronutveckling eller testa nya idéer om hur Alzheimers‑relaterade processer stör födseln och mognaden av hjärnceller. Enkelt uttryckt ger studien ett detaljerat ”kopplingsschema” för hur unga mänskliga hjärnceller växer—med och utan en viktig Alzheimers‑kopplad stressfaktor—som kommer att hjälpa fältet att dissekera när och var saker går fel.
Citering: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Nyckelord: Alzheimer’s disease, neurogenesis, single-cell sequencing, amyloid beta, neuronal differentiation