Clear Sky Science · de
Menschliche neuronale Differenzierung unter Aβ‑Exposition: ein Einzelzell‑transkriptomik‑ und Epigenomik‑Datensatz
Warum diese Studie zu Gehirnzellen wichtig ist
Die Alzheimer‑Krankheit raubt Menschen langsam Erinnerung und Denkvermögen, doch wir verstehen noch nicht vollständig, was mit neu entstehenden Gehirnzellen geschieht, während die Erkrankung voranschreitet. Diese Studie erstellt einen detaillierten „Atlas“ der Entwicklung menschlicher Nervenzellen im Labor unter Exposition gegenüber Amyloid‑beta, einem kleinen Proteinfragment, das sich in Alzheimer‑Gehirnen anreichert. Indem Tausende von Zellen einzeln verfolgt werden und nicht nur gemessen wird, welche Gene aktiv sind, sondern auch wie die DNA verpackt ist, liefern die Forschenden eine reichhaltige Referenzkarte, die andere Wissenschaftler verwenden können, um frühe Veränderungen im Zusammenhang mit Demenz zu untersuchen.
Gehirnzellen in der Petrischale züchten
Um frühe Entwicklungen von Nervenzellen kontrolliert zu untersuchen, verwendete das Team menschliche induzierte pluripotente Stammzellen, die dazu gebracht werden können, sich in neuronale Vorläuferzellen zu verwandeln – das Ausgangsmaterial für viele Hirnzelltypen. Diese Vorläufer wurden in Schalen kultiviert und dann in ein spezielles Medium überführt, das sie über 20 Tage hinweg zur Reifung zu Neuronen anregt. Einige Schalen folgten diesem Programm unter normalen Bedingungen, andere wurden von Anfang an Amyloid‑beta 1–42 ausgesetzt, demselben Peptid, das Plaques bei Alzheimer bildet. Zellen beider Gruppen wurden zu vier entscheidenden Zeitpunkten gesammelt – vor der Umstellung (Tag 0) und während der Umwandlung (Tage 7, 13 und 20) –, um die schrittweise Entfaltung ihrer Entwicklungswege einzufangen. 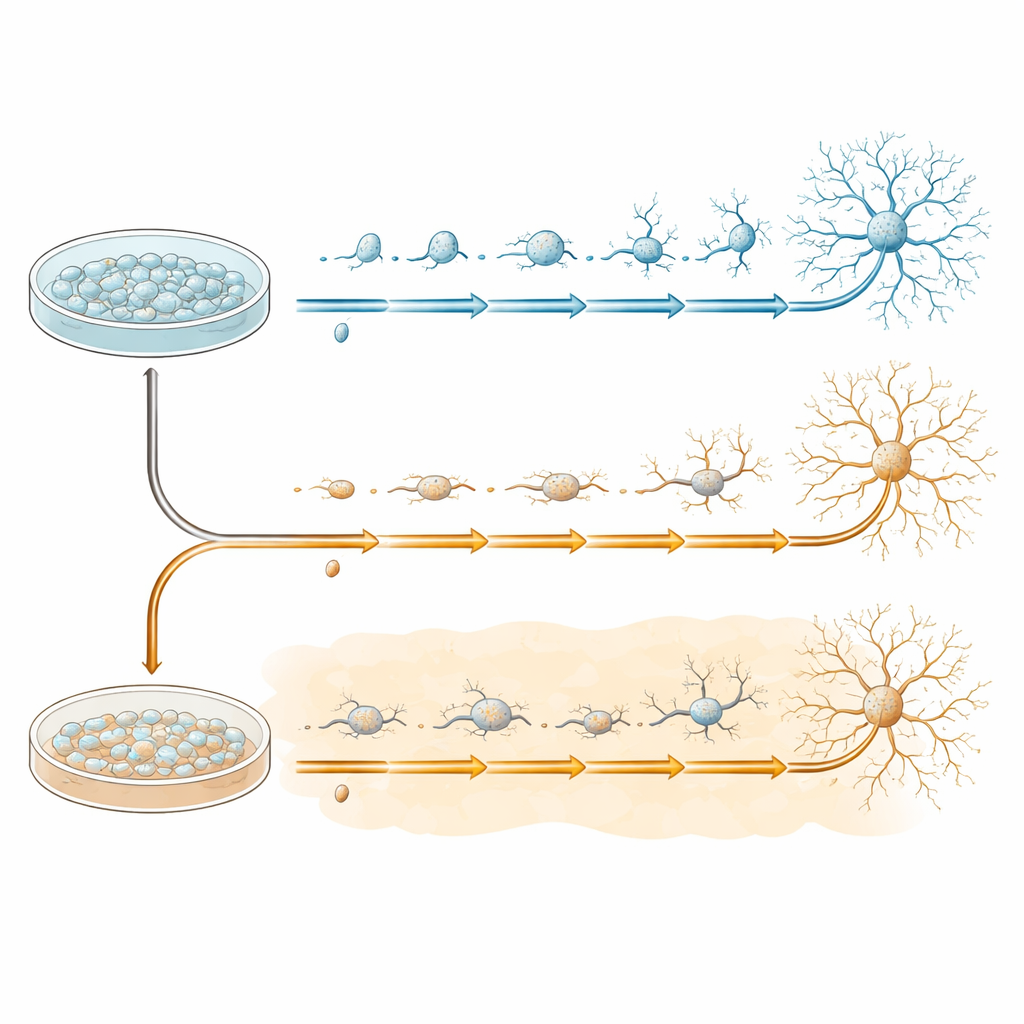
Gene abhören und das Genom öffnen
Was diese Arbeit besonders macht, ist, dass jede Zelle auf zwei komplementäre Arten untersucht wurde. Zunächst nutzten die Forschenden Einzelzell‑RNA‑Sequenzierung, um zu messen, welche Gene in mehr als 42.000 Zellen aktiviert waren. Zweitens verwendeten sie Einzelzell‑ATAC‑Sequenzierung in über 30.000 Zellen, um zu sehen, welche DNA‑Bereiche physisch zugänglich sind – ein Hinweis darauf, dass diese Regionen als Schalter zur Genregulation dienen können. Anspruchsvolle Rechenmethoden gruppierten Zellen in Cluster, ordneten sie entlang entwicklungsbezogener „Trajektorien“ von Vorläufern zu reiferen Neuronen und astrozytenähnlichen Zellen und verknüpften Muster der Genaktivität mit Veränderungen im Chromatin, dem DNA‑Protein‑Material, das unsere Gene verpackt.
Die Reise von Stammzellen zu Neuronen nachzeichnen
Innerhalb der sich entwickelnden neuronalen Zellen identifizierte das Team eine Reihe von fünf groben Stadien, bezeichnet mit A bis E, die einen schrittweisen Übergang von teilenden, stammzellähnlichen Zellen zu reifenden Neuronen mit komplexen Verzweigungen widerspiegeln. Klassische Marker‑Gene für frühe und späte neuronale Zustände veränderten sich in geordneter Weise entlang dieses Pfads, und eine unabhängige „Pseudotime“‑Analyse bestätigte dieselbe Reihenfolge. In späteren Stadien zoomten sie weiter hinein und fanden Unterwege unter den reiferen Zellen, die zeigen, dass einige Zellen leicht unterschiedliche Routen einschlagen, während sie ihre Identität verfeinern. Über diese Schritte hinweg katalogisierten die Wissenschaftler Gene, die gemeinsam verändert werden, Gene, die bei Amyloid‑beta‑Präsenz anders reagieren, und Genmengen, die offenbar nur unter Amyloid‑beta‑Exposition verändert sind.
Was Amyloid‑beta verändert – und was es intakt lässt
Obwohl die Gesamtstruktur der Entwicklungswege mit und ohne Amyloid‑beta ähnlich war, entdeckte das Team markante Verschiebungen darin, welche Gene in bestimmten Stadien bei Vorhandensein des Peptids stärker oder schwächer aktiv waren. Viele dieser Gene sind an der Kommunikation von Nervenzellen, am Wachstum von Axonen und Dendriten und an anderen Funktionen beteiligt, die für gesunde neuronale Schaltkreise entscheidend sind. Die Forschenden kombinierten außerdem Genaktivitäts‑ und Chromatin‑Daten, um Netzwerke zu erstellen, die Schlüsselkontrollproteine, sogenannte Transkriptionsfaktoren, mit Zielgenen verknüpfen. Sie entdeckten Tausende solcher „Regulons“ und zeigten, dass sich einige zwischen den Normal‑ und Amyloid‑beta‑Bedingungen unterschiedlich verhalten, obwohl großskalige Veränderungen in der DNA‑Zugänglichkeit relativ moderat bleiben. 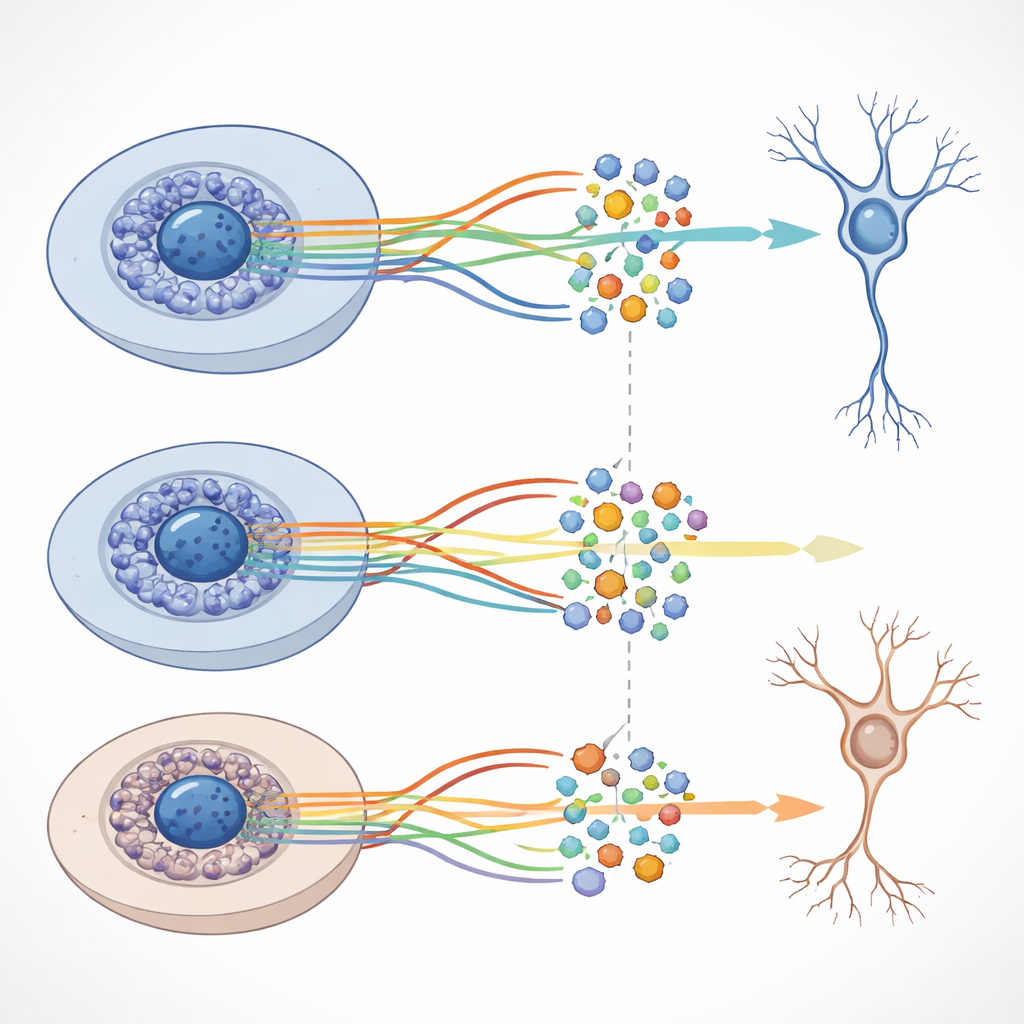
Laborbefunde mit menschlichen Alzheimer‑Gehirnen verbinden
Um die Relevanz ihres Zellkultursystems für die reale Erkrankung zu prüfen, verglichen die Autorinnen und Autoren ihre Genlisten mit einem bestehenden Datensatz von Hirngewebe von Menschen mit und ohne Alzheimer. Mehrere der gleichen Gene, die zwischen normalen und Amyloid‑beta‑behandelten Zellen unterschieden, unterschieden sich auch zwischen Kontroll‑ und Alzheimer‑Gehirnen. Behandelten sie Gruppen entwicklungsstadiumspezifischer Gene als „Signaturen“, so waren diese Signaturen in den Veränderungen, die in Patienten‑Hippocampusproben beobachtet wurden, angereichert – insbesondere für Gene, die mit neuronaler Kommunikation und Struktur verknüpft sind. Das deutet darauf hin, dass das In‑vitro‑Modell sinnvolle Aspekte der Biologie einfängt, die in den empfindlichen Erinnerungszentren des alternden Gehirns stattfinden.
Was diese Ressource für die Zukunft bietet
Das Hauptprodukt dieser Arbeit ist kein einzelnes Schlagzeilenergebnis, sondern ein öffentlicher, wiederverwendbarer Datensatz. Alle Roh‑ und verarbeiteten Informationen, zusammen mit Analysecode und einem interaktiven Webbrowser, sind frei verfügbar für andere Wissenschaftler. Forschende können diese Karte nutzen, um neue Rechenwerkzeuge zu benchmarken, zu erforschen, wie unterschiedliche Laborprotokolle die Neuronenentwicklung beeinflussen, oder neue Hypothesen darüber zu testen, wie Alzheimer‑verknüpfte Prozesse die Entstehung und Reifung von Gehirnzellen stören. Einfach gesagt liefert die Studie ein detailliertes „Schaltbild“ davon, wie junge menschliche Gehirnzellen wachsen – mit und ohne einen zentralen Alzheimer‑verknüpften Stressfaktor –, das dem Feld helfen wird zu verstehen, wann und wo Dinge schiefgehen.
Zitation: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Schlüsselwörter: Alzheimer‑Krankheit, Neurogenese, Einzelzellsequenzierung, Amyloid‑Beta, neurale Differenzierung