Clear Sky Science · ar
تمايز الخلايا العصبية البشرية تحت تعرّض Aβ: مجموعة بيانات أُحادية الخلية للنصوص والابيجينوم
لماذا تهم هذه الدراسة الخلوية الدماغية
يسلب مرض ألزهايمر الذاكرة والقدرات الفكرية تدريجياً، وما زلنا لا نفهم تماماً ما يحدث للخلايا الدماغية الوليدة أثناء تطور المرض. تبتكر هذه الدراسة «خريطة» مفصّلة لكيفية تطور الخلايا العصبية البشرية في المختبر عند تعرّضها للأميلويد‑بيتا، وهو قطعة بروتينية صغيرة تتراكم في أدمغة المصابين بألزهايمر. من خلال تتبّع آلاف الخلايا واحدة تلو الأخرى، والنظر ليس فقط إلى الجينات النشطة بل أيضاً إلى كيفية تغليف الحمض النووي، يوفر الباحثون خريطة مرجعية غنية يمكن لعلماء آخرين استخدامها للتحقيق في التغيرات المبكرة المرتبطة بالخرف.
بناء خلايا دماغية في طبق
لدراسة التطور المبكر للخلايا العصبية بطريقة مضبوطة، استخدم الفريق خلايا جذعية بشرية مستحثة متعددة القدرات، التي يمكن دفعها لتصبح خلايا سلف عصبية — المادة الأولية للعديد من أنواع خلايا الدماغ. نمت هذه الخلايا السلفية في أطباق ثم نُقلت إلى وسط خاص يشجعها على التحول إلى خلايا عصبية أكثر نضجاً خلال 20 يوماً. تابعت بعض الأطباق هذا البرنامج في ظل ظروف طبيعية، بينما تعرّضت أطباق أخرى منذ البداية للأميلويد‑بيتا 1–42، الببتيد نفسه الذي يشكل لويحات في مرض ألزهايمر. جُمعت خلايا المجموعتين في أربع لحظات رئيسية — قبل التغيير (اليوم 0) وخلال التحول (الأيام 7 و13 و20) — لالتقاط انفتاح مسارات تطورها خطوة بخطوة. 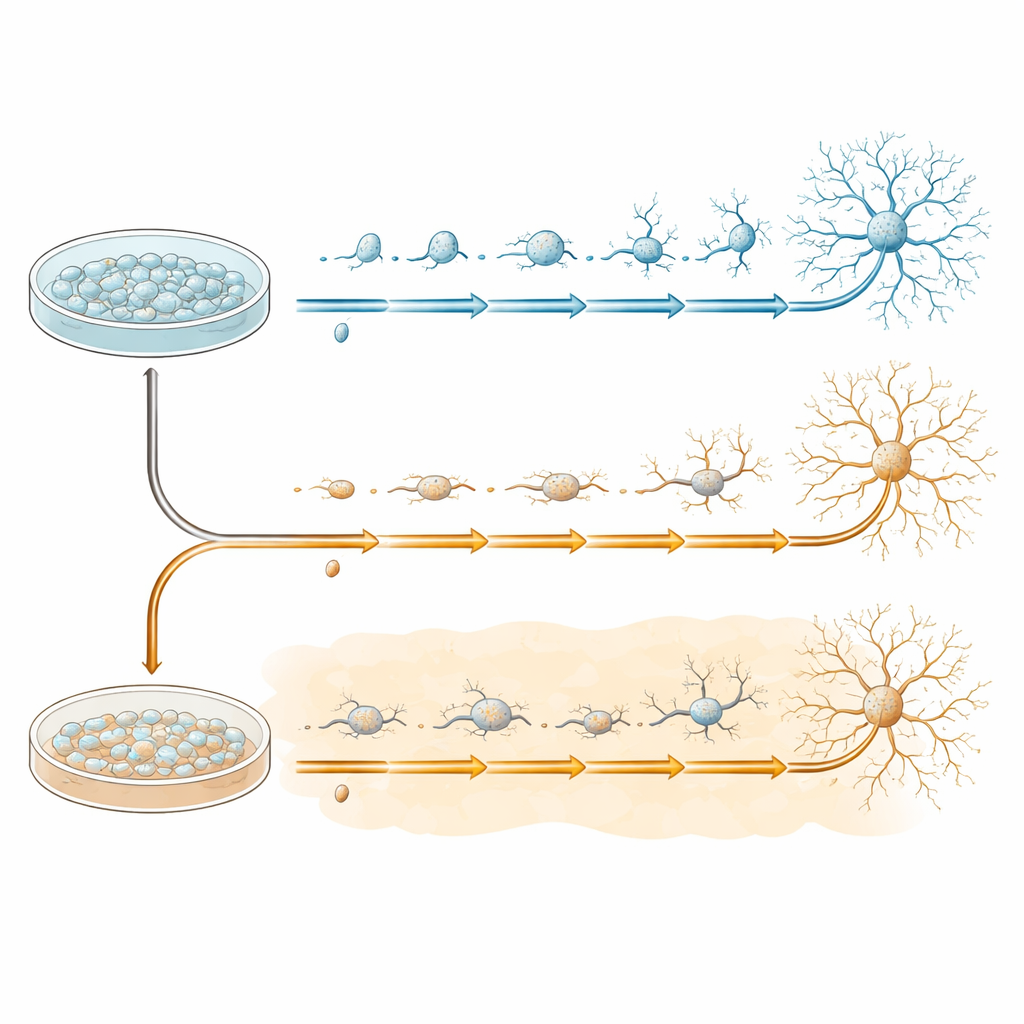
الاستماع إلى الجينات وفتح الجينوم
ما يميز هذا العمل هو فحص كل خلية بطريقتين مكملتين. أولاً، استخدم الباحثون تسلسل الحمض النووي الريبي أحادي الخلية لقياس الجينات النشطة في أكثر من 42,000 خلية. ثانياً، استخدموا تسلسل ATAC أحادي الخلية في أكثر من 30,000 خلية لرؤية أجزاء الحمض النووي التي كانت متاحة مادياً، وهو مؤشر على أنّ هذه المناطق يمكن أن تعمل كمفاتيح للتحكم في الجينات. جمّعت طرق حاسوبية متقدمة الخلايا في مجموعات، ورتبتها على امتداد «مسارات» تطورية من الخلايا السلفية إلى الخلايا العصبية الأكثر نضجاً والخلايا الشبيهة بالأستروسايت، وربطت أنماط نشاط الجينات بتغيرات في الكروماتين، مادة الحمض النووي‑البروتين التي تغلف جيناتنا.
تتبّع الرحلة من الخلايا الجذعية إلى الخلايا العصبية
داخل الخلايا العصبية النامية، حدد الفريق سلسلة من خمس مراحل عريضة، موسومة A إلى E، تعكس تحولاً تدريجياً من خلايا شبيهة بالجذع المنقسمة نحو خلايا عصبية ناضجة ذات امتدادات معقدة. تغيّرت جينات العلامة التقليدية للحالات العصبية المبكرة والمتأخرة بشكل منظم على طول هذا المسار، وأكد تحليل «الزمن الكاذب» المستقل نفس التسلسل. في المراحل المتأخرة، تعمقوا أكثر ووجدوا مسارات فرعية بين الخلايا الأكثر نضجاً، مبينين أن بعض الخلايا تتبع طرقاً مختلفة قليلاً أثناء تحديد هويتها. عبر هذه المراحل، صنّف العلماء الجينات التي تتغير معاً، والجينات التي تستجيب بشكل مختلف عند وجود الأميلويد‑بيتا، ومجموعات الجينات التي تبدو متغيرة فقط تحت تعرّض الأميلويد‑بيتا.
ما الذي يغيره الأميلويد‑بيتا — وما يتركه دون تغيير
على الرغم من أن البنية العامة للمسارات التطورية كانت متشابهة مع وبدون الأميلويد‑بيتا، كشف الفريق عن تحولات مميزة في الجينات الأكثر أو الأقل نشاطاً في مراحل معينة عند وجود الببتيد. كثير من هذه الجينات تشارك في تواصل الخلايا العصبية، ونمو المحاور والتغصّنات، ووظائف أخرى حاسمة لشبكات الدماغ السليمة. كما دمج الباحثون بيانات نشاط الجينات والكروماتين لبناء شبكات تربط بروتينات التحكم الرئيسية، المسماة عوامل النسخ، بمجموعات من الجينات المستهدفة. اكتشفوا آلاف من هذه «الرجولونات» وأظهروا أن بعضاً منها يتصرف بشكل مختلف بين الظروف الطبيعية وظروف الأميلويد‑بيتا، رغم أن تغيّرات إمكانية الوصول إلى الحمض النووي على نطاق واسع ظلت معتدلة. 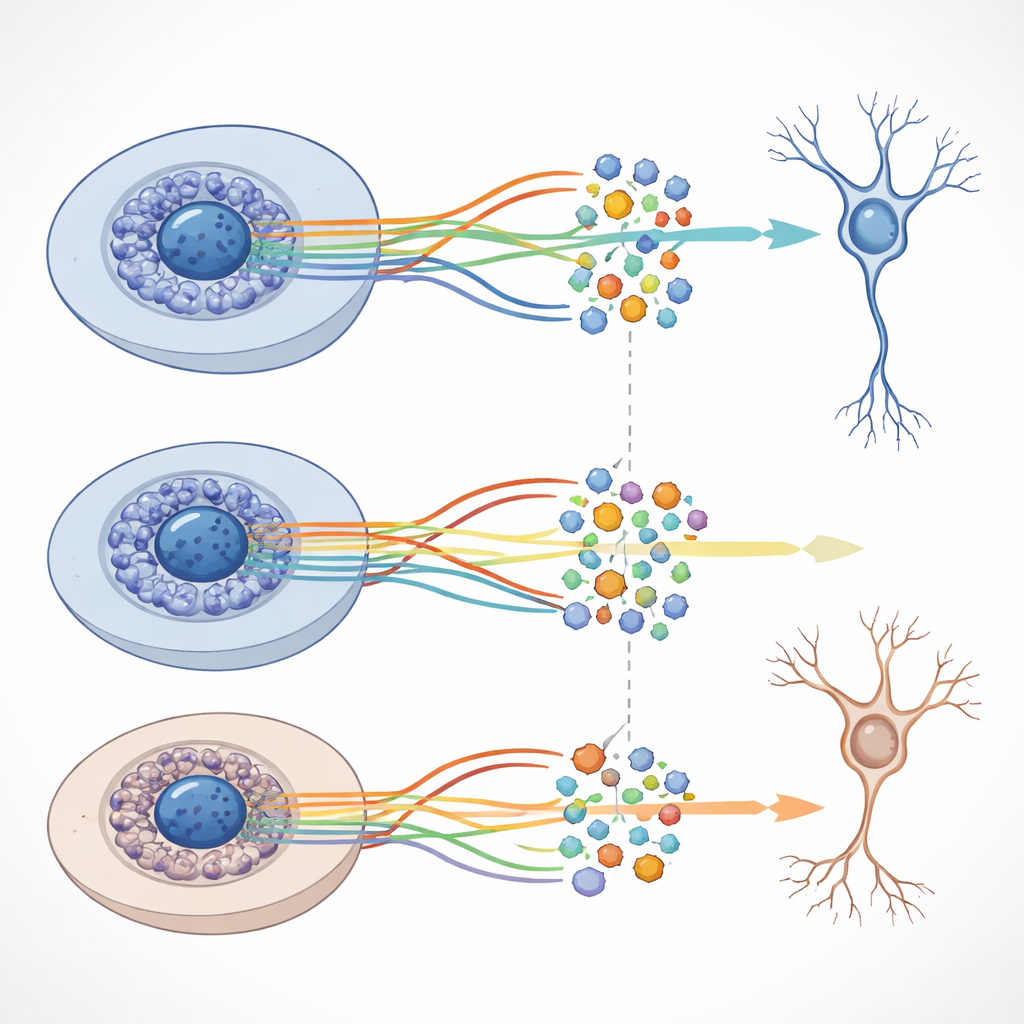
ربط نتائج المختبر بأدمغة مرضى ألزهايمر
للاطلاع على مدى أهمية نظام زرع الخلايا لديهم بالنسبة للمرض الحقيقي، قارن المؤلفون قوائم جيناتهم مع مجموعة بيانات موجودة لأنسجة الدماغ من أشخاص مصابين وغير مصابين بألزهايمر. تبين أن عدداً من الجينات نفسها التي اختلفت بين الخلايا المعالجة بالأميلويد‑بيتا والطبيعية اختلفت أيضاً بين أدمغة الضابطة وأدمغة ألزهايمر. عندما اعتبروا مجموعات الجينات الخاصة بمراحل التطور كـ«توقيعات»، كانت هذه التوقيعات غنية ضمن التغيرات المرصودة في عينات الحصين للمرضى، خاصة للجينات المرتبطة بتواصل وبنية الخلايا العصبية. يشير ذلك إلى أن النموذج المختبري يلتقط أجزاء ذات معنى من البيولوجيا الجارية في مراكز الذاكرة المعرضة للخطر في الدماغ المسن.
ما الذي يقدمه هذا المورد للمستقبل
المنتج الرئيسي لهذا العمل ليس نتيجة واحدة عناوينية، بل مجموعة بيانات عامة قابلة لإعادة الاستخدام. كل البيانات الخام والمعالجة، إلى جانب شيفرة التحليل ومتصفح ويب تفاعلي، متاحة مجاناً لعلماء آخرين. يمكن للباحثين استخدام هذه الخريطة لمعايرة أدوات حاسوبية جديدة، أو استكشاف كيف تؤثر بروتوكولات المختبر المختلفة على تطور الخلايا العصبية، أو اختبار أفكار جديدة حول كيفية تعطيل عمليات مرتبطة بألزهايمر لولادة ونضج خلايا الدماغ. ببساطة، تقدّم الدراسة «مخطط أسلاك» مفصلاً لكيفية نمو الخلايا الدماغية البشرية الشابة — مع وبدون عامل ضغط مرتبط بألزهايمر — ما سيساعد المجال على تفكيك متى وأين يحدث الخلل.
الاستشهاد: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
الكلمات المفتاحية: مرض ألزهايمر, تكوّن الأعصاب, تسلسل أحادي الخلية, أميлоيد بيتا, تمايز عصبي