Clear Sky Science · nl
Differentiering van menselijke neuronen onder Aβ‑blootstelling: een single‑cell transcriptomisch en epigenomisch dataset
Waarom deze studie van hersencellen ertoe doet
De ziekte van Alzheimer berooft mensen geleidelijk van geheugen en denkvermogen, maar we begrijpen nog niet volledig wat er met pasgevormde hersencellen gebeurt naarmate de ziekte voortschrijdt. Deze studie creëert een gedetailleerde “atlas” van hoe menselijke zenuwcellen zich in het laboratorium ontwikkelen wanneer ze worden blootgesteld aan amyloïd‑beta, een klein eiwitfragment dat zich ophoopt in de hersenen van Alzheimer‑patiënten. Door duizenden cellen één voor één te volgen, en niet alleen te kijken welke genen actief zijn maar ook hoe het DNA georganiseerd is, bieden de onderzoekers een rijke referentiekaart die andere wetenschappers kunnen gebruiken om vroege veranderingen gerelateerd aan dementie te onderzoeken.
Hersencellen kweken in een schaaltje
Om vroege ontwikkeling van zenuwcellen op een gecontroleerde manier te bestuderen, gebruikte het team menselijke geïnduceerde pluripotente stamcellen, die gestimuleerd kunnen worden om neurale voorlopercellen te worden—het uitgangsmateriaal voor veel hersenceltypen. Deze voorlopercellen werden in schalen gekweekt en vervolgens overgezet in een speciaal medium dat ze over 20 dagen aanmoedigt om zich tot meer rijpe neuronen te ontwikkelen. Sommige schalen volgden dit traject onder normale omstandigheden, terwijl andere vanaf het begin werden blootgesteld aan amyloïd‑beta 1–42, hetzelfde peptide dat plaques vormt bij de ziekte van Alzheimer. Cellen uit beide groepen werden op vier sleutelmomenten verzameld—voor de verandering (dag 0) en tijdens de transformatie (dagen 7, 13 en 20)—om het stapsgewijze verloop van hun ontwikkelingspaden vast te leggen. 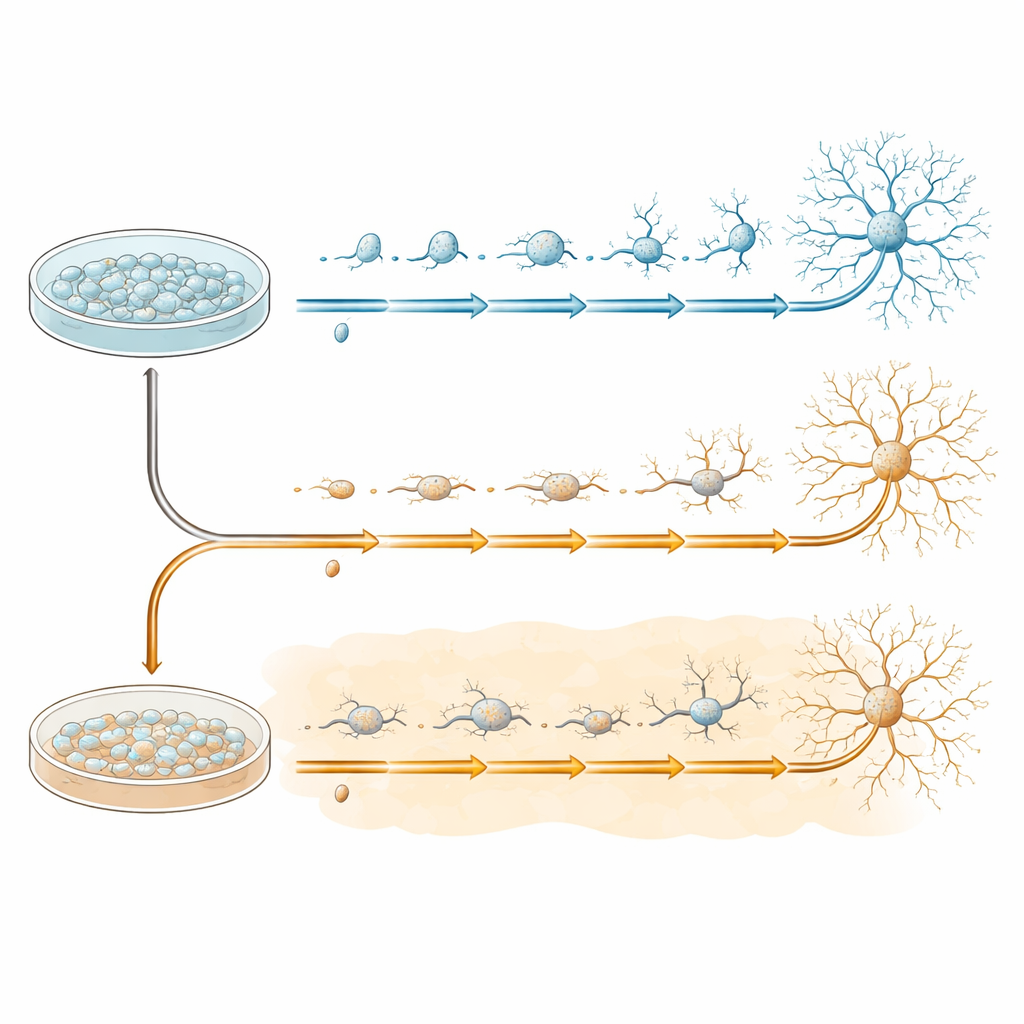
Luisteren naar genen en het openen van het genoom
Wat dit werk onderscheidt, is dat elke cel op twee aanvullende manieren werd onderzocht. Ten eerste gebruikten de onderzoekers single‑cell RNA sequencing om te meten welke genen in meer dan 42.000 cellen werden aangeschakeld. Ten tweede gebruikten ze single‑cell ATAC sequencing in meer dan 30.000 cellen om te zien welke delen van het DNA fysiek toegankelijk waren, een teken dat die regio’s als schakelaars kunnen fungeren om genen te regelen. Geavanceerde computationele methoden groepeerden cellen in clusters, rangschikten ze langs ontwikkelings“trajecten” van voorlopercellen naar meer rijpe neuronen en astrocyt‑achtige cellen, en koppelden patronen van genactiviteit aan veranderingen in chromatine, het DNA‑eiwitmateriaal dat onze genen verpakt.
Het volgen van de reis van stamcellen naar neuronen
Binnen de ontwikkelende neuronale cellen identificeerde het team een reeks van vijf brede stadia, gelabeld A tot en met E, die een geleidelijke verschuiving weergeven van delende stam‑achtige cellen naar rijpende neuronen met complexe vertakkingen. Klassieke merkergenen voor vroege en late neuronale toestanden veranderden op ordelijke wijze langs dit pad, en een onafhankelijke “pseudotime” analyse bevestigde dezelfde volgorde. In latere stadia zoomden ze verder in en vonden subpaden onder meer rijpe cellen, wat aantoont dat sommige cellen licht verschillende routes volgen terwijl ze hun identiteit verfijnen. In deze stappen catalogueerden de wetenschappers genen die samen veranderen, genen die anders reageren wanneer amyloïd‑beta aanwezig is, en groepen genen die schijnbaar alleen onder amyloïd‑beta‑blootstelling worden aangepast.
Wat amyloïd‑beta verandert — en wat intact blijft
Hoewel de algemene structuur van de ontwikkelingspaden vergelijkbaar was met en zonder amyloïd‑beta, detecteerde het team duidelijke verschuivingen in welke genen op bepaalde stadia meer of minder actief waren wanneer het peptide aanwezig was. Veel van deze genen zijn betrokken bij neuronale communicatie, groei van axonen en dendrieten en andere functies die cruciaal zijn voor gezonde hersencircuits. De onderzoekers combineerden ook de gen‑activiteits‑ en chromatinegegevens om netwerken te bouwen die sleutelcontrole eiwitten, transcriptiefactoren genoemd, koppelen aan sets doelfgenen. Ze ontdekten duizenden zulke “regulons” en toonden aan dat sommige ervan zich anders gedragen tussen de normale en amyloïd‑beta‑condities, hoewel grootschalige veranderingen in DNA‑toegankelijkheid beperkt bleven. 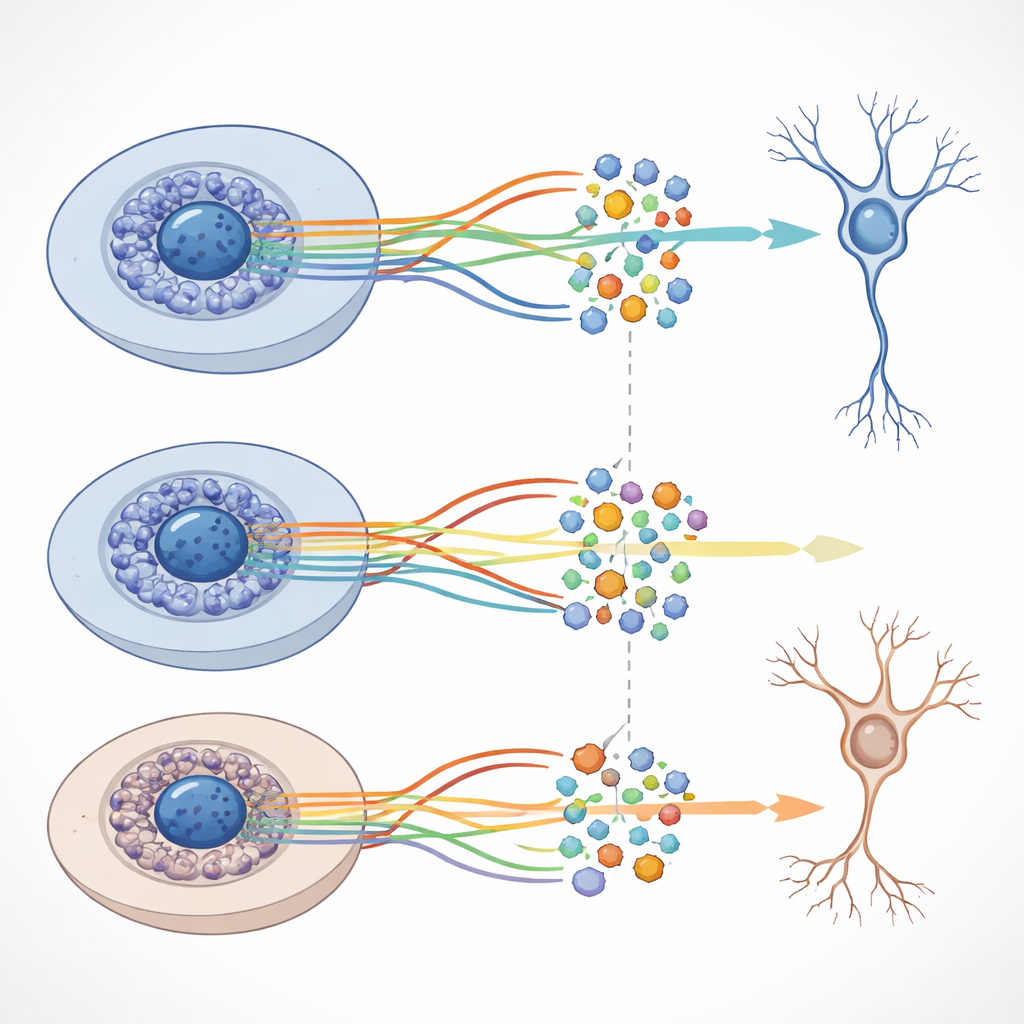
Laboratoriumbevindingen koppelen aan menselijke Alzheimer‑hersenen
Om te beoordelen hoe relevant hun kweekmodel is voor de echte ziekte, vergeleken de auteurs hun genlijsten met een bestaande dataset van hersenweefsel van mensen met en zonder Alzheimer. Verschillende van dezelfde genen die verschilden tussen normale en amyloïd‑beta‑behandelde cellen, verschilden ook tussen controlemateriaal en Alzheimer‑hersenen. Wanneer ze groepen ontwikkelingsstadium‑specifieke genen als “handtekeningen” behandelden, waren deze handtekeningen verrijkt in de veranderingen die werden gezien in hippocampus‑monsters van patiënten, vooral voor genen gekoppeld aan neuronale communicatie en structuur. Dit suggereert dat het in‑vitro model betekenisvolle onderdelen van de biologie vastlegt die optreden in de kwetsbare geheugencentra van het ouder wordende brein.
Wat deze bron voor de toekomst biedt
Het belangrijkste product van dit werk is niet één kopnieuwsresultaat, maar een openbare, herbruikbare dataset. Alle ruwe en verwerkte informatie, samen met analysecode en een interactieve webbrowser, zijn vrij beschikbaar voor andere wetenschappers. Onderzoekers kunnen deze kaart gebruiken om nieuwe computationele tools te benchmarken, te onderzoeken hoe verschillende laboratoriumprotocollen de neuronale ontwikkeling beïnvloeden, of nieuwe ideeën te testen over hoe Alzheimer‑gerelateerde processen de geboorte en rijping van hersencellen verstoren. Simpel gezegd biedt de studie een gedetailleerd “bedradingsdiagram” van hoe jonge menselijke hersencellen groeien—met en zonder een belangrijke Alzheimer‑gekoppelde stressor—dat het veld zal helpen uitzoeken wanneer en waar het misgaat.
Bronvermelding: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Trefwoorden: Ziekte van Alzheimer, neurogenese, single‑cell sequencing, amyloïd‑beta, neurale differentiatie