Clear Sky Science · es
Diferenciación neuronal humana bajo exposición a Aβ: un conjunto de datos transcriptómicos y epigenómicos a nivel de célula única
Por qué importa este estudio sobre células cerebrales
La enfermedad de Alzheimer roba lentamente la memoria y las capacidades cognitivas, pero aún no comprendemos por completo qué les ocurre a las células cerebrales recién formadas a medida que avanza la enfermedad. Este estudio crea un “atlas” detallado de cómo se desarrollan en el laboratorio las neuronas humanas cuando están expuestas a la beta‑amiloide, un pequeño fragmento proteico que se acumula en los cerebros con Alzheimer. Al seguir miles de células una por una y observar no solo qué genes están activos sino también cómo está empaquetado el ADN, los investigadores ofrecen un mapa de referencia rico que otros científicos pueden usar para investigar cambios tempranos vinculados a la demencia.
Construir células cerebrales en un plato
Para estudiar el desarrollo temprano de las neuronas de forma controlada, el equipo utilizó células madre pluripotentes inducidas humanas, que pueden ser inducidas a convertirse en células progenitoras neurales—el material de partida para muchos tipos celulares del cerebro. Estas progenitoras se cultivaron en placas y luego se cambiaron a un medio especial que las estimula a convertirse en neuronas más maduras durante 20 días. Algunas placas siguieron este programa en condiciones normales, mientras que otras estuvieron expuestas desde el inicio a beta‑amiloide 1–42, el mismo péptido que forma placas en la enfermedad de Alzheimer. Se recogieron células de ambos grupos en cuatro momentos clave—antes del cambio (día 0) y durante la transformación (días 7, 13 y 20)—para capturar paso a paso el desenvolvimiento de sus trayectorias de desarrollo. 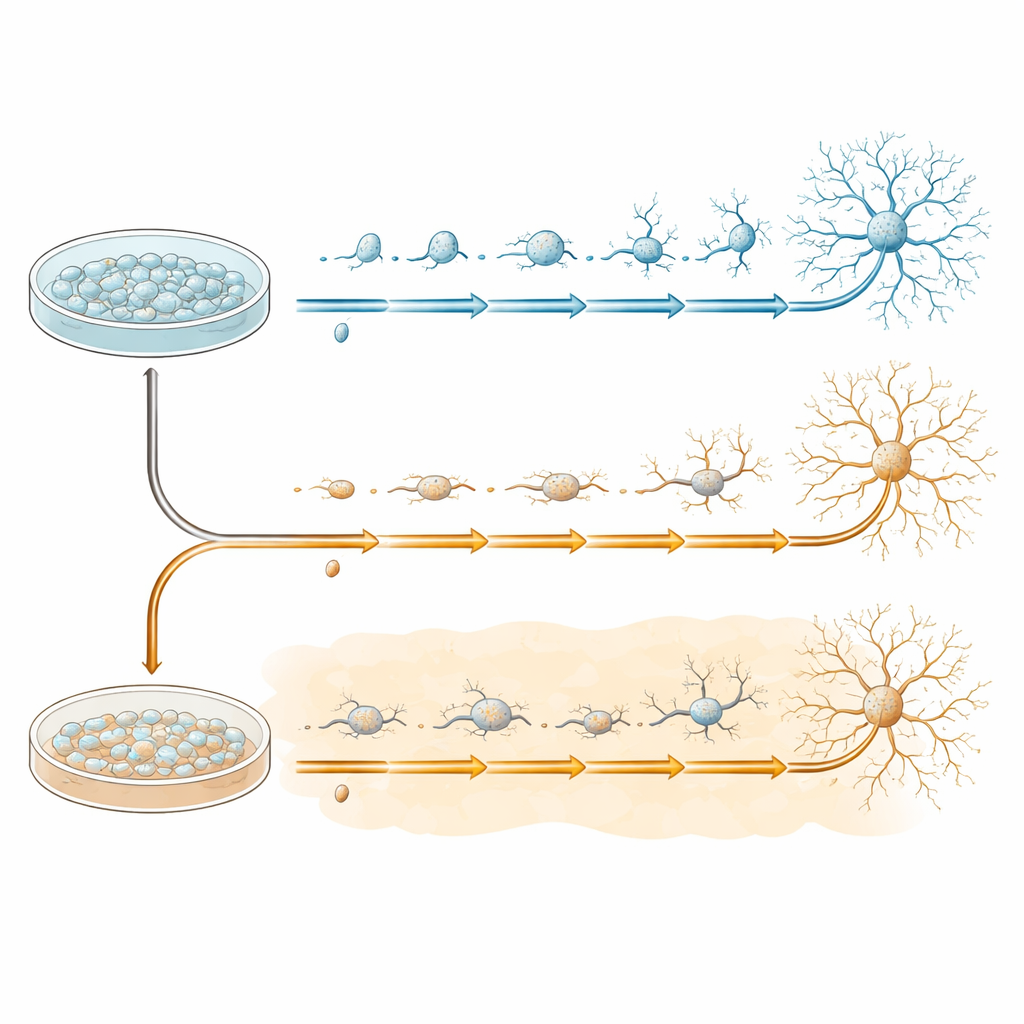
Escuchar a los genes y abrir el genoma
Lo que distingue a este trabajo es que cada célula fue examinada de dos maneras complementarias. Primero, los investigadores usaron secuenciación de ARN de célula única para medir qué genes estaban activados en más de 42.000 células. En segundo lugar, emplearon secuenciación ATAC de célula única en más de 30.000 células para ver qué regiones del ADN eran físicamente accesibles, una señal de que estas zonas pueden funcionar como interruptores para controlar la expresión génica. Métodos computacionales sofisticados agruparon las células en clústeres, las ordenaron a lo largo de “trayectorias” de desarrollo desde progenitores hasta neuronas más maduras y células con rasgos similares a astrocitos, y vincularon los patrones de actividad génica a cambios en la cromatina, el material ADN‑proteína que empaqueta nuestros genes.
Rastreando el viaje de las células madre a las neuronas
Dentro de las células neuronales en desarrollo, el equipo identificó una serie de cinco etapas generales, etiquetadas de la A a la E, que reflejan un desplazamiento gradual de células divisorias de tipo madre hacia neuronas en maduración con ramas complejas. Genes marcadores clásicos de estados neuronales tempranos y tardíos cambiaron de forma ordenada a lo largo de este recorrido, y un análisis independiente de “seudotiempo” confirmó la misma secuencia. En etapas posteriores, hicieron un zoom adicional y hallaron sub‑trayectorias entre células más maduras, mostrando que algunas siguen rutas ligeramente diferentes al afinar su identidad. A lo largo de estos pasos, los científicos catalogaron genes que cambian de forma concertada, genes que responden de manera distinta cuando está presente la beta‑amiloide y conjuntos de genes que parecen alterarse solo bajo exposición a la beta‑amiloide.
Lo que la beta‑amiloide altera — y lo que deja intacto
Aunque la estructura general de las trayectorias de desarrollo fue similar con y sin beta‑amiloide, el equipo detectó cambios distintos en qué genes estaban más o menos activos en etapas particulares cuando el péptido estaba presente. Muchos de estos genes participan en la comunicación neuronal, el crecimiento de axones y dendritas y otras funciones críticas para circuitos cerebrales saludables. Los investigadores también combinaron los datos de actividad génica y cromatina para construir redes que enlazan proteínas reguladoras clave, llamadas factores de transcripción, con conjuntos de genes diana. Descubrieron miles de tales “regulones” y mostraron que algunos se comportan de forma diferente entre las condiciones normales y las tratadas con beta‑amiloide, aunque los cambios a gran escala en la accesibilidad del ADN permanecen modestos. 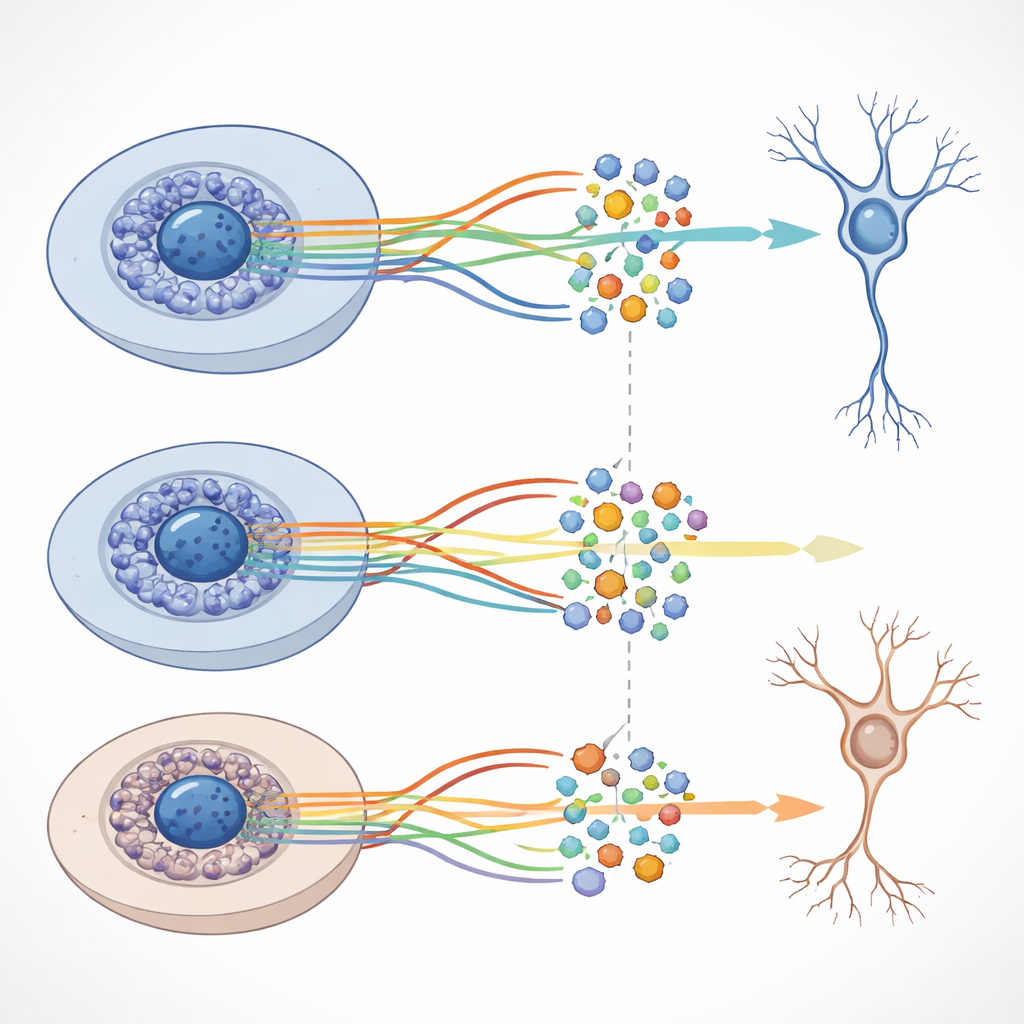
Conectar los hallazgos de laboratorio con cerebros humanos con Alzheimer
Para evaluar la relevancia de su sistema de cultivo celular respecto a la enfermedad real, los autores compararon sus listas de genes con un conjunto de datos existente de tejido cerebral de personas con y sin Alzheimer. Varios de los mismos genes que diferían entre células normales y tratadas con beta‑amiloide también diferían entre cerebros control y cerebros con Alzheimer. Cuando trataron grupos de genes específicos de estadios de desarrollo como “firmas”, estas firmas se enriquecieron entre los cambios observados en muestras de hipocampo de pacientes, especialmente para genes ligados a la comunicación y estructura neuronal. Esto sugiere que el modelo in vitro captura fragmentos significativos de la biología que ocurre en los centros de memoria vulnerables del cerebro envejecido.
Qué ofrece este recurso para el futuro
El producto principal de este trabajo no es un único resultado llamativo, sino un conjunto de datos público y reutilizable. Toda la información cruda y procesada, junto con el código de análisis y un navegador web interactivo, están disponibles libremente para otros científicos. Los investigadores pueden usar este mapa para evaluar nuevas herramientas computacionales, explorar cómo diferentes protocolos de laboratorio afectan el desarrollo neuronal o poner a prueba ideas sobre cómo los procesos relacionados con el Alzheimer interfieren en el nacimiento y la maduración de las células cerebrales. En términos simples, el estudio proporciona un “diagrama de cableado” detallado de cómo crecen las células cerebrales humanas jóvenes—con y sin un estresor clave vinculado al Alzheimer—que ayudará al campo a diseccionar cuándo y dónde algo sale mal.
Cita: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Palabras clave: Enfermedad de Alzheimer, neurogénesis, secuenciación de célula única, beta amiloide, diferenciación neuronal