Clear Sky Science · pl
Różnicowanie neuronów ludzkich pod wpływem Aβ: transkryptomiczne i epigenomiczne dane pojedynczych komórek
Dlaczego to badanie komórek mózgowych ma znaczenie
Choroba Alzheimera stopniowo odbiera ludziom pamięć i zdolności myślenia, lecz wciąż nie rozumiemy w pełni, co dzieje się z nowo powstającymi komórkami mózgu w miarę postępu choroby. To badanie tworzy szczegółowy „atlas” rozwoju ludzkich neuronów w warunkach laboratoryjnych, gdy są one wystawione na działanie amyloid‑beta, krótkiego fragmentu białka gromadzącego się w mózgach chorych na Alzheimera. Śledząc tysiące komórek pojedynczo i analizując nie tylko aktywność genów, ale także sposób pakowania DNA, autorzy oferują bogatą mapę odniesienia, z której inni naukowcy mogą korzystać, by badać wczesne zmiany związane z demencją.
Tworzenie komórek mózgowych w naczyniu
Aby badać wczesny rozwój neuronów w kontrolowany sposób, zespół wykorzystał ludzkie indukowane pluripotentne komórki macierzyste, które można skłonić do przekształcenia w progenitory nerwowe — materiał wyjściowy dla wielu typów komórek mózgu. Te progenitory hodowano w naczyniach, a następnie przestawiano do specjalnego medium sprzyjającego dojrzewaniu w kierunku neuronów przez 20 dni. Część naczyń prowadzono w warunkach kontrolnych, a inne od początku eksponowano na amyloid‑beta 1–42, ten sam peptyd tworzący blaszki w chorobie Alzheimera. Komórki z obu grup pobierano w czterech kluczowych momentach — przed zmianą (dzień 0) oraz w trakcie transformacji (dni 7, 13 i 20) — aby uchwycić krok po kroku rozwój ich ścieżek rozwojowych. 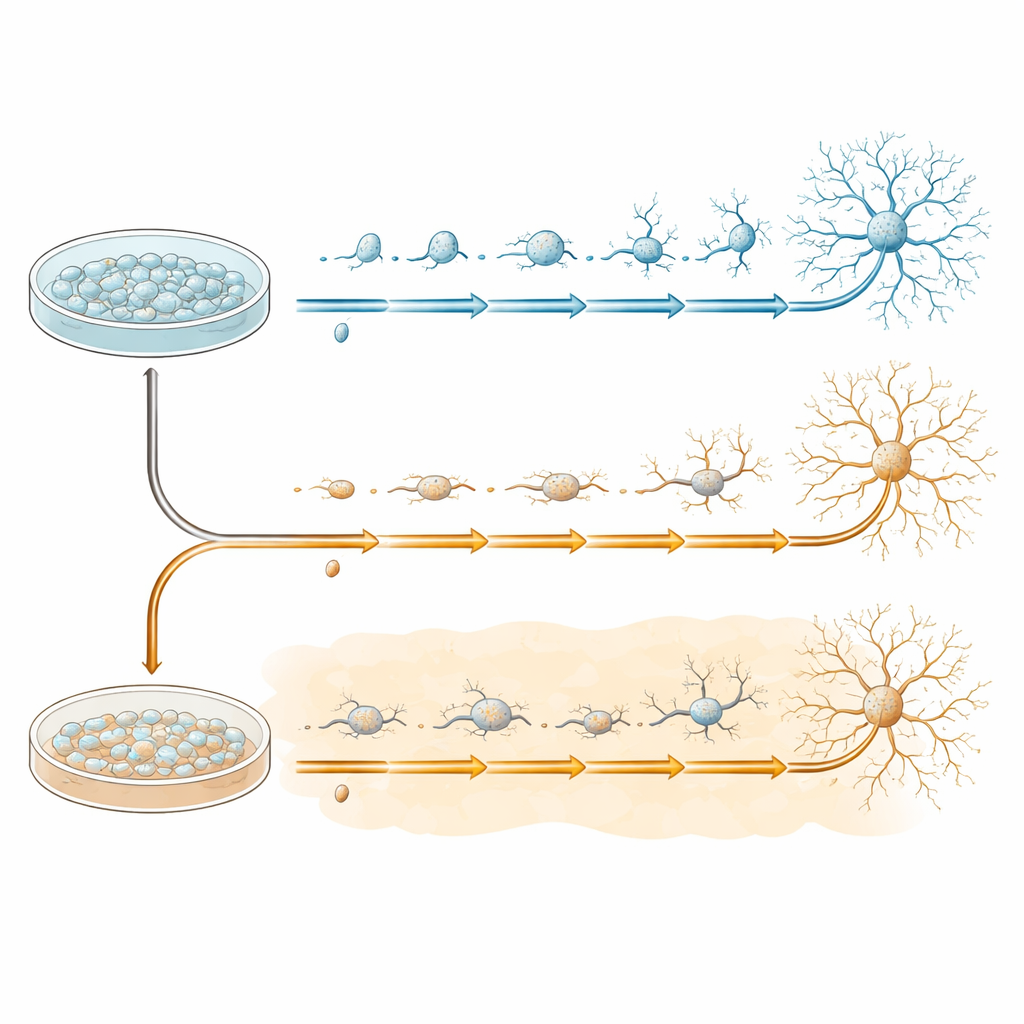
Słuchanie genów i otwieranie genomu
Co wyróżnia tę pracę, to fakt, że każda komórka została zbadana dwiema komplementarnymi metodami. Po pierwsze, badacze użyli sekwencjonowania RNA pojedynczych komórek, aby zmierzyć, które geny są aktywne w ponad 42 000 komórek. Po drugie, zastosowali sekwencjonowanie ATAC pojedynczych komórek w ponad 30 000 komórek, by zobaczyć, które fragmenty DNA są fizycznie dostępne — co świadczy o tym, że te regiony mogą działać jako przełączniki kontrolujące geny. Zaawansowane metody obliczeniowe pogrupowały komórki w klastry, uporządkowały je wzdłuż „trajektorii” rozwojowych od progenitorów do bardziej dojrzałych neuronów i komórek przypominających astrocyty oraz powiązały wzorce aktywności genów ze zmianami w chromatynie, materiale DNA‑białkowym pakującym nasze geny.
Śledzenie drogi od komórek macierzystych do neuronów
Wśród rozwijających się komórek neuronalnych zespół wyróżnił serię pięciu szerokich etapów, oznaczonych literami A–E, które odzwierciedlają stopniowe przejście od dzielących się komórek przypominających komórki macierzyste do dojrzewających neuronów o rozgałęzionej strukturze. Klasyczne markery genowe dla wczesnych i późnych stanów neuronalnych zmieniały się uporządkowanie wzdłuż tej ścieżki, a niezależna analiza „pseudoczasu” potwierdziła tę samą sekwencję. Na późniejszych etapach badacze przyjrzeli się uważniej i znaleźli pod‑ścieżki wśród bardziej dojrzałych komórek, pokazując, że niektóre komórki podążają nieco odmiennymi drogami w procesie wyspecjalizowania. W całym tym procesie naukowcy skatalogowali geny, które zmieniają się razem, geny reagujące odmiennie przy obecności amyloid‑beta oraz zestawy genów, które wydają się zmienione jedynie pod wpływem ekspozycji na amyloid‑beta.
Co zmienia amyloid‑beta — i co pozostawia bez zmian
Chociaż ogólna struktura ścieżek rozwojowych była podobna z amyloid‑beta i bez niego, zespół wykrył wyraźne przesunięcia w aktywności niektórych genów na konkretnych etapach, gdy peptyd był obecny. Wiele z tych genów bierze udział w komunikacji neuronów, wzroście aksonów i dendrytów oraz w innych funkcjach kluczowych dla zdrowych obwodów mózgowych. Badacze połączyli też dane o aktywności genów i o chromatynie, aby zbudować sieci łączące kluczowe białka kontrolne, zwane czynnikami transkrypcyjnymi, z zestawami genów docelowych. Odkryli tysiące takich „regulonów” i wykazali, że niektóre z nich zachowują się inaczej w warunkach kontrolnych i przy obecności amyloid‑beta, nawet jeśli zmiany dostępności DNA na dużą skalę pozostają umiarkowane. 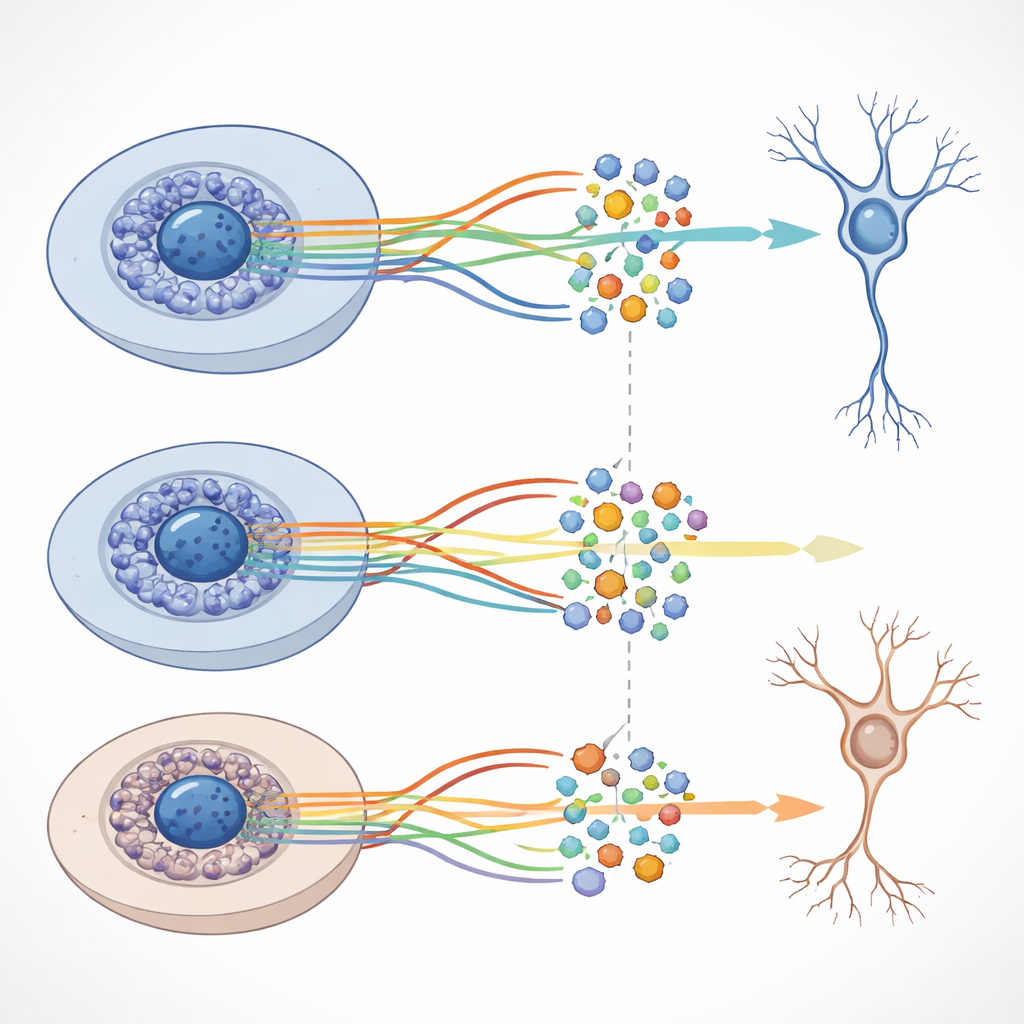
Łączenie wyników laboratoryjnych z mózgami osób chorych na Alzheimera
Aby sprawdzić, na ile ich model hodowli komórek odnosi się do rzeczywistej choroby, autorzy porównali swoje listy genów z istniejącym zbiorem danych z tkanki mózgowej osób z i bez choroby Alzheimera. Kilka z tych samych genów, które różniły się między komórkami kontrolnymi a traktowanymi amyloid‑beta, również różniło się między tkankami kontrolnymi a mózgami osób z Alzheimerem. Gdy traktowali grupy genów specyficznych dla etapów rozwojowych jako „sygnatury”, sygnatury te były wzbogacone wśród zmian obserwowanych w próbkach hipokampa pacjentów, szczególnie dla genów związanych z komunikacją neuronalną i strukturą. Sugeruje to, że model in vitro uchwycił istotne elementy biologii występującej w wrażliwych ośrodkach pamięci starzejącego się mózgu.
Co ten zasób oferuje na przyszłość
Głównym produktem tej pracy nie jest pojedynczy sensacyjny wynik, lecz publicznie dostępny, możliwy do ponownego wykorzystania zbiór danych. Wszystkie surowe i przetworzone informacje, wraz z kodem analitycznym oraz interaktywną przeglądarką internetową, są dostępne bezpłatnie dla innych naukowców. Badacze mogą używać tej mapy do oceny nowych narzędzi obliczeniowych, eksplorowania wpływu różnych protokołów laboratoryjnych na rozwój neuronów lub testowania nowych hipotez dotyczących tego, jak procesy związane z Alzheimerem zaburzają narodziny i dojrzewanie komórek mózgowych. Mówiąc prosto, badanie dostarcza szczegółowego „diagramu połączeń” pokazującego, jak rosną młode ludzkie komórki mózgowe — z i bez istotnego czynnika stresowego związanego z Alzheimerem — który pomoże środowisku naukowemu rozpoznać, kiedy i gdzie pojawiają się zaburzenia.
Cytowanie: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Słowa kluczowe: Choroba Alzheimera, neurogeneza, sekwencjonowanie pojedynczych komórek, amyloid beta, różnicowanie neuronów