Clear Sky Science · ru
Дифференцировка человеческих нейронов при воздействии Aβ: датасет одно‑клеточной транскриптомики и эпигеномики
Почему это исследование клеток мозга важно
Болезнь Альцгеймера постепенно лишает людей памяти и мышления, но мы до сих пор не полностью понимаем, что происходит с новорожденными клетками мозга по мере развития болезни. В этом исследовании создан подробный «атлас» того, как человеческие нервные клетки развиваются в лаборатории при воздействии амилоид‑бета — небольшого фрагмента белка, который накапливается в мозге при Альцгеймере. Отслеживая тысячи клеток по одной и изучая не только активность генов, но и то, как упакована ДНК, авторы предлагают богатую справочную карту, которую другие учёные могут использовать для изучения ранних изменений, связанных с деменцией.
Выращивание клеток мозга в чашке
Чтобы исследовать раннее развитие нервных клеток в контролируемых условиях, команда использовала человеческие индуцированные плюрипотентные стволовые клетки, которые можно направлять в нейрональные прогениторы — исходный материал для многих типов клеток мозга. Эти прогениторы выращивали в чашках и затем переводили в специальную среду, стимулирующую превращение в более зрелые нейроны в течение 20 дней. Некоторые чашки проходили этот процесс в нормальных условиях, а другие с самого начала подвергались воздействию амилоид‑бета 1–42 — того же пептида, который образует бляшки при болезни Альцгеймера. Клетки из обеих групп собирали в четыре ключевых момента — до изменения (день 0) и в ходе трансформации (дни 7, 13 и 20) — чтобы зафиксировать пошаговое развитие их траекторий. 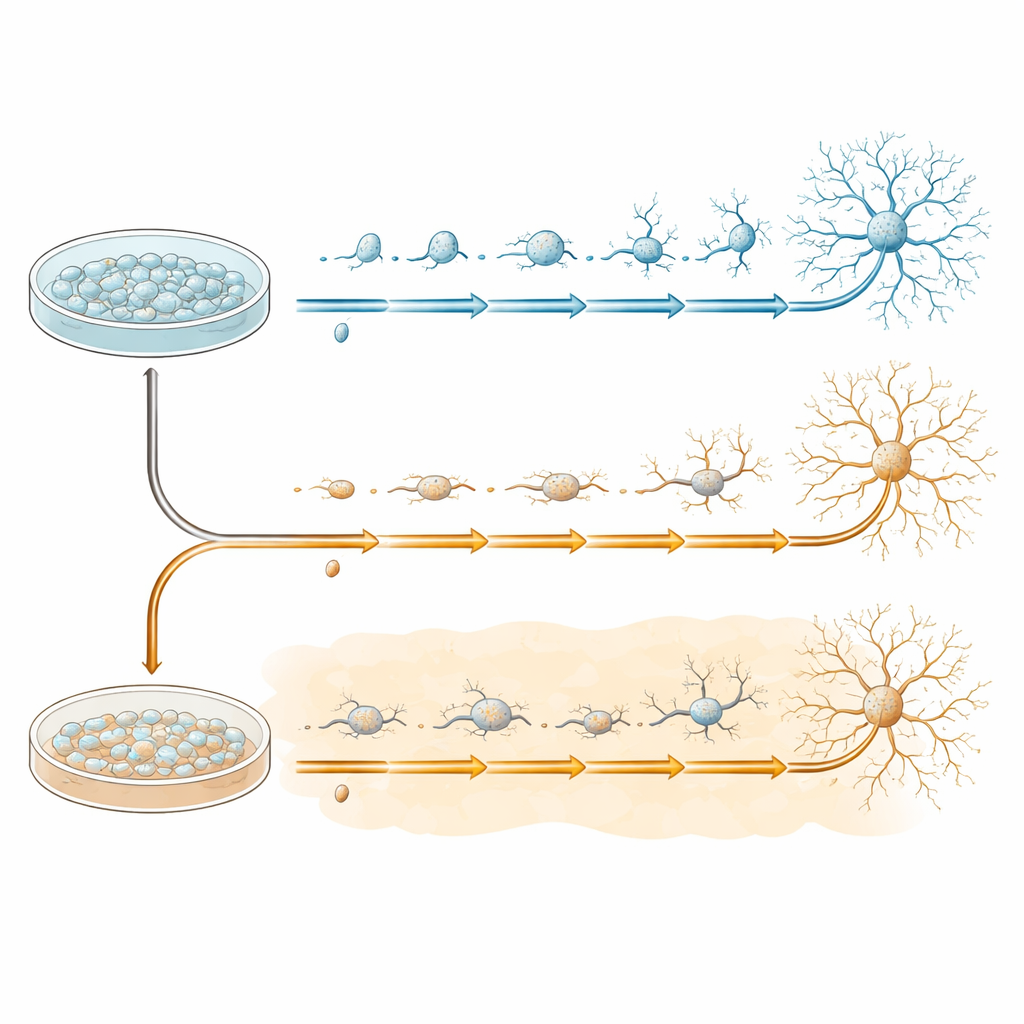
Слушая гены и раскрывая геном
Особенность работы в том, что каждую клетку исследовали двумя взаимодополняющими способами. Сначала авторы использовали одно‑клеточную РНК‑секвенцию, чтобы измерить, какие гены активны в более чем 42 000 клеток. Затем они провели одно‑клеточную ATAC‑секвенцию более чем в 30 000 клеток, чтобы определить, какие участки ДНК физически доступны — признак того, что эти регионы могут служить переключателями для управления генами. Сложные вычислительные методы сгруппировали клетки в кластеры, упорядочили их вдоль развивающихся «траекторий» от прогениторов к более зрелым нейронам и клеткам, напоминающим астроциты, и связали паттерны активности генов с изменениями в хроматине — ДНК‑белковом материале, упаковывающем наши гены.
От стволовых клеток к нейронам: отслеживание пути
В развивающихся нейрональных клетках команда выделила пять широких стадий, обозначенных буквами A–E, которые отражают постепенный переход от делящихся стволоподобных клеток к созревающим нейронам с разветвлёнными отростками. Классические маркерные гены ранних и поздних нейронных состояний менялись упорядоченно вдоль этого пути, а независимый анализ «псевдовремени» подтвердил ту же последовательность. На более поздних стадиях исследователи детализировали картину и обнаружили суб‑пути среди более зрелых клеток, показывающие, что некоторые клетки следуют слегка разным траекториям по мере уточнения своей идентичности. На всех этапах учёные каталогизировали гены, которые изменяются совместно, гены, по‑разному реагирующие при наличии амилоид‑бета, и наборы генов, изменяющихся только при экспозиции амилоид‑бета.
Что меняет амилоид‑бета — и что остаётся неизменным
Хотя общая структура траекторий развития была схожей с амилоид‑бета и без него, команда обнаружила отчётливые сдвиги в активности отдельных генов на конкретных стадиях при наличии пептида. Многие из этих генов вовлечены в передачу нервных сигналов, рост аксонов и дендритов и другие функции, критические для здоровых мозговых цепей. Исследователи также совместили данные об активности генов и хроматине, чтобы построить сети, связывающие ключевые регуляторные белки — транскрипционные факторы — с наборами целевых генов. Они выявили тысячи таких «регулонов» и показали, что некоторые из них ведут себя по‑разному в нормальных и амилоид‑бета условиях, хотя масштабные изменения доступности ДНК остаются умеренными. 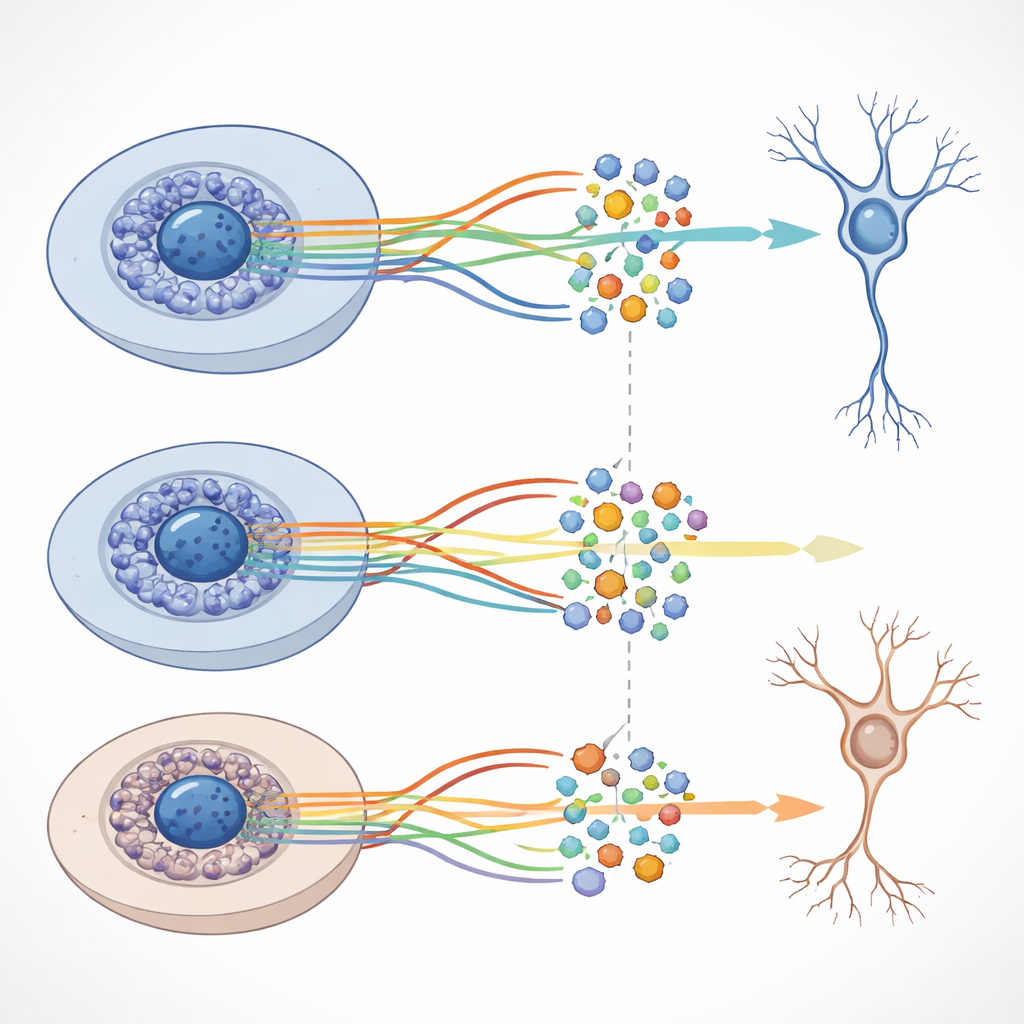
Соединяя лабораторные результаты с мозгами людей с Альцгеймером
Чтобы оценить релевантность своей культуры клеток реальному заболеванию, авторы сопоставили свои списки генов с существующим датасетом тканей мозга людей с болезнью Альцгеймера и без неё. Несколько тех же генов, отличавшихся между нормальными и обработанными амилоид‑бета клетками, также различались между контрольными и больными образцами. Рассматривая группы генов, специфичных для стадий развития, как «подписи», эти подписи оказались обогащёнными среди изменений, обнаруженных в образцах гиппокампа пациентов, особенно для генов, связанных с нейронной коммуникацией и структурой. Это указывает на то, что модель in vitro отражает значимые элементы биологии, происходящей в уязвимых центрах памяти стареющего мозга.
Что этот ресурс даёт на будущее
Главный продукт этой работы — не единичный заголовок, а публичный, многоразовый набор данных. Вся исходная и обработанная информация, вместе с кодом анализа и интерактивным веб‑просмотрщиком, доступна бесплатно для других учёных. Исследователи могут использовать эту карту для проверки новых вычислительных инструментов, изучать, как разные лабораторные протоколы влияют на развитие нейронов, или тестировать гипотезы о том, как процессы, связанные с Альцгеймером, нарушают рождение и созревание клеток мозга. Проще говоря, исследование предоставляет подробную «схему проводки» того, как молодые человеческие клетки мозга растут — с ключевым стрессором, связанным с Альцгеймером, и без него — что поможет полю разобраться, когда и где происходят сбои.
Цитирование: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Ключевые слова: Болезнь Альцгеймера, нейрогенез, одно‑клеточное секвенирование, амилоид‑бета, нейронная дифференцировка