Clear Sky Science · pt
Diferenciação neuronal humana sob exposição a Aβ: um conjunto de dados transcriptômicos e epigenômicos em célula única
Por que este estudo de células cerebrais é importante
A doença de Alzheimer rouba lentamente a memória e a capacidade cognitiva das pessoas, mas ainda não compreendemos totalmente o que acontece com as células cerebrais recém‑formadas à medida que a doença progride. Este estudo cria um “atlas” detalhado de como os neurônios humanos se desenvolvem em laboratório quando expostos à beta‑amiloide, um pequeno fragmento proteico que se acumula no cérebro de portadores de Alzheimer. Ao acompanhar milhares de células uma a uma, e observando não apenas quais genes estão ativos, mas também como o DNA é organizado, os pesquisadores oferecem um mapa de referência rico que outros cientistas podem usar para investigar mudanças precoces associadas à demência.
Construindo células cerebrais em cultura
Para estudar o desenvolvimento inicial de neurônios de forma controlada, a equipe utilizou células-tronco pluripotentes induzidas humanas, que podem ser direcionadas para se tornarem células progenitoras neurais — o material de partida para muitos tipos celulares do cérebro. Essas progenitoras foram cultivadas em placas e então transferidas para um meio especial que estimula a diferenciação em neurônios mais maduros ao longo de 20 dias. Algumas culturas seguiram esse programa em condições normais, enquanto outras foram expostas desde o início à beta‑amiloide 1–42, o mesmo peptídeo que forma placas na doença de Alzheimer. Células de ambos os grupos foram coletadas em quatro momentos-chave — antes da mudança (dia 0) e durante a transformação (dias 7, 13 e 20) — para capturar, passo a passo, o desdobrar de suas trajetórias de desenvolvimento. 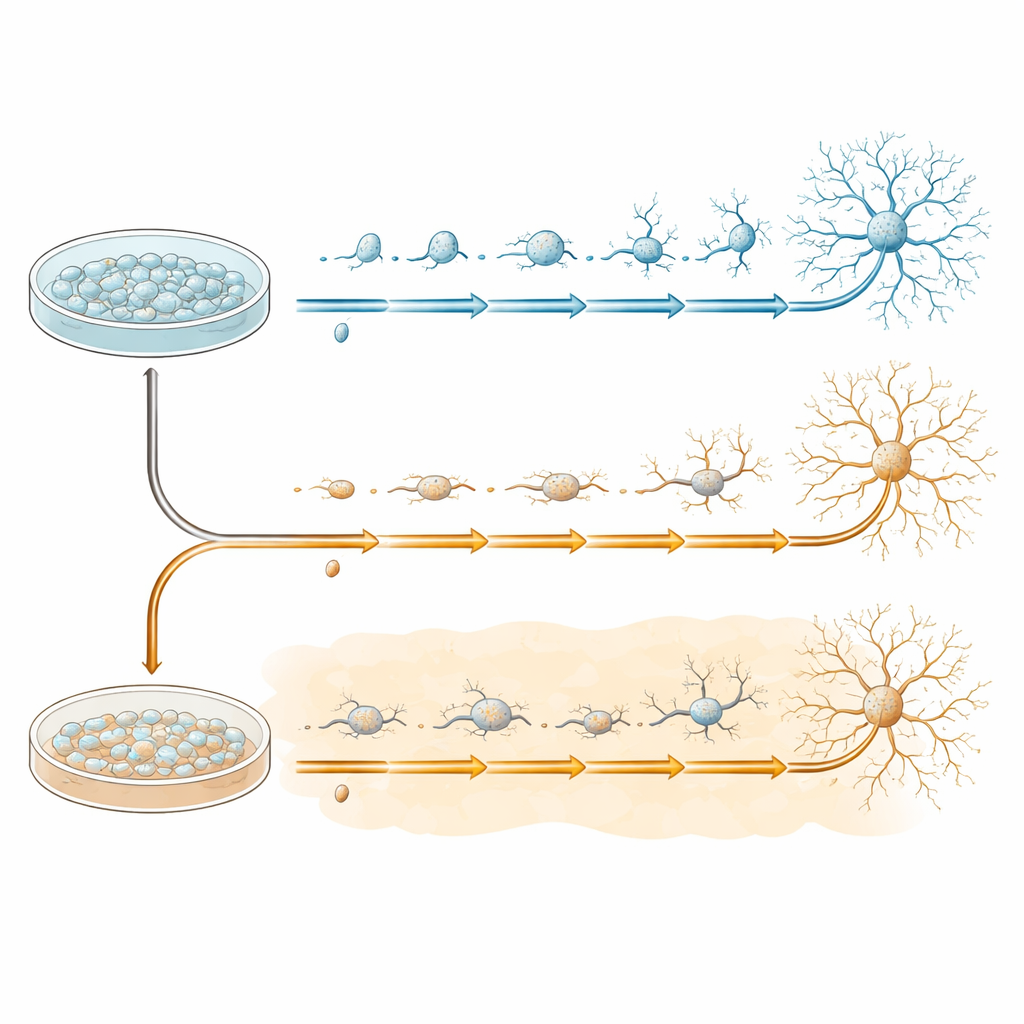
Ouvindo genes e abrindo o genoma
O que destaca este trabalho é que cada célula foi examinada de duas maneiras complementares. Primeiro, os pesquisadores usaram sequenciamento de RNA em célula única para medir quais genes estavam ativados em mais de 42.000 células. Em segundo lugar, aplicaram sequenciamento ATAC em célula única em mais de 30.000 células para identificar quais partes do DNA estavam fisicamente acessíveis, um indicativo de que essas regiões podem funcionar como interruptores de controle gênico. Métodos computacionais sofisticados agruparam as células em clusters, ordenaram‑nas ao longo de “trajetórias” de desenvolvimento desde progenitores até neurônios mais maduros e células com aspecto de astrócitos, e relacionaram padrões de atividade gênica a alterações na cromatina, o complexo DNA‑proteína que acondiciona nossos genes.
Traçando a jornada de células-tronco a neurônios
Dentro das células neuronais em desenvolvimento, a equipe identificou uma série de cinco estágios amplos, rotulados de A a E, que refletem uma transição gradual de células em divisão com características de tronco para neurônios em amadurecimento com ramos complexos. Genes clássicos marcadores de estados neuronais iniciais e tardios variaram de forma ordenada ao longo desse percurso, e uma análise independente de “pseudotempo” confirmou a mesma sequência. Em estágios mais avançados, eles aprofundaram a análise e encontraram sub‑rotas entre células mais maduras, mostrando que algumas seguem trajetórias ligeiramente diferentes ao refinarem sua identidade. Ao longo desses estágios, os cientistas catalogaram genes que mudam em conjunto, genes que respondem de modo distinto na presença da beta‑amiloide e conjuntos de genes que parecem alterados apenas sob exposição à beta‑amiloide.
O que a beta‑amiloide altera — e o que mantém intacto
Embora a estrutura geral das trajetórias de desenvolvimento fosse semelhante com e sem beta‑amiloide, a equipe detectou deslocamentos distintos em quais genes estavam mais ou menos ativos em determinados estágios quando o peptídeo estava presente. Muitos desses genes estão envolvidos na comunicação entre neurônios, no crescimento de axônios e dendritos e em outras funções críticas para circuitos cerebrais saudáveis. Os pesquisadores também combinaram os dados de atividade gênica e cromatina para construir redes que vinculam proteínas de controle chave, chamadas fatores de transcrição, a conjuntos de genes‑alvo. Eles descobriram milhares desses “regulons” e mostraram que alguns se comportam de maneira diferente entre as condições normais e com beta‑amiloide, embora as mudanças em larga escala na acessibilidade do DNA permaneçam modestamente limitadas. 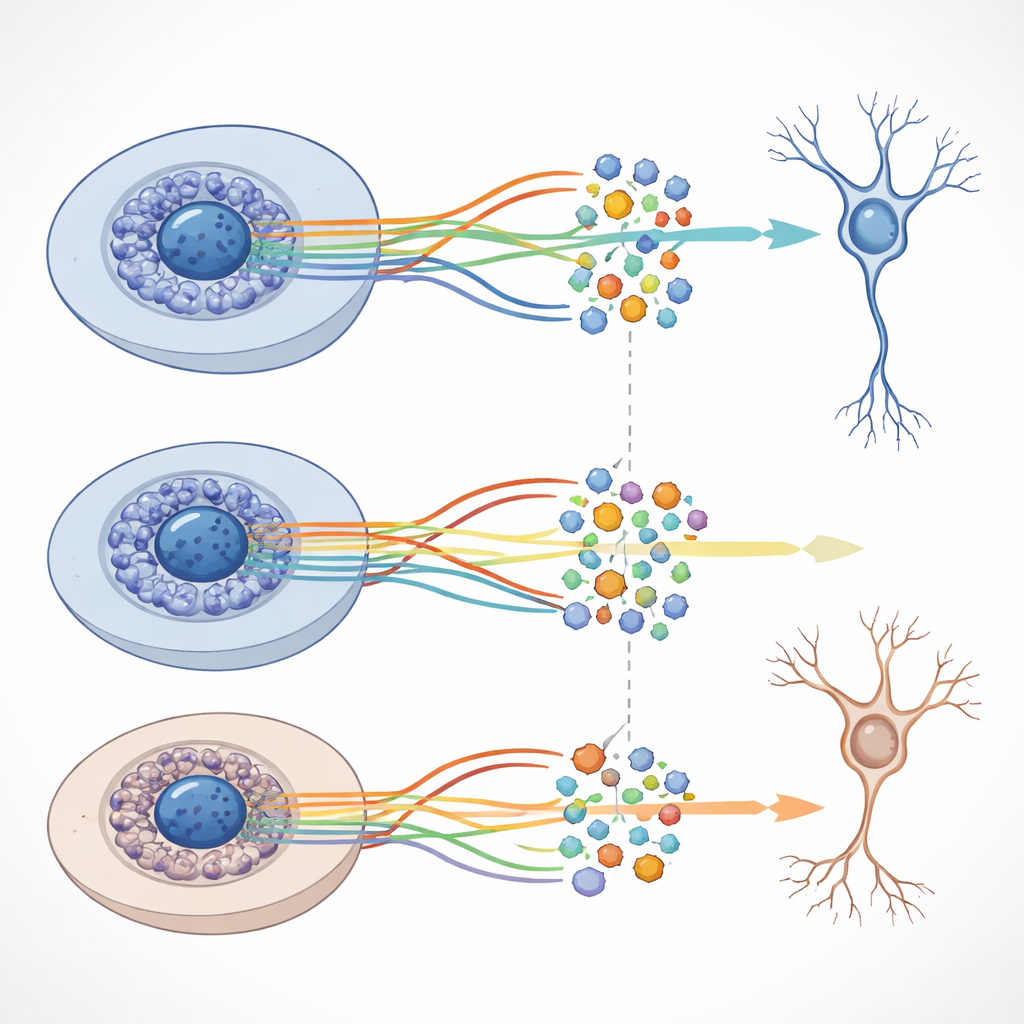
Conectando achados de laboratório ao cérebro de pessoas com Alzheimer
Para avaliar quão relevante é o sistema em cultura para a doença real, os autores compararam suas listas de genes a um conjunto de dados existente de tecido cerebral de pessoas com e sem Alzheimer. Vários dos mesmos genes que diferiram entre células normais e tratadas com beta‑amiloide também diferiam entre cérebros controle e de Alzheimer. Quando trataram grupos de genes específicos de estágios de desenvolvimento como “assinaturas”, essas assinaturas mostraram enriquecimento entre as alterações observadas em amostras de hipocampo de pacientes, especialmente para genes ligados à comunicação e à estrutura neuronal. Isso sugere que o modelo in vitro captura fragmentos significativos da biologia que ocorrem nos centros de memória vulneráveis do cérebro envelhecido.
O que esse recurso oferece para o futuro
O produto principal deste trabalho não é um único resultado de destaque, mas um conjunto de dados público e reutilizável. Todas as informações brutas e processadas, juntamente com o código de análise e um navegador web interativo, estão livremente disponíveis para outros cientistas. Pesquisadores podem usar este mapa para avaliar novas ferramentas computacionais, explorar como diferentes protocolos de laboratório afetam o desenvolvimento neuronal ou testar hipóteses sobre como processos relacionados ao Alzheimer interrompem o nascimento e a maturação de células cerebrais. Em termos simples, o estudo fornece um “diagrama de fiação” detalhado de como células cerebrais humanas jovens crescem — com e sem um importante fator de estresse associado ao Alzheimer — que ajudará a área a dissecar quando e onde as coisas dão errado.
Citação: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Palavras-chave: Doença de Alzheimer, neurogênese, sequenciamento unicelular, beta amiloide, diferenciação neuronal