Clear Sky Science · it
Differenziazione neuronale umana sotto esposizione ad Aβ: un dataset trascrittomico ed epigenomico a singola cellula
Perché questo studio sulle cellule cerebrali è importante
La malattia di Alzheimer sottrae lentamente memoria e capacità di pensiero, ma non comprendiamo ancora pienamente cosa accada alle cellule cerebrali neoformate durante il decorso della malattia. Questo studio crea un “atlante” dettagliato di come i neuroni umani si sviluppano in vitro quando sono esposti all’amiloide‑beta, un piccolo frammento proteico che si accumula nel cervello dei pazienti affetti da Alzheimer. Tracciando migliaia di cellule una per una e osservando non solo quali geni sono attivi ma anche come il DNA è impacchettato, i ricercatori offrono una mappa di riferimento ricca che altri scienziati possono usare per indagare i cambiamenti precoci collegati alla demenza.
Costruire cellule cerebrali in provetta
Per studiare lo sviluppo precoce dei neuroni in modo controllato, il team ha utilizzato cellule staminali pluripotenti indotte umane, che possono essere indirizzate a diventare progenitori neurali—il materiale di partenza per molti tipi di cellule cerebrali. Questi progenitori sono stati coltivati in piatti e poi trasferiti in un mezzo speciale che favorisce la loro trasformazione in neuroni più maturi in 20 giorni. Alcuni piatti hanno seguito questo programma in condizioni normali, mentre altri sono stati esposti fin dall’inizio all’amiloide‑beta 1–42, lo stesso peptide che forma le placche nella malattia di Alzheimer. Le cellule di entrambi i gruppi sono state raccolte in quattro momenti chiave—prima del cambio (giorno 0) e durante la trasformazione (giorni 7, 13 e 20)—per catturare lo svolgersi passo dopo passo dei loro percorsi di sviluppo. 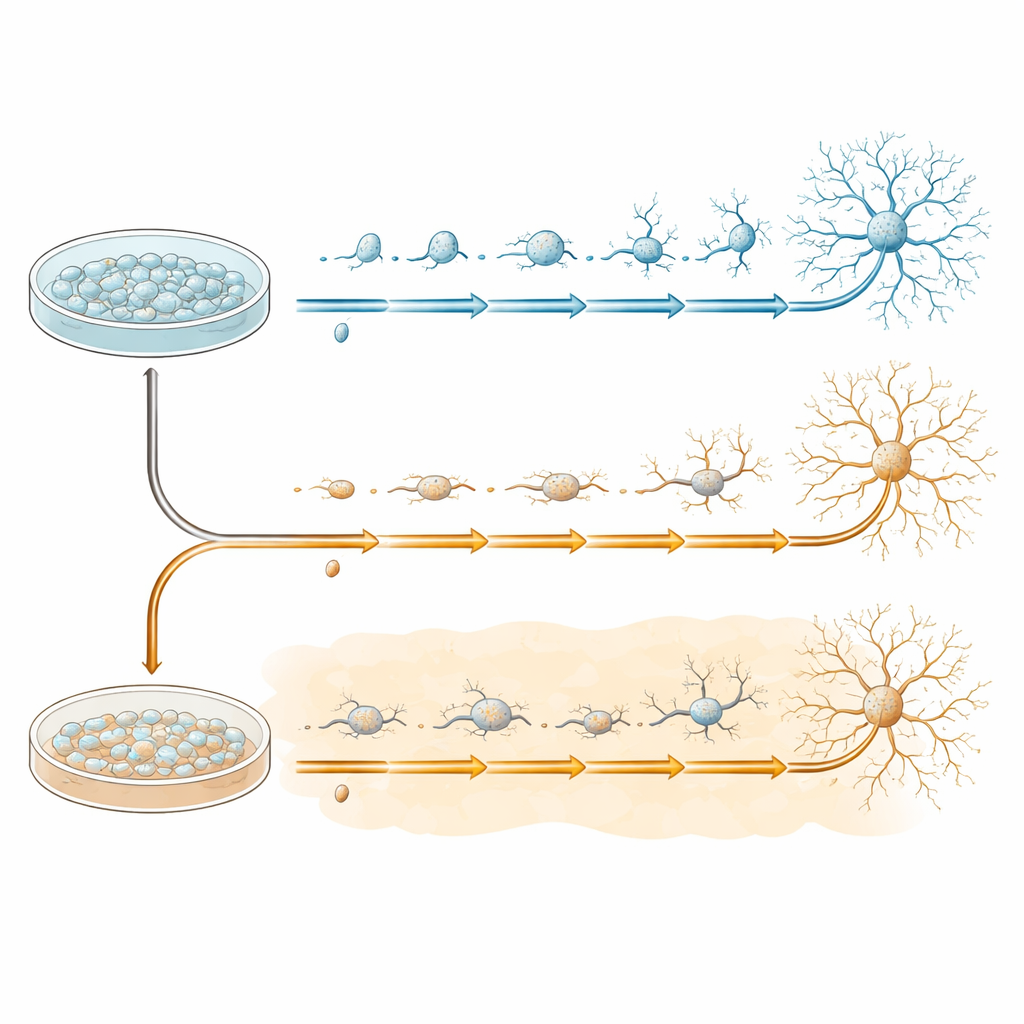
Ascoltare i geni e aprire il genoma
Ciò che distingue questo lavoro è che ogni cellula è stata esaminata in due modi complementari. Innanzitutto, i ricercatori hanno usato il sequenziamento RNA a singola cellula per misurare quali geni erano attivi in oltre 42.000 cellule. In secondo luogo, hanno impiegato il sequenziamento ATAC a singola cellula in più di 30.000 cellule per vedere quali parti del DNA erano fisicamente accessibili, segno che quelle regioni possono fungere da interruttori per il controllo genico. Metodi computazionali sofisticati hanno raggruppato le cellule in cluster, ordinate lungo “traiettorie” di sviluppo dai progenitori verso neuroni più maturi e cellule con caratteristiche astrocitarie, e hanno collegato i modelli di attività genica ai cambiamenti nella cromatina, il materiale DNA‑proteina che impacchetta i nostri geni.
Tracciare il percorso dalle staminali ai neuroni
All’interno delle cellule neuronali in sviluppo, il team ha identificato una serie di cinque stadi ampi, etichettati da A a E, che riflettono uno spostamento graduale da cellule simili a staminali in divisione verso neuroni maturi con rami complessi. I geni marker classici per stati neuronali precoci e tardivi cambiavano in modo ordinato lungo questo percorso, e un’analisi indipendente di “pseudotime” ha confermato la stessa sequenza. Negli stadi più avanzati, hanno esaminato più in dettaglio e trovato sotto‑percorsi tra le cellule più mature, mostrando che alcune cellule seguono rotte leggermente diverse mentre affinano la loro identità. Attraverso questi passaggi, gli scienziati hanno catalogato geni che cambiano insieme, geni che rispondono in modo differente quando è presente l’amiloide‑beta, e insiemi di geni che sembrano alterati solo sotto esposizione ad amiloide‑beta.
Cosa cambia con l’amiloide‑beta—e cosa resta intatto
Benché la struttura complessiva dei percorsi di sviluppo fosse simile con e senza amiloide‑beta, il team ha rilevato spostamenti distinti nell’attività di specifici geni in particolari stadi quando il peptide era presente. Molti di questi geni sono coinvolti nella comunicazione neuronale, nella crescita di assoni e dendriti e in altre funzioni critiche per circuiti cerebrali sani. I ricercatori hanno anche combinato i dati sull’attività genica e sulla cromatina per costruire reti che collegano proteine di controllo chiave, chiamate fattori di trascrizione, a gruppi di geni bersaglio. Hanno scoperto migliaia di tali “regulon” e dimostrato che alcuni di essi si comportano in modo diverso tra le condizioni normali e quelle con amiloide‑beta, anche se i cambiamenti su larga scala nell’accessibilità del DNA rimangono modesti. 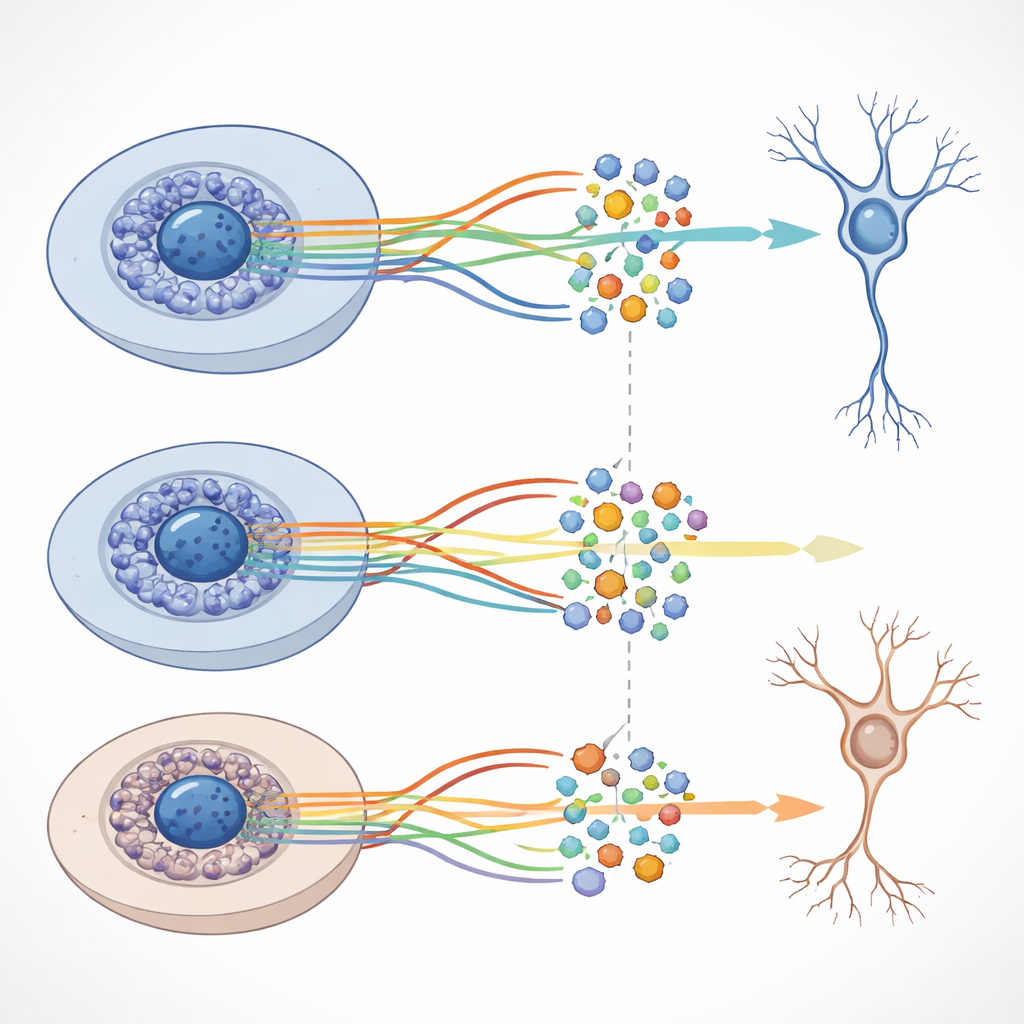
Collegare i risultati di laboratorio ai cervelli umani con Alzheimer
Per valutare quanto sia rilevante il loro sistema in coltura rispetto alla malattia reale, gli autori hanno confrontato le loro liste di geni con un dataset esistente di tessuto cerebrale di persone con e senza Alzheimer. Diversi degli stessi geni che differivano tra cellule normali e trattate con amiloide‑beta differivano anche tra cervelli di controllo e cervelli con Alzheimer. Quando hanno trattato gruppi di geni specifici per stadio di sviluppo come “firme”, queste firme risultavano arricchite tra i cambiamenti osservati nei campioni di ippocampo dei pazienti, in particolare per i geni legati alla comunicazione e alla struttura neuronale. Questo suggerisce che il modello in vitro cattura elementi significativi della biologia che si verificano nei centri della memoria vulnerabili nel cervello che invecchia.
Cosa offre questa risorsa per il futuro
Il prodotto principale di questo lavoro non è un singolo risultato clou, ma un dataset pubblico e riutilizzabile. Tutte le informazioni grezze e processate, insieme al codice di analisi e a un browser web interattivo, sono liberamente disponibili per altri ricercatori. Gli scienziati possono usare questa mappa per valutare nuovi strumenti computazionali, esplorare come diversi protocolli di laboratorio influenzano lo sviluppo neuronale o testare nuove ipotesi su come i processi legati all’Alzheimer interrompano la nascita e la maturazione delle cellule cerebrali. In termini semplici, lo studio fornisce un “diagramma dei collegamenti” dettagliato di come crescono le giovani cellule cerebrali umane—con e senza un importante fattore di stress associato all’Alzheimer—che aiuterà il campo a capire quando e dove le cose cominciano ad andare storte.
Citazione: Blanco-Luquin, I., Martínez-de-Morentin, X., Vilas-Zornoza, A. et al. Human neuronal differentiation under Aβ exposure: a single-cell transcriptomic and epigenomic dataset. Sci Data 13, 638 (2026). https://doi.org/10.1038/s41597-026-06971-4
Parole chiave: Malattia di Alzheimer, neurogenesi, sequenziamento a singola cellula, amiloide beta, differenziazione neuronale