Clear Sky Science · zh
关于 IscB 基于 RNA 盖板的失活机制的结构洞见
带有内置安全锁的小型基因剪刀
像 CRISPR–Cas9 这样的基因编辑工具已改变了生物学领域,但它们体积庞大,难以安全地传递到人类组织中。该研究考察了 IscB——一种比 Cas9 小得多的近缘蛋白——以理解它如何在遇到完全匹配的 DNA 序列之前保持安全关闭。通过在近原子分辨率下观察 IscB 的微小活动部件,作者揭示了它如何防止误切以及如何调整其性能以适应未来的医疗应用。 
CRISPR 主力的微小祖先
IscB 来源于古老的移动遗传元件,被认为是 Cas9 的进化祖先。像 Cas9 一样,IscB 使用 RNA 向导定位匹配的 DNA 并切割它,但其体积不到实验室常用 Cas9 的一半。这样的紧凑性对于依赖病毒载体的治疗很有吸引力,因为载体对载货量有严格限制。然而直到现在,研究者只见过 IscB 与 DNA 结合时的单一快照。关键缺失之处在于蛋白处于闲置状态时的构型、它如何检测潜在靶点,以及它如何从无害的旁观者转变为活跃的切割酶。
捕捉蛋白质的运作过程
为补全这一图景,团队设计了一种略作修饰、更加稳定的 IscB,并使用冷冻电子显微镜进行了观察。他们捕获了四个不同状态:无 DNA 的静息形态、两个中间态(RNA 向导分别与 6 或 10 个 DNA 核苷酸配对)以及一个已就绪的状态(配对了 16 个核苷酸,DNA 准备被切割)。这些高分辨率图像描绘了从完全关闭到完全开启的连续通路。它们显示 IscB 的两个切割中心异常靠近,且由短“铰链”相连而不是长而松弛的连接区,这有助于解释如此小的蛋白如何执行复杂任务。
RNA 盖板与分子“油门踏板”
结构显示 IscB 使用其自身 RNA 形成一个优雅的双重锁系统。RNA 的一部分像盖子一样覆盖第一个切割中心,而另一部分横跨第二个切割中心,阻挡外来 DNA 链的接近。随着 RNA 向导逐步与正确的 DNA 靶点配对,它并非一次性移动;相反,它分阶段位移,类似于慢慢踩下的汽车油门踏板。当大约 11 个匹配字母配对时,这一运动最终将 RNA 盖板推开并重塑一个称为 HNH 结构域的关键区域,该结构域大约旋转 90 度进入活性位置。这个阈值有助于确保 IscB 仅对高度匹配的序列做出反应,从而限制脱靶切割。 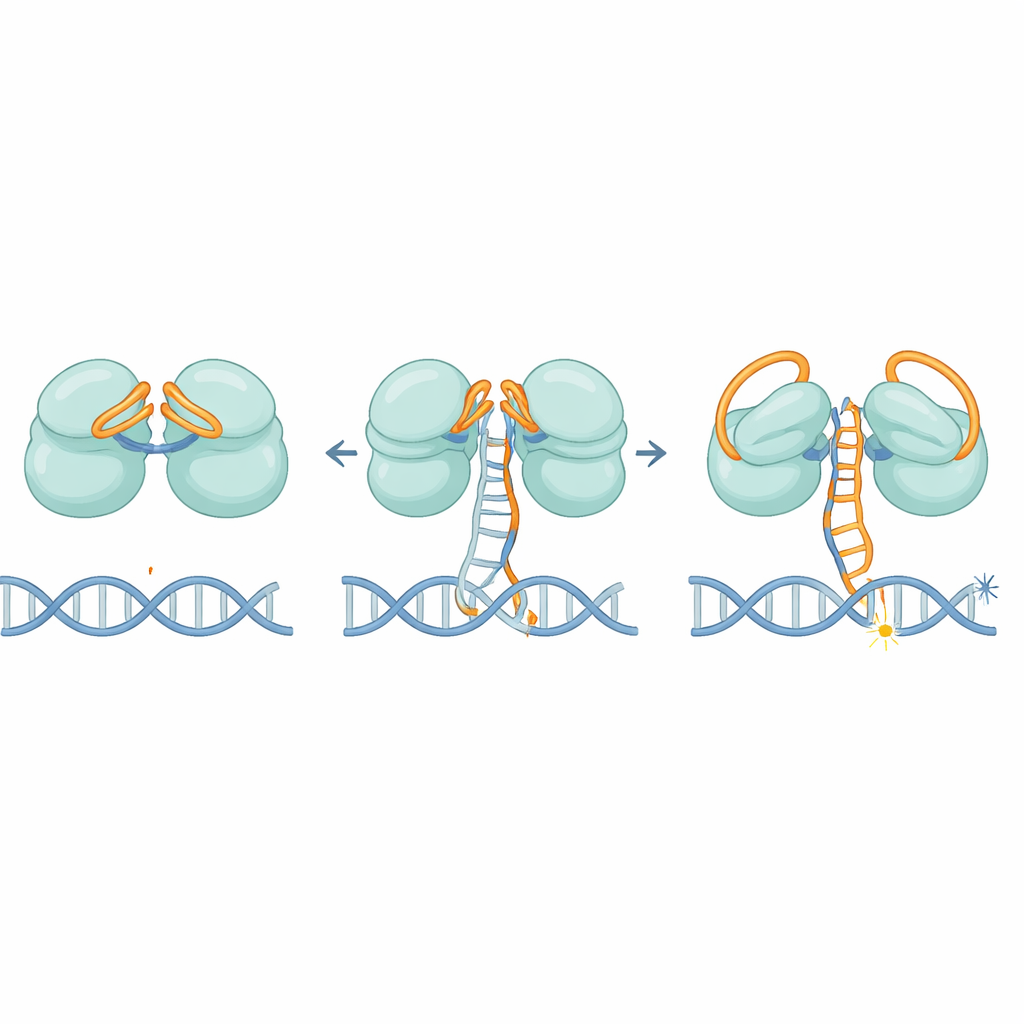
IscB 如何撬开 DNA 并将其固定
一旦被激活,IscB 必须将 DNA 双螺旋的两条链分开并保持足够的时间以完成切割。作者鉴定出蛋白上的一个小环突入 DNA,使链在 RNA 与 DNA 形成杂交区域处分开。沿着铰链的带正电荷的斑块随后抓住被挤出的链,稳定这种气泡状的“R 环”。削弱该楔子或带电带的突变会显著降低切割活性,证实它们对打开并固定 DNA 至关重要。
调节铰链以打造更好的编辑器
由于铰链控制 HNH 结构域进入活性位的难易程度,研究人员测试了在该处进行微妙改变是否能提升性能。通过用更小、更灵活的氨基酸替换某些体积较大的残基,他们创造了铰链活动性更大的 IscB 变体。在人类细胞中,这些工程化版本中的两个(命名为 Hig1 和 Hig2)表现出明显更高的编辑活性。其中一个变体的效率接近先进 Cas9 工具,同时在全基因组范围内引发的非预期断裂更少,这表明适度放松这些铰链可以使 IscB 更强大且更精确。
这对未来基因治疗的意义
综上,这些发现展示了一个紧凑的基因编辑酶如何在遇到近乎完美的 DNA 匹配之前保持安全锁定,然后迅速重排自身以在正确位点切割。通过绘制从保护切割中心的 RNA 盖板到触发激活的油门踏板式运动再到决定最终切割的铰链的每一步,该研究为设计更小、更安全的基因组编辑器提供了蓝图。此类工具更易于包装进医疗递送系统,最终可能实现更精确、并发症更少的治疗方案。
引用: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
关键词: IscB, 基因组编辑, CRISPR, RNA 引导核酸酶, 结构生物学