Clear Sky Science · fr
Compréhension structurelle du mécanisme d’inactivation d’IscB basé sur un capuchon d’ARN
Des ciseaux génétiques plus petits avec un verrou de sécurité intégré
Les outils d’édition génomique comme CRISPR–Cas9 ont transformé la biologie, mais leur grande taille complique leur administration sûre dans les tissus humains. Cette étude examine IscB, un cousin beaucoup plus petit de Cas9, pour comprendre comment il reste désactivé en toute sécurité jusqu’à ce qu’il rencontre exactement la bonne séquence d’ADN. En observant les très petits éléments mobiles d’IscB à une résolution quasi atomique, les auteurs révèlent comment il se protège contre les coupures errantes et comment ses performances peuvent être modulées pour de futures applications médicales. 
Un minuscule ancêtre du cheval de bataille de CRISPR
IscB provient d’éléments génétiques mobiles anciens et est considéré comme un ancêtre évolutif de Cas9. Comme Cas9, il utilise un guide ARN pour cibler un ADN complémentaire puis le cliver, mais il fait moins de la moitié de la taille du Cas9 standard utilisé en laboratoire. Cette compacité est attrayante pour les thérapies reposant sur des vecteurs viraux, qui imposent des limites strictes de charge. Jusqu’à présent, toutefois, les chercheurs n’avaient observé qu’un seul instantané d’IscB lié à l’ADN. Les pièces manquantes clés étaient l’apparence de la protéine à l’état inactif, la manière dont elle teste des cibles potentielles et la façon dont elle passe d’un état inoffensif à un état actif coupeur.
Saisir la protéine en action
Pour compléter ce tableau, l’équipe a conçu une version légèrement modifiée et plus stable d’IscB et l’a examinée par cryo‑microscopie électronique. Ils ont capturé quatre états distincts : une forme au repos sans ADN, deux intermédiaires où le guide ARN s’apparie avec seulement 6 ou 10 bases d’ADN, et un état amorcé où 16 bases sont appariées et l’ADN est prêt à être clivé. Ces images à haute résolution tracent une voie continue du totalement éteint au totalement activé. Elles montrent que les deux centres de coupure d’IscB sont exceptionnellement rapprochés et reliés par de courts « charnières » plutôt que par de longs linkers souples, ce qui aide à expliquer comment une si petite protéine peut réaliser une tâche complexe.
Capuchons d’ARN et une pédale moléculaire
Les structures révèlent qu’IscB utilise un élégant système à double verrou constitué de son propre ARN. Une partie de l’ARN se replie au‑dessus du premier centre de coupure comme un capuchon, tandis qu’une autre section se courbe au‑dessus du second, bloquant l’accès aux brins d’ADN errants. Au fur et à mesure que le guide ARN s’apparie progressivement avec une cible ADN correcte, il ne se déplace pas d’un seul coup ; il se déplace plutôt par étapes, comme une pédale de voiture que l’on enfonce lentement. Lorsqu’environ 11 bases appariées sont atteintes, ce mouvement écarte finalement les capuchons d’ARN et remodele une région clé appelée domaine HNH, qui bascule d’environ 90 degrés en position active. Ce seuil aide à garantir qu’IscB ne répond qu’aux séquences fortement complémentaires, limitant ainsi les coupes hors cible. 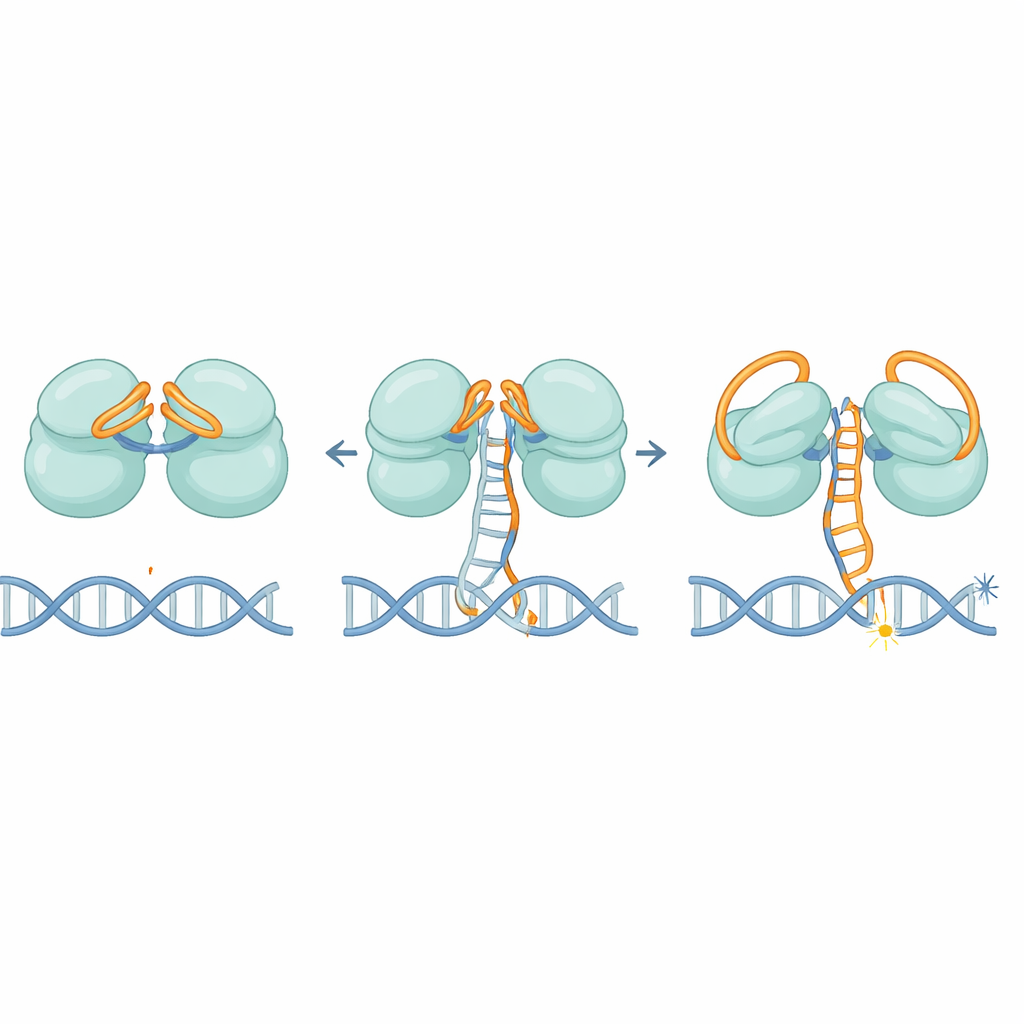
Comment IscB écarte l’ADN et le maintient en place
Une fois activé, IscB doit séparer les deux brins de la double hélice d’ADN et les maintenir écartés suffisamment longtemps pour couper. Les auteurs identifient une petite boucle sur la protéine qui s’intercale dans l’ADN, forçant les brins à se séparer dans la région où l’ARN et l’ADN forment un hybride. Des zones chargées positivement le long des charnières saisissent ensuite le brin déplacé, stabilisant cette bulle en forme de « R-loop ». Des mutations affaiblissant cette cale ou la bande chargée réduisent fortement l’activité de clivage de l’ADN, confirmant qu’elles sont essentielles tant pour l’ouverture que pour le maintien de l’ADN en place.
Ajuster les charnières pour concevoir de meilleurs éditeurs
Parce que les charnières contrôlent la facilité avec laquelle le domaine HNH peut basculer en action, les chercheurs ont testé si des modifications subtiles pouvaient améliorer les performances. En remplaçant certains acides aminés volumineux par des résidus plus petits et plus flexibles, ils ont créé des variantes d’IscB dont les charnières bougent plus librement. Dans des cellules humaines, deux de ces versions conçues, nommées Hig1 et Hig2, ont montré une activité d’édition sensiblement plus élevée. Une variante a atteint une efficacité proche de celle d’un outil Cas9 avancé tout en provoquant moins de coupures involontaires à travers le génome, suggérant que l’assouplissement contrôlé de ces charnières peut rendre IscB à la fois plus puissant et plus précis.
Pourquoi cela compte pour les thérapies géniques futures
Dans l’ensemble, ces résultats montrent comment une enzyme d’édition du génome compacte peut rester verrouillée en toute sécurité jusqu’à ce qu’elle rencontre une correspondance ADN presque parfaite, puis se réarranger rapidement pour couper au bon endroit. En cartographiant chaque étape — des capuchons d’ARN qui protègent les centres de coupure à la motion en pédale qui déclenche l’activation et les charnières qui orientent la coupe finale — ce travail offre une feuille de route pour concevoir des éditeurs du génome plus petits et plus sûrs. De tels outils pourraient être plus faciles à conditionner dans des systèmes de distribution médicaux et pourraient finalement permettre des traitements plus précis avec moins d’effets secondaires.
Citation: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Mots-clés: IscB, édition du génome, CRISPR, nucléase guidée par ARN, biologie structurale