Clear Sky Science · pl
Wgląd strukturalny w mechanizm inaktywacji IscB opartej na „zasuwce” RNA
Mniejsze nożyce genowe z wbudowanym blokadą bezpieczeństwa
Narzędzia do edycji genów, takie jak CRISPR–Cas9, zrewolucjonizowały biologię, ale ich duże rozmiary utrudniają bezpieczne dostarczenie do tkanek ludzkich. W tej pracy badany jest IscB, znacznie mniejszy krewny Cas9, aby zrozumieć, jak pozostaje wyłączony aż do chwili napotkania dokładnie odpowiedniej sekwencji DNA. Obserwując drobne ruchome elementy IscB z niemal atomową rozdzielczością, autorzy ujawniają, jak zapobiega przypadkowym przecięciom oraz jak można dostroić jego działanie dla przyszłych zastosowań medycznych. 
Maleńki przodek konia roboczego CRISPR
IscB pochodzi ze starożytnych elementów genetycznych mobilnych i uważa się go za ewolucyjnego przodka Cas9. Podobnie jak Cas9, używa przewodnika RNA do odnalezienia dopasowanego DNA i następnie jego przecięcia, ale jest mniej niż w połowie wielkości standardowego Cas9 stosowanego w laboratoriach. Ta kompaktowość jest atrakcyjna dla terapii opartych na wektorach wirusowych, które mają rygorystyczne limity ładunku. Do tej pory badacze mieli jednak tylko jeden obraz IscB związany z DNA. Brakowało kluczowych elementów: jak wygląda białko, gdy jest w spoczynku, jak testuje potencjalne cele i jak przechodzi z neutralnego obserwatora w aktywny nożyk.
Uchwycenie białka in flagranti
Aby uzupełnić ten obraz, zespół zaprojektował nieco zmodyfikowaną, bardziej stabilną wersję IscB i zbadał ją za pomocą krioelektronowej mikroskopii. Ujęto cztery odrębne stany: formę spoczynkową bez DNA, dwa pośrednie, w których przewodnik RNA łączy się tylko z 6 lub 10 zasadami DNA, oraz stan przygotowany, w którym sparowanych jest 16 zasad i DNA jest gotowe do przecięcia. Te obrazy o wysokiej rozdzielczości odwzorowują ciągłą ścieżkę od całkowitego wyłączenia do pełnej aktywacji. Pokazują, że dwa centry przecinające IscB są umieszczone wyjątkowo blisko siebie i połączone krótkimi „zawiasami” zamiast długich, wiotkich łączników, co pomaga wyjaśnić, jak tak małe białko może wykonać złożone zadanie.
RNA-„zasuwy” i molekularny pedał samochodowy
Struktury ujawniają, że IscB wykorzystuje elegancki podwójny zamek zbudowany z własnego RNA. Jedna część RNA składa się nad pierwszym centrum przecinającym jak pokrywka, podczas gdy inny fragment wygina się nad drugim, blokując dostęp obcym niciom DNA. W miarę jak przewodnik RNA stopniowo łączy się z prawidłowym celem DNA, nie przesuwa się on jednocześnie; zamiast tego porusza się etapami, jakby powoli naciskany pedał samochodu. Gdy sparowanych jest około 11 pasujących zasad, ten ruch w końcu wypycha RNA-„zasuwy” na bok i przekształca kluczowy obszar zwany domeną HNH, która obraca się o mniej więcej 90 stopni do pozycji aktywnej. Ten próg pomaga zapewnić, że IscB reaguje tylko na silnie dopasowane sekwencje, ograniczając cięcia poza celem. 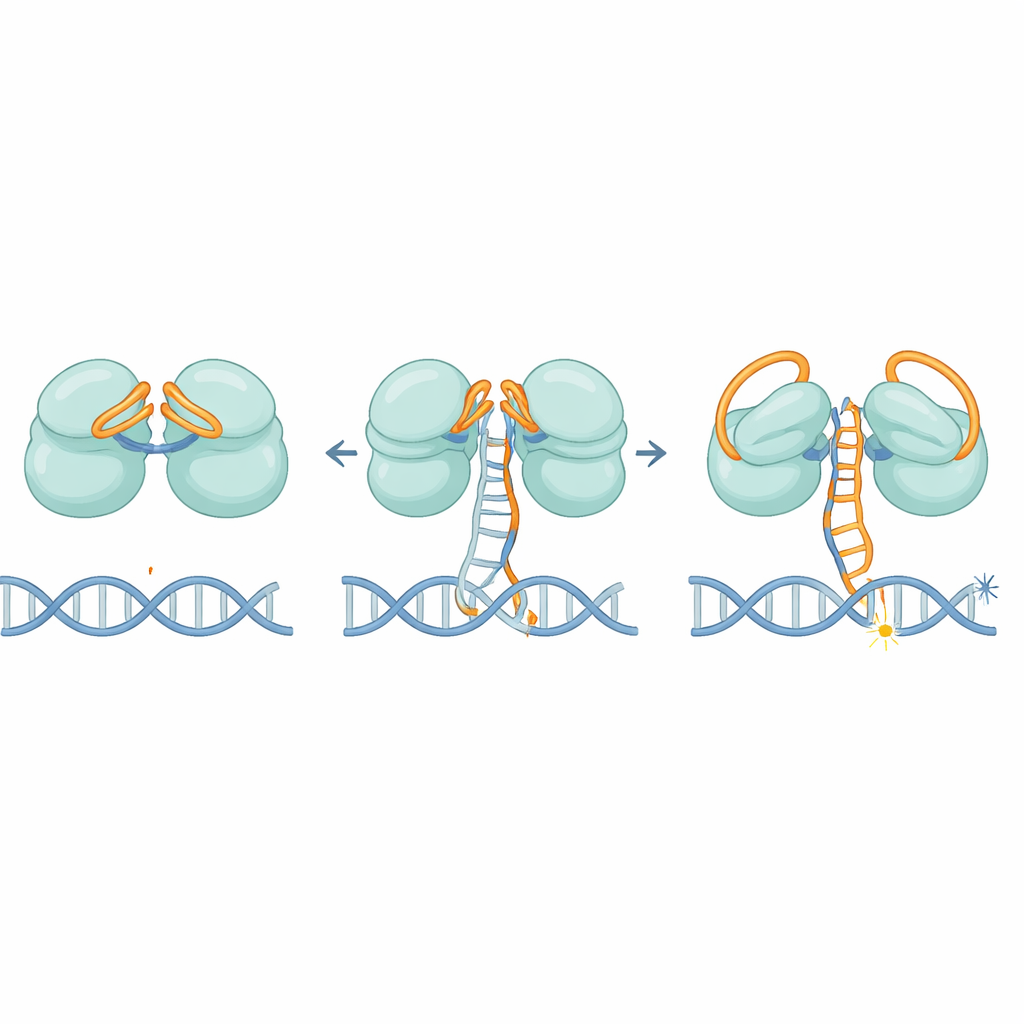
Jak IscB rozdziela DNA i utrzymuje je w pozycji
Gdy zostanie aktywowany, IscB musi rozdzielić dwie nici podwójnej helisy DNA i utrzymać je oddzielone wystarczająco długo, by przeciąć. Autorzy identyfikują małą pętlę w białku, która klinuje się w DNA, zmuszając nici do rozdzielenia w obszarze, gdzie RNA i DNA tworzą hybrydę. Dodatnio naładowane miejsca wzdłuż zawiasów następnie chwytają zdeplasowaną nić, stabilizując tę bańkową „pętlę R”. Mutacje osłabiające ten klin lub pas naładowanych reszt ostro zmniejszają aktywność cięcia DNA, potwierdzając, że są niezbędne zarówno do otwarcia, jak i utrzymania DNA w miejscu.
Dostrajanie zawiasów, by zbudować lepsze edytory
Ponieważ zawiasy kontrolują, jak łatwo domena HNH może wejść w akcję, badacze sprawdzili, czy subtelne zmiany tam mogą zwiększyć wydajność. Poprzez zastąpienie niektórych dużych aminokwasów mniejszymi, bardziej elastycznymi, stworzyli warianty IscB, których zawiasy poruszają się swobodniej. W komórkach ludzkich dwa z tych zmodyfikowanych wariantów, nazwane Hig1 i Hig2, wykazały wyraźnie wyższą aktywność edycyjną. Jeden wariant zbliżył się do wydajności zaawansowanego narzędzia Cas9, powodując jednocześnie mniej niezamierzonych pęknięć DNA w całym genomie, co sugeruje, że ostrożne poluzowanie tych zawiasów może uczynić IscB zarówno silniejszym, jak i bardziej precyzyjnym.
Dlaczego to ma znaczenie dla przyszłych terapii genowych
Razem te odkrycia pokazują, jak kompaktowa enzymatyczna maszyna do edycji genów może pozostać bezpiecznie zablokowana, dopóki nie napotka niemal idealnego dopasowania DNA, a następnie szybko przeorganizować się, by przeciąć we właściwym miejscu. Mapując każdy etap — od RNA-„zasuw” osłaniających centra przecinające, przez ruch przypominający pedał samochodowy uruchamiający aktywację, po zawiasy kierujące końcowym cięciem — praca oferuje plan działania dla projektowania mniejszych, bezpieczniejszych edytorów genomu. Takie narzędzia mogą być łatwiejsze do zapakowania w systemy dostarczania medycznego i ostatecznie umożliwić bardziej precyzyjne terapie z mniejszą liczbą skutków ubocznych.
Cytowanie: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Słowa kluczowe: IscB, edytowanie genomu, CRISPR, nukleaza kierowana przez RNA, biologia strukturalna