Clear Sky Science · pt
Insight estrutural sobre o mecanismo de inativação baseado em tampa de RNA do IscB
Tesouras gênicas menores com um cadeado de segurança embutido
Ferramentas de edição genética como o CRISPR–Cas9 transformaram a biologia, mas seu grande tamanho dificulta a entrega segura em tecidos humanos. Este estudo explora o IscB, um primo muito menor do Cas9, para entender como ele permanece desativado até encontrar exatamente a sequência de DNA correta. Ao observar as pequenas peças móveis do IscB em detalhes quase atômicos, os autores revelam como ele se protege contra cortes indesejados e como seu desempenho pode ser ajustado para aplicações médicas futuras. 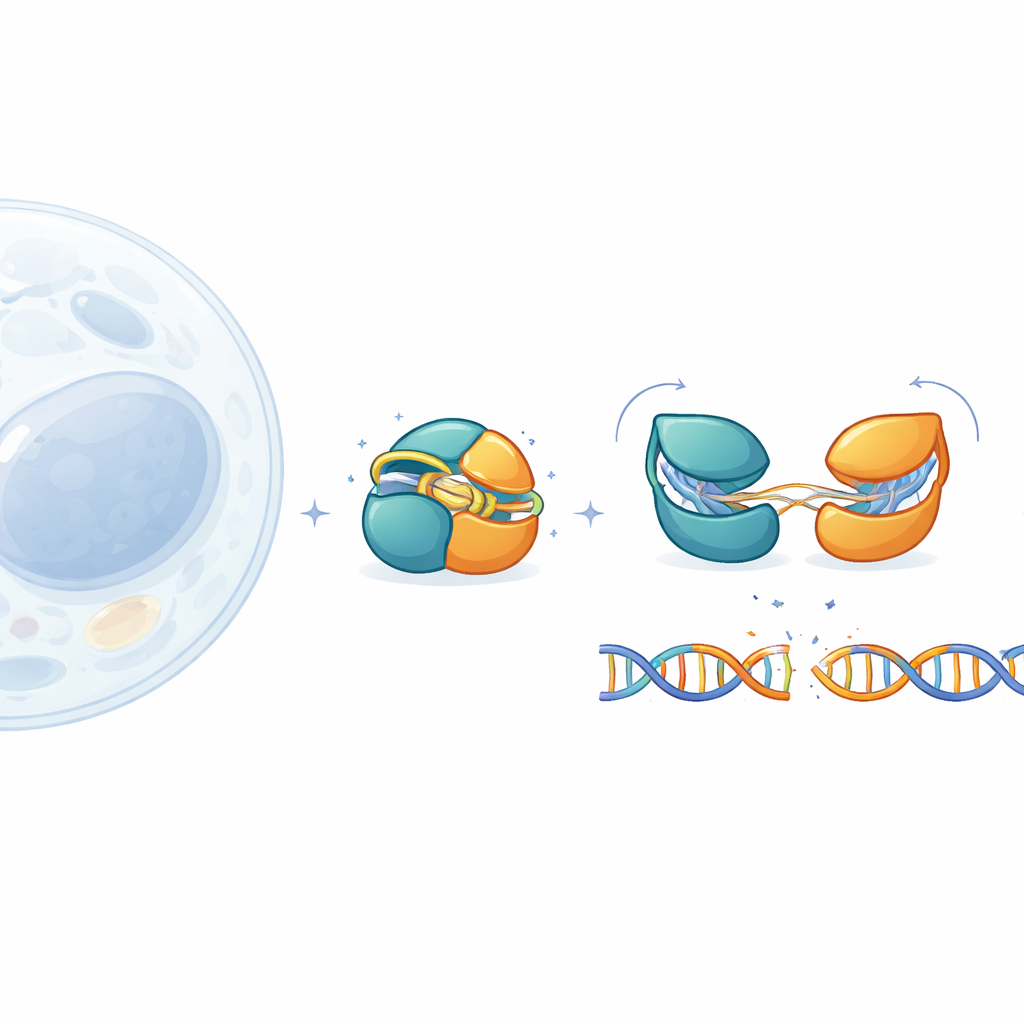
Um pequeno ancestral do cavalo de batalha do CRISPR
O IscB provém de elementos genéticos móveis ancestrais e é considerado um ancestral evolutivo do Cas9. Como o Cas9, ele usa um RNA guia para localizar DNA correspondente e então cortá-lo, mas tem menos da metade do tamanho do Cas9 padrão usado em laboratórios. Essa compacidade é atraente para terapias que dependem de vetores virais, os quais têm limites rígidos de carga. Até agora, entretanto, os pesquisadores tinham observado apenas um instantâneo do IscB ligado ao DNA. As peças-chave que faltavam eram como a proteína se apresenta quando está inativa, como ela testa alvos potenciais e como ela passa de um observador inofensivo para um cortador ativo.
Capturando a proteína em ação
Para completar esse quadro, a equipe projetou uma versão ligeiramente modificada e mais estável do IscB e a examinou usando crio–microscopia eletrônica. Eles capturaram quatro estados distintos: uma forma de repouso sem DNA, dois intermediários onde o RNA guia pareia com apenas 6 ou 10 letras do DNA, e um estado preparado em que 16 letras estão pareadas e o DNA está pronto para ser cortado. Essas imagens de alta resolução traçam um caminho contínuo do totalmente desligado ao totalmente ligado. Elas mostram que os dois centros de corte do IscB estão empacotados de forma incomum e conectados por "dobradiças" curtas em vez de longos elos frouxos, ajudando a explicar como uma proteína tão pequena pode realizar uma tarefa complexa.
Tampas de RNA e um pedal molecular de carro
As estruturas revelam que o IscB usa um elegante sistema de trava dupla feito de seu próprio RNA. Uma parte do RNA dobra-se sobre o primeiro centro de corte como uma tampa, enquanto outra seção se curva sobre o segundo, bloqueando o acesso a fitas de DNA errantes. À medida que o RNA guia pareia gradualmente com um alvo de DNA correto, ele não se move de uma só vez; em vez disso, desloca-se em etapas, como um pedal de carro sendo pressionado lentamente. Quando cerca de 11 letras correspondentes estão pareadas, esse movimento finalmente empurra as tampas de RNA para fora do caminho e remodela uma região chave chamada domínio HNH, que gira cerca de 90 graus para uma posição ativa. Esse limiar ajuda a garantir que o IscB responda apenas a sequências fortemente correlacionadas, limitando cortes fora do alvo. 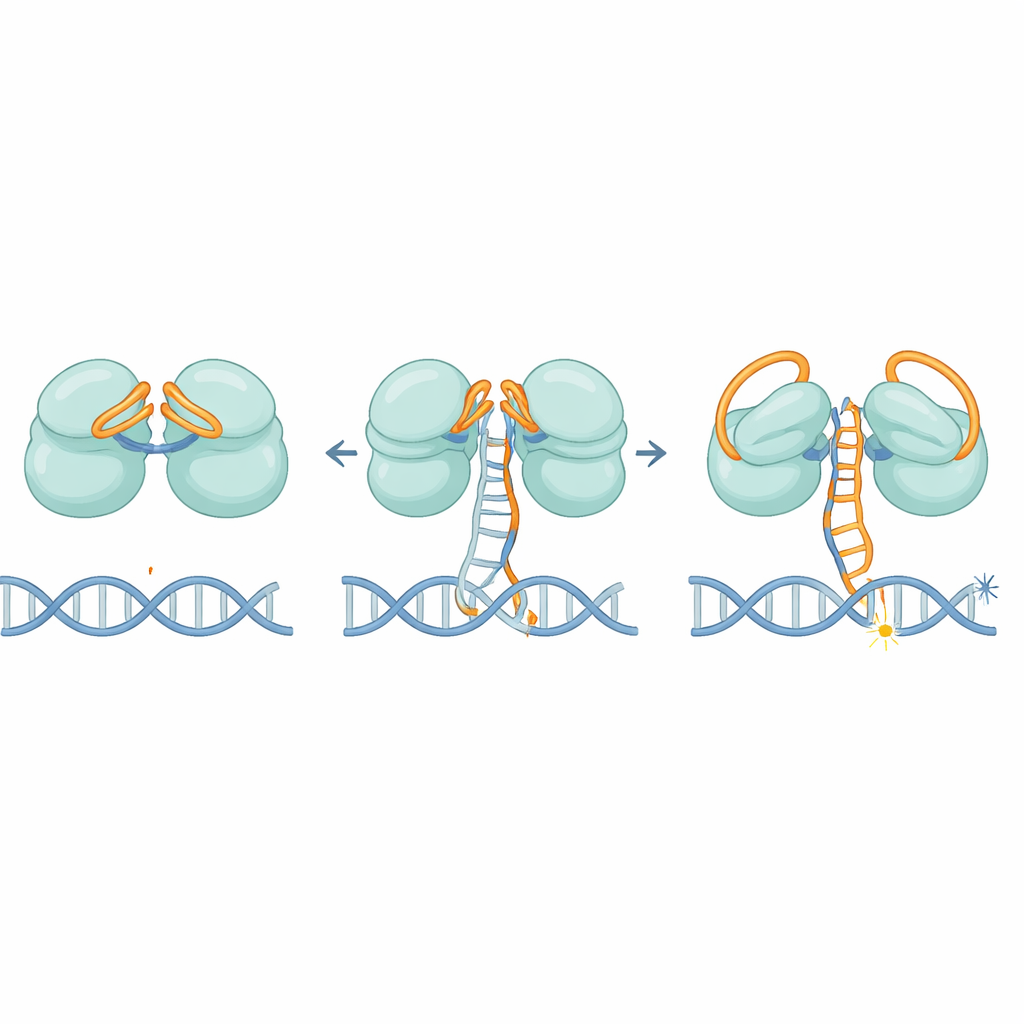
Como o IscB abre o DNA e o mantém estável
Uma vez ativado, o IscB deve separar as duas fitas da dupla hélice do DNA e mantê-las afastadas tempo suficiente para cortar. Os autores identificam um pequeno loop na proteína que se insere no DNA, forçando as fitas a se separarem na região onde o RNA e o DNA formam uma estrutura híbrida. Manchas carregadas positivamente ao longo das dobradiças então prendem a fita deslocada, estabilizando essa bolha tipo "R-loop". Mutações que enfraquecem essa cunha ou a faixa carregada reduzem drasticamente a atividade de corte do DNA, confirmando que são essenciais tanto para abrir quanto para manter o DNA no lugar.
Ajustando as dobradiças para criar editores melhores
Como as dobradiças controlam com que facilidade o domínio HNH pode girar para a ação, os pesquisadores testaram se mudanças sutis ali poderiam melhorar o desempenho. Ao substituir certos aminoácidos volumosos por outros menores e mais flexíveis, eles criaram variantes do IscB cujas dobradiças se movem com mais liberdade. Em células humanas, duas dessas versões engenheiradas, apelidadas Hig1 e Hig2, mostraram atividade de edição visivelmente maior. Uma variante aproximou-se da eficiência de uma ferramenta Cas9 avançada enquanto causava menos quebras de DNA não intencionais pelo genoma, sugerindo que afrouxar cuidadosamente essas dobradiças pode tornar o IscB tanto mais potente quanto mais preciso.
Por que isso importa para terapias gênicas futuras
Em conjunto, esses achados mostram como uma enzima de edição genômica compacta pode permanecer seguramente trancada até encontrar uma correspondência de DNA quase perfeita, então se reorganizar rapidamente para cortar no local certo. Ao mapear cada etapa — das tampas de RNA que protegem os centros de corte ao movimento tipo pedal de carro que aciona a ativação e às dobradiças que orientam o corte final — o trabalho oferece um roteiro para projetar editores genômicos menores e mais seguros. Tais ferramentas podem ser mais fáceis de embalar em sistemas de entrega médica e, em última instância, possibilitar tratamentos mais precisos com menos efeitos colaterais.
Citação: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Palavras-chave: IscB, edição genômica, CRISPR, nuclease guiada por RNA, biologia estrutural