Clear Sky Science · es
Visión estructural del mecanismo de inactivación basado en una "tapa" de ARN de IscB
Tijeras genéticas más pequeñas con un seguro integrado
Herramientas de edición genética como CRISPR–Cas9 han transformado la biología, pero su gran tamaño dificulta su administración segura en tejidos humanos. Este estudio explora IscB, un primo mucho más pequeño de Cas9, para entender cómo permanece desactivado hasta encontrarse con la secuencia de ADN exactamente correcta. Al observar las pequeñas piezas móviles de IscB con detalle casi atómico, los autores revelan cómo evita cortes indeseados y cómo se puede ajustar su rendimiento para aplicaciones médicas futuras. 
Un ancestro diminuto del caballo de batalla de CRISPR
IscB procede de elementos genéticos móviles ancestrales y se considera un posible antecesor evolutivo de Cas9. Como Cas9, utiliza una guía de ARN para localizar el ADN coincidente y luego cortarlo, pero mide menos de la mitad que el Cas9 estándar usado en los laboratorios. Esa compacidad es atractiva para terapias que dependen de vectores virales, que imponen límites estrictos de carga. Hasta ahora, sin embargo, los investigadores solo habían obtenido una instantánea de IscB unido al ADN. Las piezas clave que faltaban eran cómo luce la proteína en reposo, cómo evalúa posibles dianas y cómo pasa de ser un observador inocuo a un cortador activo.
Capturar la proteína en acción
Para completar este panorama, el equipo diseñó una versión ligeramente modificada y más estable de IscB y la examinó mediante criomicroscopía electrónica. Capturaron cuatro estados distintos: una forma de reposo sin ADN, dos intermedios donde la guía de ARN empareja solo 6 o 10 bases del ADN, y un estado preparado en el que 16 bases están emparejadas y el ADN está listo para ser cortado. Estas imágenes de alta resolución trazan una vía continua desde totalmente inactiva hasta totalmente activa. Muestran que los dos centros de corte de IscB están excepcionalmente próximos y conectados por «bisagras» cortas en lugar de largos conectores flexibles, lo que ayuda a explicar cómo una proteína tan pequeña puede realizar una tarea compleja.
Tapas de ARN y un "pedal" molecular
Las estructuras revelan que IscB emplea un elegante sistema de doble cierre construido con su propio ARN. Una parte del ARN se pliega sobre el primer centro de corte como una tapa, mientras que otra sección se pliega sobre el segundo, bloqueando el acceso de hebras de ADN errantes. A medida que la guía de ARN se empareja gradualmente con una diana de ADN correcta, no se desplaza de una vez; en cambio, avanza por etapas, como un pedal de coche que se presiona lentamente. Cuando alrededor de 11 bases coinciden, este movimiento finalmente expulsa las tapas de ARN y remodela una región clave llamada dominio HNH, que gira aproximadamente 90 grados hacia una posición activa. Este umbral ayuda a asegurar que IscB responda solo a secuencias con alta coincidencia, limitando cortes fuera de objetivo. 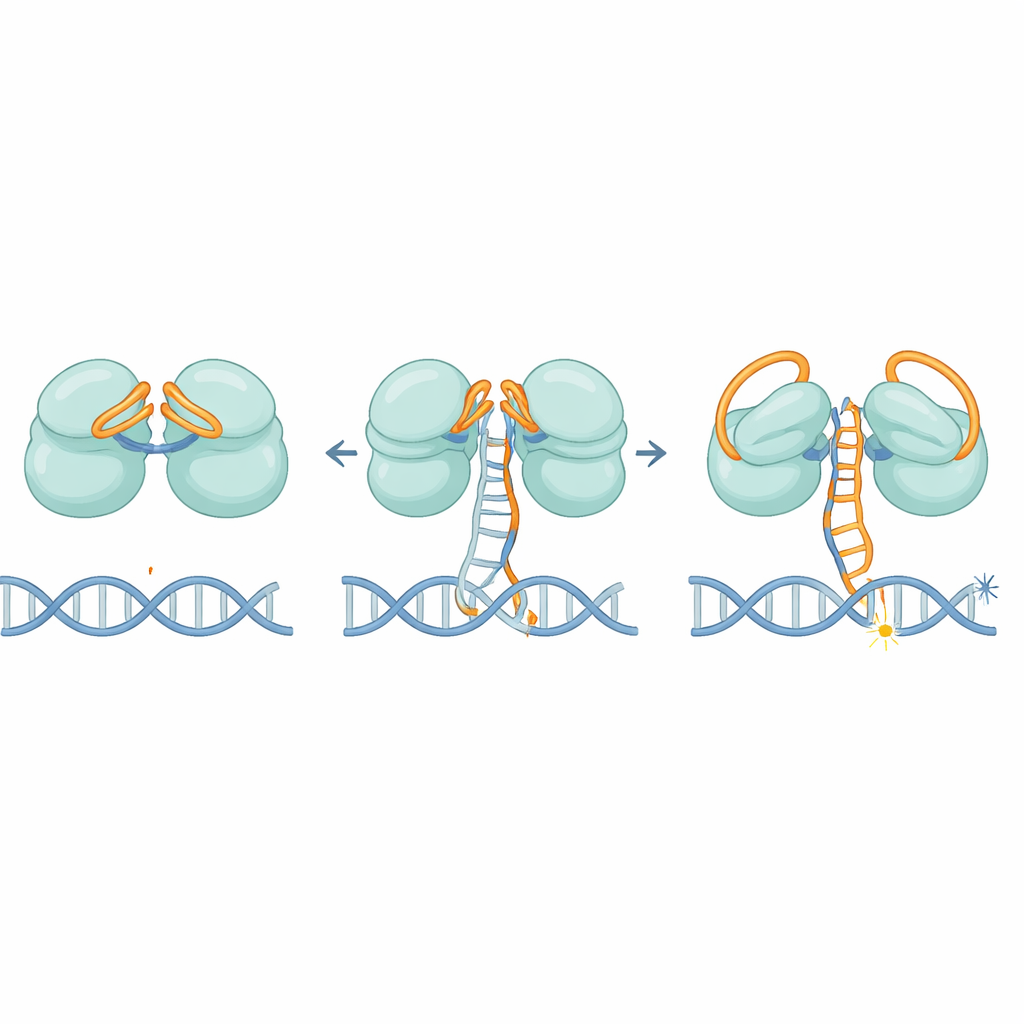
Cómo IscB abre el ADN y lo mantiene firme
Una vez activado, IscB debe separar las dos hebras de la doble hélice y mantenerlas apartadas el tiempo suficiente para cortar. Los autores identifican un pequeño bucle en la proteína que se inserta en el ADN, forzando la separación de las hebras en la región donde el ARN y el ADN forman una estructura híbrida. Parchees cargados positivamente a lo largo de las bisagras luego sujetan la hebra desplazada, estabilizando esta burbuja tipo "R-loop". Mutaciones que debilitan ese cuña o la franja cargada reducen drásticamente la actividad de corte del ADN, confirmando que son esenciales tanto para abrir como para mantener el ADN en su lugar.
Ajustar las bisagras para crear mejores editores
Dado que las bisagras controlan cuán fácilmente puede girar en acción el dominio HNH, los investigadores probaron si cambios sutiles allí podrían mejorar el rendimiento. Reemplazando ciertos aminoácidos voluminosos por otros más pequeños y flexibles, crearon variantes de IscB cuyas bisagras se mueven con mayor libertad. En células humanas, dos de estas versiones modificadas, denominadas Hig1 y Hig2, mostraron una actividad de edición notablemente superior. Una variante alcanzó una eficiencia cercana a la de una herramienta Cas9 avanzada mientras provocaba menos roturas de ADN no deseadas a lo largo del genoma, lo que sugiere que aflojar con cuidado estas bisagras puede hacer a IscB tanto más potente como más preciso.
Por qué esto importa para las terapias génicas futuras
En conjunto, estos hallazgos muestran cómo una enzima de edición del genoma compacta puede permanecer segura y bloqueada hasta encontrar una coincidencia de ADN casi perfecta, y luego reorganizarse rápidamente para cortar en el lugar adecuado. Al mapear cada paso —desde las tapas de ARN que protegen los centros de corte hasta el movimiento tipo pedal que desencadena la activación y las bisagras que dirigen el corte final— el trabajo ofrece un plano para diseñar editores del genoma más pequeños y seguros. Tales herramientas podrían ser más fáciles de empaquetar en sistemas de administración médica y, en última instancia, permitir tratamientos más precisos con menos efectos secundarios.
Cita: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Palabras clave: IscB, edición del genoma, CRISPR, Nucleasa guiada por ARN, biología estructural