Clear Sky Science · sv
Strukturell insikt i IscB:s RNA-lock-baserade inaktiveringsmekanism
Mindre gensax med inbyggd säkerhetslås
Genredigeringsverktyg som CRISPR–Cas9 har förändrat biologin, men deras stora storlek gör dem svåra att leverera säkert till mänsklig vävnad. Denna studie undersöker IscB, en mycket mindre kusin till Cas9, för att förstå hur den förblir säkert avstängd tills den möter exakt rätt DNA-sekvens. Genom att i nästan atomär detalj följa IscB:s små rörliga delar visar författarna hur proteinet skyddar mot oönskade klipp och hur dess prestanda kan justeras för framtida medicinska tillämpningar. 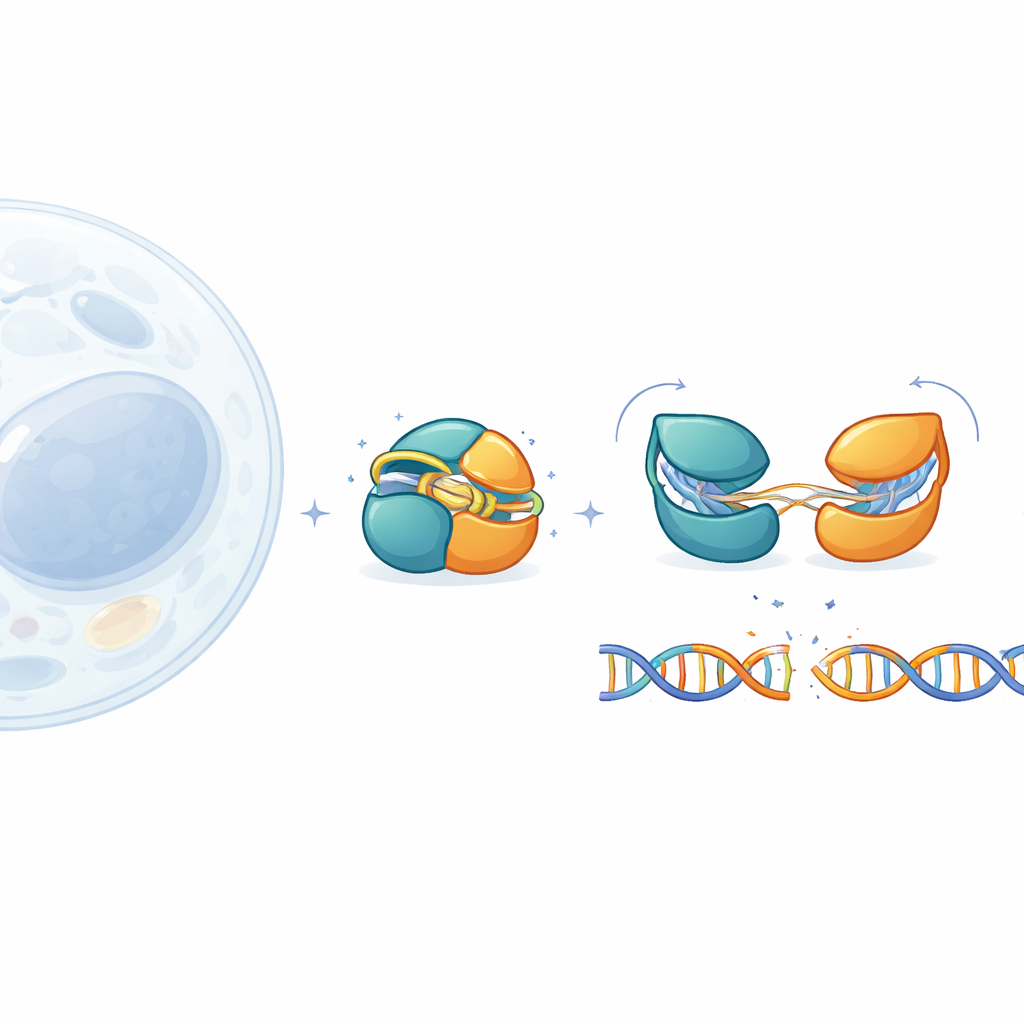
En liten förfader till CRISPR:s arbetshäst
IscB härstammar från gamla mobila genetiska element och antas vara en evolutionär föregångare till Cas9. Likt Cas9 använder den en RNA-guide för att hitta matchande DNA och sedan skära det, men den är mindre än hälften så stor som den standard-Cas9 som används i laboratorier. Denna kompakthet är attraktiv för terapier som förlitar sig på virusvektorer, vilka har strikta lastbegränsningar. Fram till nu hade forskare dock endast sett en ögonblicksbild av IscB bunden till DNA. De viktiga saknade bitarna var hur proteinet ser ut när det är inaktivt, hur det testar potentiella mål och hur det går från att vara en harmlös åskådare till en aktiv sax.
Fånga proteinet i arbete
För att fylla i denna bild konstruerade teamet en något modifierad, mer stabil version av IscB och undersökte den med kryoelektronmikroskopi. De fångade fyra distinkta tillstånd: en vilande form utan DNA, två intermediära där RNA-guiden parar med bara 6 respektive 10 DNA-bokstäver, och ett förberett tillstånd där 16 bokstäver är parade och DNA:t är redo att klippas. Dessa högupplösta bilder skildrar en kontinuerlig väg från helt av till helt på. De visar att IscB:s två klyvningscentra ligger ovanligt nära varandra och är förbundna med korta ”gångjärn” snarare än långa sladdriga länkar, vilket bidrar till att förklara hur ett så litet protein kan utföra en komplex uppgift.
RNA-lock och ett molekylärt bilpedal
Strukturerna visar att IscB använder ett elegant dubbel-låssystem uppbyggt av sitt eget RNA. En del av RNA:t viks över det första klyvningscentret som ett lock, medan en annan sektion böjer sig över det andra och blockerar åtkomst för främlings-DNA-strängar. När RNA-guiden gradvis parar sig med ett korrekt DNA-mål rör den sig inte allt på en gång; i stället förskjuts den i steg, likt en bilpedal som trycks ned långsamt. När ungefär 11 matchande bokstäver är parade trycker denna rörelse slutligen RNA-locken åt sidan och omformar en nyckelregion kallad HNH-domänen, som svänger ungefär 90 grader till en aktiv position. Denna tröskel hjälper till att säkerställa att IscB endast reagerar på starkt matchande sekvenser, vilket begränsar oönskade klipp. 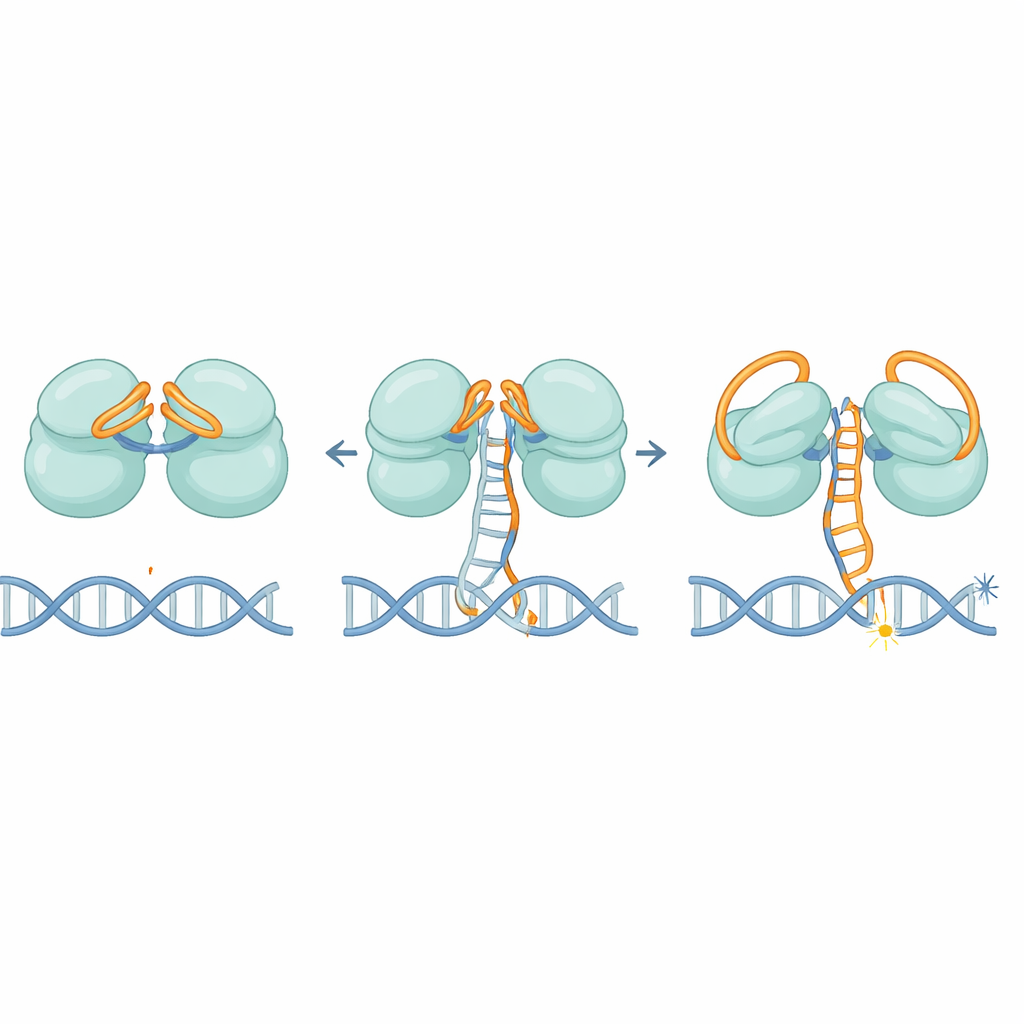
Hur IscB kilas upp DNA och håller det stabilt
När den väl aktiverats måste IscB separera de två strängarna i DNA-dubbelhelixen och hålla dem isär tillräckligt länge för att klippa. Författarna identifierar en liten slinga på proteinet som kilas in i DNA:t och tvingar strängarna isär i det område där RNA och DNA bildar en hybridstruktur. Positivt laddade ytor längs gångjärnen greppar sedan den förskjutna strängen och stabiliserar denna bubbelliknande ”R-loop”. Mutationer som försvagar denna kil eller det laddade bandet minskar skarpt DNA-klippaktiviteten, vilket bekräftar att de är avgörande för både att öppna och hålla DNA:t på plats.
Finjustera gångjärnen för att bygga bättre redskap
Eftersom gångjärnen styr hur lätt HNH-domänen kan svänga i aktion testade forskarna om subtila förändringar där kunde förbättra prestandan. Genom att ersätta vissa skrymmande aminosyror med mindre, mer flexibla sådana skapade de IscB-varianter vars gångjärn rör sig friare. I humana celler visade två av dessa konstruerade varianter, döpta Hig1 och Hig2, märkbart högre redigeringsaktivitet. En variant närmade sig effektiviteten hos ett avancerat Cas9-verktyg samtidigt som den orsakade färre oönskade DNA-brott över genomet, vilket tyder på att en noggrann uppluckring av dessa gångjärn kan göra IscB både kraftfullare och mer precis.
Varför detta är viktigt för framtida genterapier
Tillsammans visar dessa fynd hur ett kompakt genredigeringsenzym kan förbli säkert låst tills det stöter på en nästan perfekt DNA-match och sedan snabbt omorganisera sig för att skära på rätt ställe. Genom att kartlägga varje steg — från RNA-lock som skärmar av klyvningscentrumen till den bilpedalsliknande rörelsen som utlöser aktivering och gångjärnen som styr den slutliga snittet — erbjuder arbetet en plan för att designa mindre, säkrare genredigerare. Sådana verktyg kan vara enklare att paketera i medicinska leveranssystem och kan i slutändan möjliggöra mer precisa behandlingar med färre biverkningar.
Citering: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Nyckelord: IscB, genredigering, CRISPR, RNA-styrt nukleas, struktural biologi