Clear Sky Science · ar
رؤية بنيوية لآلية إيقاف تشغيل IscB القائمة على غطاء الحمض النووي الريبي
مقصات جينية أصغر مزودة بقفل أمان مدمج
أدوات تحرير الجينات مثل CRISPR–Cas9 غيرت وجه علم الأحياء، لكن حجمها الكبير يصعّب إيصالها بأمان إلى أنسجة الإنسان. يستكشف هذا البحث IscB، قِرْينًا أصغر بكثير من Cas9، لفهم كيف يبقى معطلاً بأمان حتى يصادف تسلسل الحمض النووي الصحيح بالضبط. من خلال مراقبة الأجزاء المتحركة الصغيرة في IscB بتفصيل قريب من الذري، يكشف المؤلفون كيف يمنع الشقوق العرضية وكيف يمكن ضبط أدائه لتطبيقات طبية مستقبلية. 
سلف صغير لمحرك CRISPR
ينحدر IscB من عناصر جينية متنقلة قديمة ويُعتقد أنه سلف تطوري لـ Cas9. مثل Cas9، يستخدم دليلاً من الحمض النووي الريبي للعثور على الحمض النووي المطابق ثم قطعه، لكنه أقل من نصف حجم Cas9 القياسي المستخدم في المختبرات. هذه الصغرية جذابة للعلاجات التي تعتمد على نواقل فيروسية ذات حدود صارمة للحِمل. حتى الآن، مع ذلك، رأى الباحثون لقطة واحدة فقط لـ IscB مرتبطًا بالحمض النووي. كانت القطع المفقودة الرئيسية هي شكل البروتين عندما يكون في حالة سكون، وكيف يختبر الأهداف المحتملة، وكيف ينتقل من مجرد مراقب غير مؤذ إلى قاطع نشط.
ملاحقة البروتين في حالة العمل
لملء هذه الصورة، صمم الفريق نسخة معدلة قليلاً وأكثر استقرارًا من IscB وفحصها باستخدام المجهر الإلكتروني بالتبريد. التقطوا أربع حالات مميزة: شكل في حالة سكون بدون حمض نووي، حالتا وسيطة حيث يقترن دليل الحمض النووي الريبي مع 6 أو 10 حروف من الحمض النووي فقط، وحالة مهيأة حيث يتزاوج 16 حرفًا ويصبح الحمض النووي جاهزًا للقطع. تتبع هذه الصور عالية الدقة مسارًا مستمرًا من الحالة المعطلة تمامًا إلى الحالة النشطة تمامًا. تُظهر أن مركزي القطع في IscB مكتظان بشكل غير اعتيادي وبمترابطين بواسطة «مفاصل» قصيرة بدلًا من روابط طويلة مرنة، ما يساعد على تفسير كيف يمكن لبروتين صغير جدًا أن يقوم بمهمة معقدة.
أغطية الحمض النووي الريبي ودواسة جزيئية
تكشف الهياكل أن IscB يستخدم نظام قفل مزدوج أنيق مصنوعًا من حمضه النووي الريبي الخاص. جزء من الحمض النووي الريبي يطوى فوق مركز القطع الأول مثل غطاء، بينما ينحني قسم آخر عبر الثاني، مانعًا الوصول إلى سلاسل الحمض النووي غير المرغوب فيها. مع اقتران دليل الحمض النووي الريبي تدريجيًا بالهدف الصحيح من الحمض النووي، لا ينتقل كله دفعة واحدة؛ بل يتحرك على مراحل، مثل دواسة سيارة تُضغط ببطء. عندما يتزاوج نحو 11 حرفًا متطابقًا، يدفع هذا التحرك أخيرًا أغطية الحمض النووي الريبي بعيدًا ويُعيد تشكيل منطقة رئيسية تُسمى دومين HNH، الذي يدور بحوالي 90 درجة إلى وضع نشط. يساعد هذا العتبة على ضمان استجابة IscB فقط لتسلسلات متطابقة بقوة، محددًا الشقوق خارج الهدف.
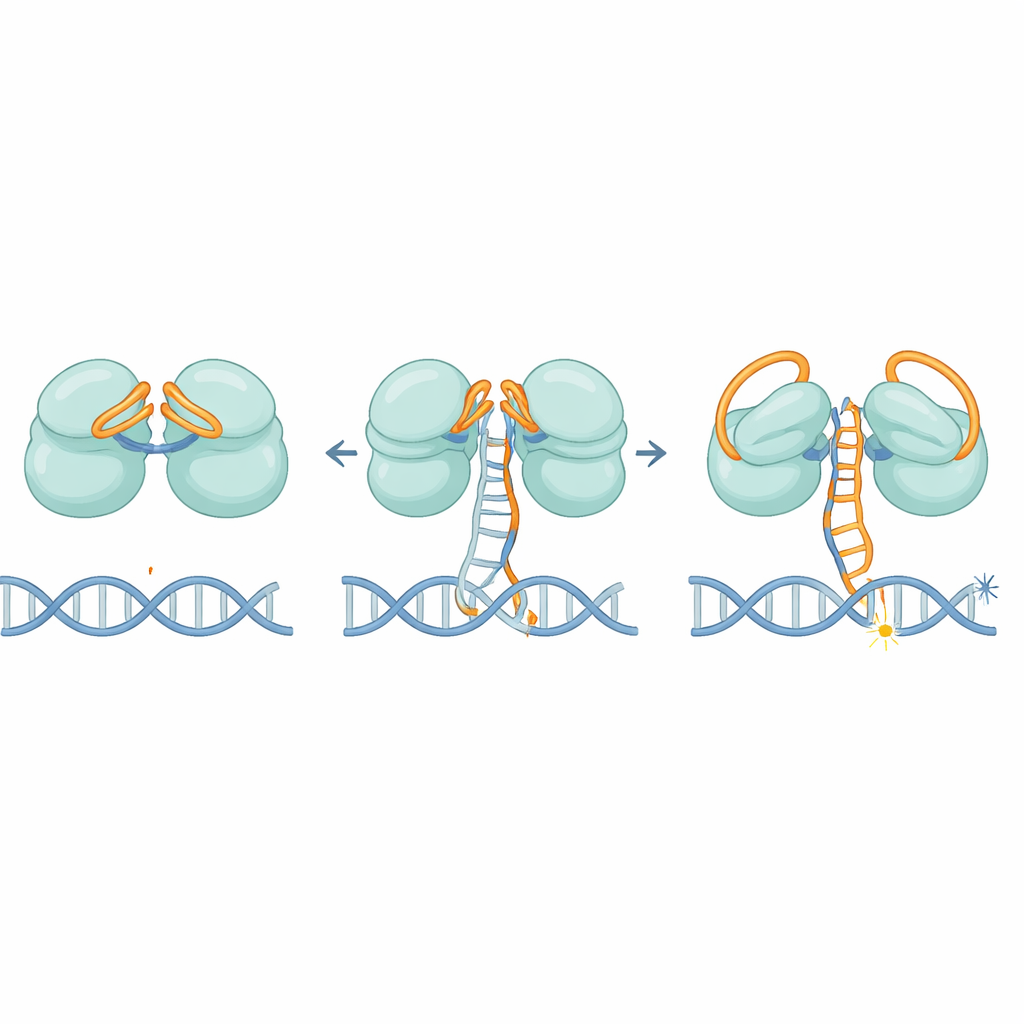
كيف يفتح IscB الحمض النووي ويثبته
بمجرد تفعيله، يجب على IscB فصل سلسلتي لولب الحمض النووي والاحتفاظ بهما مفصولتين بما يكفي لإجراء القطع. يحدد المؤلفون حلقة صغيرة على البروتين تعمل وتدًا في الحمض النووي، فتفصل السلاسل في المنطقة التي يشكل فيها الحمض النووي الريبي والحمض النووي هجينًا. ثم تمسك بقع مشحونة إيجابيًا على طول المفاصل بالسلسلة المزعزعة، مثبتة فقاعة تشبه الحَلْقَة تُسمى R-loop. تقلل الطفرات التي تضعف هذا الوتد أو الشريط المشحون بدرجة كبيرة من نشاط قطع الحمض النووي، مؤكدة أنها أساسية لكل من فتح الحمض النووي وإبقائه في موضعه.
ضبط المفاصل لبناء محررات أفضل
لأن المفاصل تتحكم في سهولة تأرجح دومين HNH نحو العمل، اختبر الباحثون ما إذا كانت تغييرات طفيفة هناك يمكن أن تعزز الأداء. عن طريق استبدال بعض الأحماض الأمينية الضخمة بأخرى أصغر وأكثر مرونة، صنعوا متغيرات من IscB تتحرك مفاصلها بحرية أكبر. في خلايا بشرية، أظهرت اثنتان من هذه النسخ المصمّمة، المسماة Hig1 وHig2، نشاط تحرير أعلى بشكل ملحوظ. اقترب أحد المتغيرات من كفاءة أداة Cas9 متقدمة مع إحداث عدد أقل من الشقوق غير المقصودة عبر الجينوم، مما يوحي بأن تخفيف هذه المفاصل بعناية يمكن أن يجعل IscB أكثر قوة ودقة في آن واحد.
لماذا هذا مهم لعلاجات الجينات المستقبلية
معًا، تُظهر هذه النتائج كيف يمكن لإنزيم تحرير جينات مدمج أن يظل مقفلاً بأمان حتى يواجه مطابقة قريبة للكمال في تسلسل الحمض النووي، ثم يعيد ترتيب نفسه بسرعة ليقطع في الموضع الصحيح. من خلال تتبع كل خطوة — من أغطية الحمض النووي الريبي التي تحمي مراكز القطع إلى حركة شبيهة بدواسة السيارة التي تُشغّل التفعيل والمفاصل التي توجه الشق النهائي — يقدم العمل مخططًا لتصميم محررات جينوم أصغر وأكثر أمانًا. قد يكون من الأسهل تعبئة مثل هذه الأدوات في أنظمة التوصيل الطبية وقد تمكّن في نهاية المطاف علاجات أكثر دقة بآثار جانبية أقل.
الاستشهاد: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
الكلمات المفتاحية: IscB, تحرير الجينات, CRISPR, نيوكلياز موجَّه بالحمض النووي الريبي, بيولوجيا بنيوية