Clear Sky Science · it
Intuizioni strutturali sul meccanismo di inattivazione basato su un coperchio di RNA di IscB
Forbici geniche più piccole con un blocco di sicurezza integrato
Strumenti per l’editing genico come CRISPR–Cas9 hanno trasformato la biologia, ma le loro grandi dimensioni rendono difficile la somministrazione sicura nei tessuti umani. Questo studio esplora IscB, un cugino molto più piccolo di Cas9, per capire come rimane spento in modo sicuro fino a quando non incontra esattamente la sequenza di DNA corretta. Osservando le piccole parti mobili di IscB a dettaglio quasi atomico, gli autori rivelano come esso si protegga da tagli accidentali e come le sue prestazioni possano essere modulate per future applicazioni mediche. 
Un piccolo antenato della macchina da lavoro del CRISPR
IscB proviene da antichi elementi genetici mobili ed è ritenuto un antenato evolutivo di Cas9. Come Cas9, utilizza una guida di RNA per riconoscere il DNA corrispondente e poi tagliarlo, ma è meno della metà delle dimensioni del Cas9 standard impiegato nei laboratori. Questa compattezza è attraente per terapie che si basano su vettori virali, i quali hanno limiti rigorosi di carico. Finora, tuttavia, i ricercatori avevano osservato solo un’istantanea di IscB legato al DNA. I tasselli mancanti erano come appare la proteina quando è a riposo, come testa potenziali bersagli e come passa da spettatore innocuo a taglierino attivo.
Cogliere la proteina in azione
Per completare questo quadro, il team ha ingegnerizzato una versione leggermente modificata e più stabile di IscB e l’ha esaminata mediante crio-microscopia elettronica. Hanno catturato quattro stati distinti: una forma a riposo senza DNA, due intermedi in cui la guida di RNA si appaia con solo 6 o 10 basi del DNA, e uno stato pronto in cui 16 basi sono appaiate e il DNA è pronto per essere tagliato. Queste immagini ad alta risoluzione tracciano un percorso continuo dall’off completamente all’on. Mostrano che i due centri di taglio di IscB sono confezionati in modo insolitamente ravvicinato e collegati da brevi “cerniere” anziché da lunghi connettori flessibili, contribuendo a spiegare come una proteina così piccola possa svolgere un compito complesso.
Coperchi di RNA e un pedale molecolare
Le strutture rivelano che IscB impiega un elegante sistema a doppia serratura fatto dal suo stesso RNA. Una parte dell’RNA si ripiega sopra il primo centro di taglio come un coperchio, mentre un’altra sezione si piega sopra il secondo, bloccando l’accesso a filamenti di DNA estranei. Man mano che la guida di RNA si appaia gradualmente con un bersaglio DNA corretto, non si sposta tutta in una volta; invece si muove per fasi, come un pedale dell’auto che viene premuto lentamente. Quando circa 11 basi corrispondenti sono appaiate, questo movimento sposta finalmente i coperchi di RNA e rimodella una regione chiave chiamata dominio HNH, che ruota di circa 90 gradi nella posizione attiva. Questa soglia aiuta a garantire che IscB risponda solo a sequenze fortemente corrispondenti, limitando i tagli fuori bersaglio. 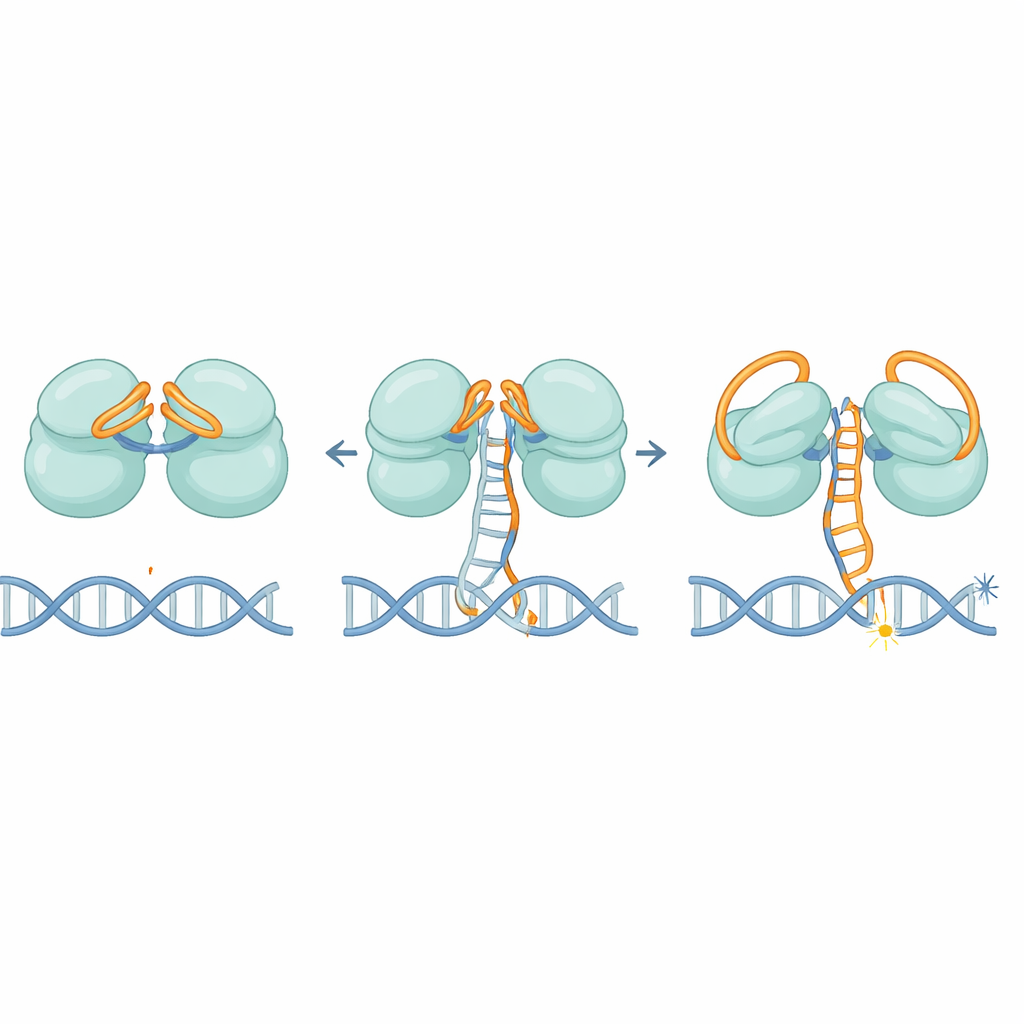
Come IscB apre il DNA e lo mantiene stabile
Una volta attivato, IscB deve separare i due filamenti della doppia elica di DNA e tenerli distanziati abbastanza a lungo da poter tagliare. Gli autori identificano un piccolo anello sulla proteina che si infila nel DNA, forzando l’allontanamento dei filamenti nella regione dove RNA e DNA formano un ibrido. Chiazze cariche positivamente lungo le cerniere poi aggrappano il filamento spostato, stabilizzando questa struttura a bolle chiamata “R-loop”. Mutazioni che indeboliscono questo cuneo o la banda carica riducono drasticamente l’attività di taglio del DNA, confermando che sono essenziali sia per aprire sia per mantenere il DNA in posizione.
Regolare le cerniere per costruire editor migliori
Poiché le cerniere controllano quanto facilmente il dominio HNH può innescare il movimento, i ricercatori hanno testato se modifiche sottili lì potessero migliorare le prestazioni. Sostituendo alcuni amminoacidi voluminosi con altri più piccoli e flessibili, hanno creato varianti di IscB con cerniere più mobili. In cellule umane, due di queste versioni ingegnerizzate, nominate Hig1 e Hig2, hanno mostrato un’attività di editing nettamente superiore. Una variante ha raggiunto un’efficienza vicina a quella di uno strumento Cas9 avanzato pur causando meno rotture di DNA non intenzionali nel genoma, suggerendo che allentare con attenzione queste cerniere può rendere IscB sia più potente sia più preciso.
Perché questo conta per le future terapie geniche
Nel loro insieme, questi risultati mostrano come un enzima per l’editing genico compatto possa rimanere bloccato in modo sicuro finché non incontra una corrispondenza quasi perfetta del DNA, per poi riorganizzarsi rapidamente e tagliare nel punto giusto. Mappando ogni passaggio — dai coperchi di RNA che schermano i centri di taglio al movimento simile a un pedale che innesca l’attivazione e alle cerniere che guidano il taglio finale — il lavoro offre un progetto per progettare editor genomici più piccoli e più sicuri. Strumenti del genere potrebbero essere più facili da imballare nei sistemi di somministrazione medica e potrebbero infine permettere terapie più precise con meno effetti collaterali.
Citazione: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Parole chiave: IscB, editing genomico, CRISPR, nucleasi guidata da RNA, biologia strutturale