Clear Sky Science · ru
Структурное понимание механизма инактивации IscB на основе РНК-крышки
Меньшие «генные ножницы» с встроенным предохранителем
Инструменты для редактирования генов, такие как CRISPR–Cas9, преобразили биологию, но их большой размер затрудняет безопасную доставку в ткани человека. В этом исследовании изучают IscB — гораздо меньшего родственника Cas9 — чтобы понять, как он остаётся выключенным до тех пор, пока не встретит именно ту ДНК‑последовательность. Наблюдая за крошечными подвижными частями IscB с почти атомарным разрешением, авторы показывают, как белок защищается от случайных разрезов и как можно настроить его работу для будущих медицинских применений. 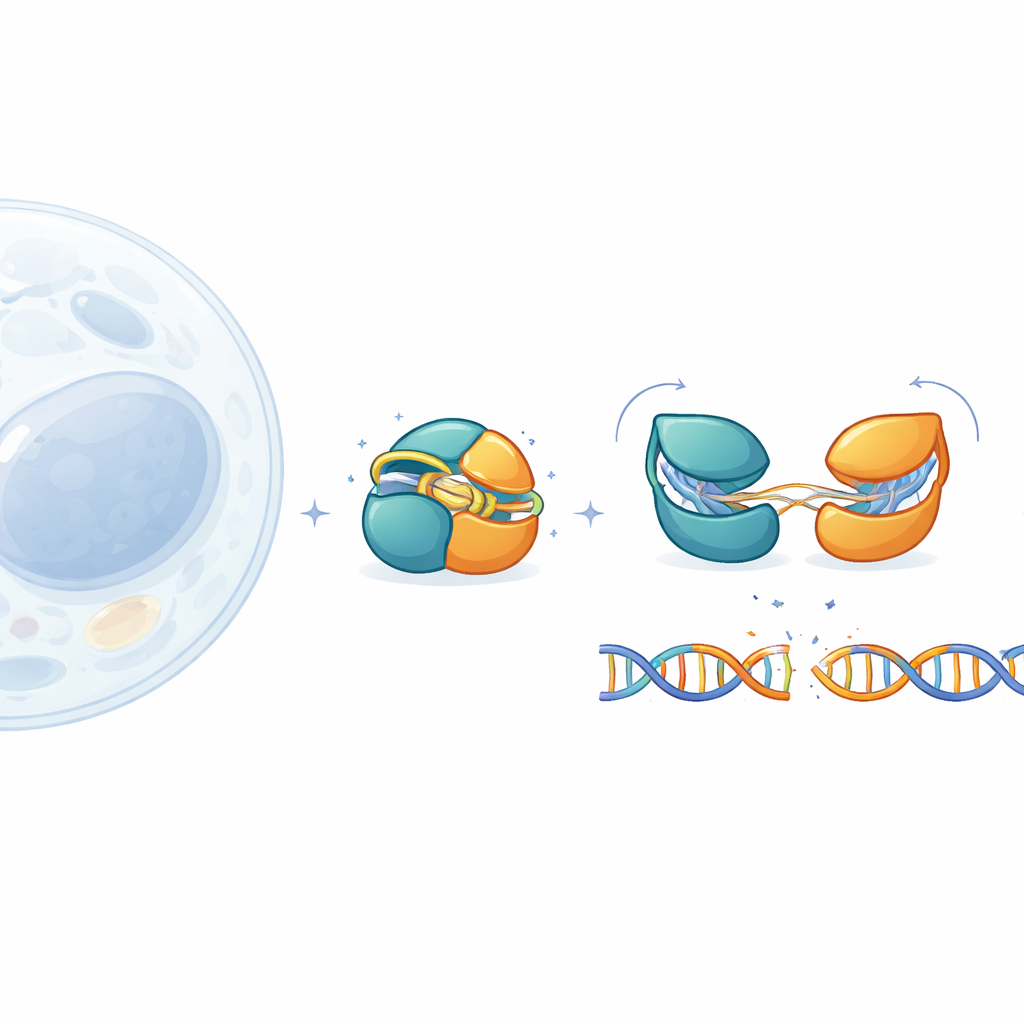
Крошечный предок «трудяги» CRISPR
IscB происходит из древних мобильных генетических элементов и считается эволюционным предшественником Cas9. Как и Cas9, он использует РНК-наводчик, чтобы находить совпадающую ДНК и затем разрезать её, но его размер менее чем вдвое меньше стандартного лабораторного Cas9. Такая компактность привлекательна для терапии, основанной на вирусных векторах, у которых строго ограничен объём груза. До сих пор исследователи видели лишь один снимок IscB, связанного с ДНК. Ключевыми недостающими фрагментами оставались то, как белок выглядит в спокойном состоянии, как он проверяет потенциальные мишени и как переключается из безобидного наблюдателя в активный режущий фермент.
Поймать белок в действии
Чтобы восполнить эту картину, команда разработала слегка модифицированную, более стабильную версию IscB и исследовала её с помощью крио‑электронной микроскопии. Они зафиксировали четыре разных состояния: спокойную форму без ДНК, два промежуточных состояния, где РНК‑наводчик спаривается лишь с 6 или 10 буквами ДНК, и «готовое» состояние, в котором спарены 16 букв и ДНК подготовлена к разрезу. Эти изображения высокого разрешения прослеживают непрерывный путь от полностью выключенного до полностью активного состояния. Они показывают, что два режущих центра IscB расположены необычно близко и соединены короткими «шарнирами», а не длинными гибкими связками, что помогает объяснить, как такой небольшой белок способен выполнять сложную задачу.
РНК‑крышки и молекулярная педаль газа
Структуры показывают, что IscB использует изящную двойную систему блокировок, выполненную из его собственной РНК. Одна часть РНК складывается над первым режущим центром как крышка, в то время как другая секция изгибается над вторым, блокируя доступ посторонних нитей ДНК. По мере того как РНК‑наводчик постепенно спаривается с правильной ДНК‑мишенью, он не двигается сразу; вместо этого сдвиги происходят ступенчато, как педаль автомобиля, которая медленно нажимается. При спаривании примерно 11 совпадающих букв этот ход в конечном счёте выталкивает РНК‑крышки в сторону и перестраивает ключевую область, называемую доменом HNH, который поворачивается примерно на 90 градусов в активное положение. Этот порог помогает гарантировать, что IscB срабатывает только на тесно совпадающие последовательности, ограничивая побочные разрезы. 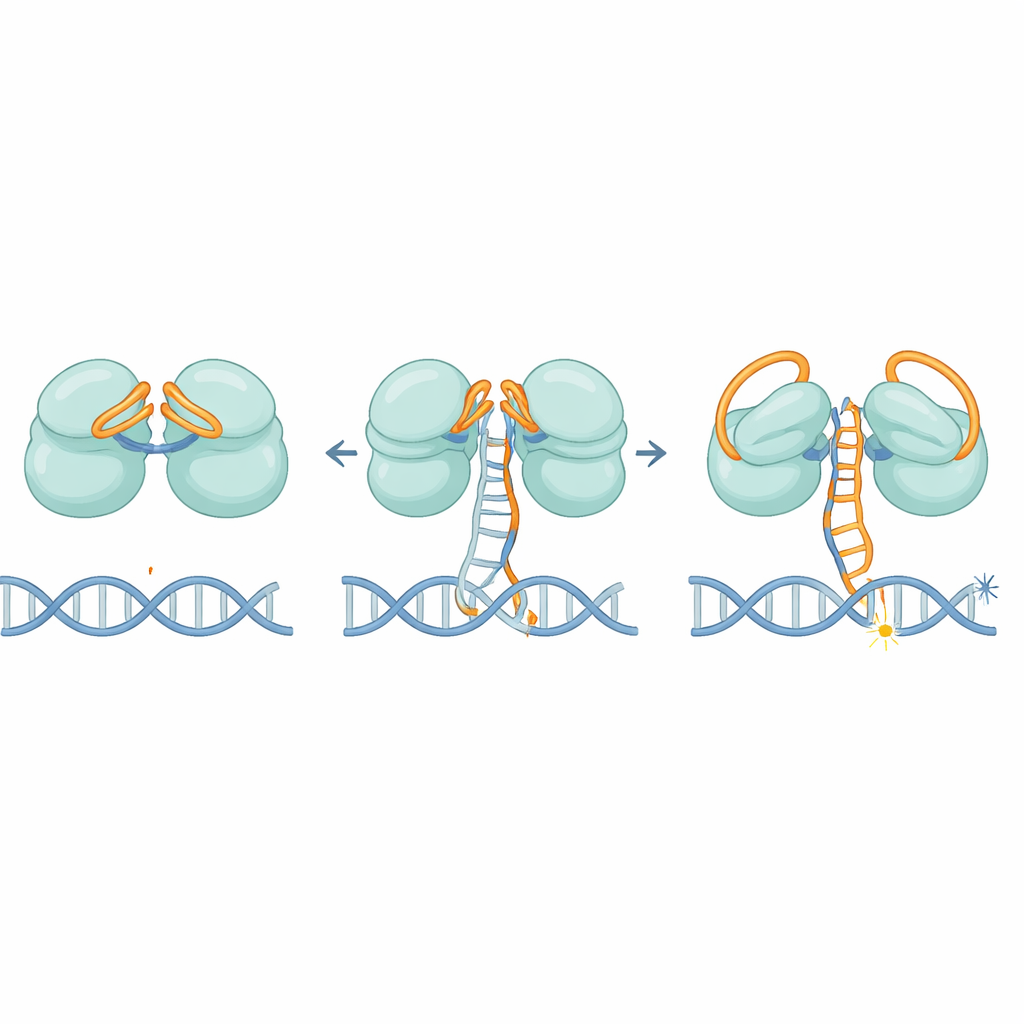
Как IscB раскрывает ДНК и удерживает её в стабильном состоянии
После активации IscB должен раздвинуть две нити двойной спирали ДНК и держать их раздельно достаточно долго, чтобы выполнить разрез. Авторы выявили небольшой петельчатый участок на белке, который клином втапливается в ДНК, раздвигая нити в области, где РНК и ДНК формируют гибрид. Положительно заряженные участки вдоль шарниров затем захватывают смещённую нитку, стабилизируя эту пузырчатую «R‑петлю». Мутации, ослабляющие этот клин или заряженную полосу, резко снижают активность по разрезанию ДНК, что подтверждает их ключевую роль в раскрытии и удержании ДНК.
Настройка шарниров для создания лучших редакторов
Поскольку шарниры контролируют, насколько легко домен HNH может размахнуться в активное положение, исследователи проверили, не улучшится ли работа при тонких изменениях там. Заменив некоторые крупные аминокислоты на более мелкие и гибкие, они создали варианты IscB с более подвижными шарнирами. В человеческих клетках два из этих инженерных вариантов, названные Hig1 и Hig2, продемонстрировали заметно более высокую активность редактирования. Один вариант приблизился по эффективности к продвинутому инструменту Cas9, причиняя при этом меньше непреднамеренных разрезов по всему геному, что указывает на то, что аккуратное ослабление шарниров может сделать IscB одновременно мощнее и точнее.
Почему это важно для будущих генотерапий
Вместе эти результаты показывают, как компактный фермент для редактирования генома может оставаться надёжно заблокированным до встречи с почти идеальным совпадением ДНК, а затем быстро перестраиваться, чтобы разрезать в нужном месте. Нанесение на карту каждого шага — от РНК‑крышек, защищающих режущие центры, до «педальноподобного» движения, запускающего активацию, и шарниров, направляющих окончательный разрез — даёт план для разработки меньших и безопаснее редакторов генома. Такие инструменты легче упаковывать в медицинские системы доставки и они потенциально позволят добиться более точных терапий с меньшим числом побочных эффектов.
Цитирование: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Ключевые слова: IscB, редактирование генома, CRISPR, Нуклеаза, направляемая РНК, структурная биология