Clear Sky Science · nl
Structureel inzicht in het RNA-deksel-gebaseerde inactivatiemechanisme van IscB
Kleinere gen-scharen met een ingebouwd veiligheidsslot
Gereedschappen voor genbewerking zoals CRISPR–Cas9 hebben de biologie getransformeerd, maar hun grote omvang bemoeilijkt veilige levering in menselijke weefsels. Deze studie onderzoekt IscB, een veel kleinere verwant van Cas9, om te begrijpen hoe het veilig uitgeschakeld blijft totdat het precies de juiste DNA-sequentie tegenkomt. Door IscB’s kleine bewegende onderdelen tot bijna atomair detail te volgen, onthullen de auteurs hoe het beschermt tegen toevallige knipsels en hoe de werking kan worden bijgesteld voor toekomstige medische toepassingen. 
Een klein vooroudertje van CRISPR’s werkpaard
IscB stamt uit oude mobiele genetische elementen en wordt gezien als een evolutionaire voorloper van Cas9. Net als Cas9 gebruikt het een RNA-gids om naar overeenkomstig DNA te zoeken en dit vervolgens te knippen, maar het is minder dan de helft zo groot als de standaard Cas9 die in laboratoria wordt gebruikt. Die compactheid is aantrekkelijk voor therapieën die op virale vectoren vertrouwen, die strikte vrachtgrenzen hebben. Tot nu toe hadden onderzoekers echter slechts één momentopname gezien van IscB gebonden aan DNA. De belangrijke ontbrekende stukken waren hoe het eiwit eruitziet in rust, hoe het potentiële doelwitten test en hoe het omschakelt van een onschuldig toeschouwer naar een actief knipmiddel.
Het eiwit in actie vangen
Om dit beeld aan te vullen, maakten de onderzoekers een licht aangepast, stabieler variant van IscB en onderzochten die met cryo-elektronenmicroscopie. Ze legden vier verschillende toestanden vast: een rustvorm zonder DNA, twee tussenstadia waarin de RNA-gids slechts met 6 of 10 DNA-letters paart, en een geprimede toestand waarin 16 letters zijn gepaard en het DNA klaar is om geknipt te worden. Deze hoge-resolutiebeelden volgen een continu pad van volledig uit naar volledig aan. Ze tonen dat IscB’s twee snijcentra ongebruikelijk dicht bijeen liggen en verbonden zijn door korte “scharnieren” in plaats van lange slappe verbindingsstukken, wat helpt verklaren hoe zo’n klein eiwit een complexe taak kan uitvoeren.
RNA-deksels en een moleculaire gaspedaal
De structuren laten zien dat IscB een elegant dubbel-slot systeem gebruikt dat door het eigen RNA wordt gevormd. Een deel van het RNA vouwt zich over het eerste snijcentrum als een deksel, terwijl een andere sectie over het tweede buigt en de toegang tot losse DNA-strengen blokkeert. Terwijl de RNA-gids geleidelijk met een correct DNA-doel paart, beweegt die niet in één keer; in plaats daarvan verschuift hij in fases, als een autopedaal die langzaam wordt ingedrukt. Wanneer ongeveer 11 overeenkomende letters gepaard zijn, duwt deze beweging uiteindelijk de RNA-deksels opzij en hervormt een sleutelregio, het HNH-domein, dat ongeveer 90 graden doorslaat naar een actieve positie. Deze drempel helpt ervoor te zorgen dat IscB alleen reageert op sterk overeenkomende sequenties en beperkt zo off-target knipsels.
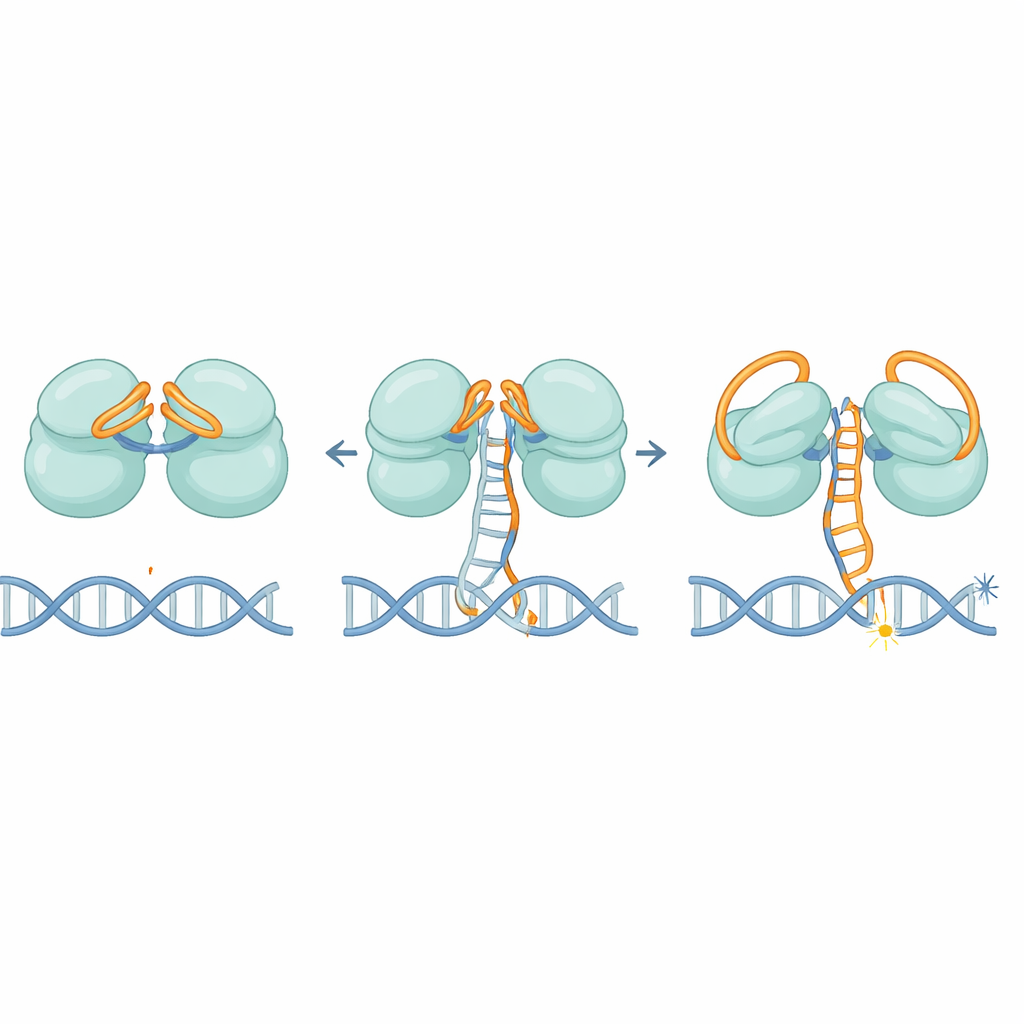
Hoe IscB DNA opentrekt en vasthoudt
Eens geactiveerd moet IscB de twee strengen van de DNA-dubbelhelix van elkaar scheiden en ze lang genoeg uit elkaar houden om te knippen. De auteurs identificeren een kleine lus op het eiwit die zich in het DNA klemt en de strengen uit elkaar dwingt in het gebied waar RNA en DNA een hybride vormen. Positief geladen zones langs de scharnieren grijpen vervolgens de verplaatste streng vast en stabiliseren deze belachtige “R-loop.” Mutaties die deze wig of de geladen band verzwakken, verminderen de DNA-knipactiviteit sterk, wat bevestigt dat ze essentieel zijn voor zowel het openen als het vasthouden van het DNA.
De scharnieren afstemmen om betere editors te bouwen
Aangezien de scharnieren bepalen hoe gemakkelijk het HNH-domein in actie kan zwaaien, testten de onderzoekers of subtiele wijzigingen daar de prestaties konden verbeteren. Door bepaalde volumineuze aminozuren te vervangen door kleinere, meer flexibele exemplaren, creëerden ze IscB-varianten waarvan de scharnieren vlotter bewegen. In menselijke cellen toonden twee van deze ontworpen versies, genoemd Hig1 en Hig2, duidelijk hogere bewerkingsactiviteit. Eén variant benaderde de efficiëntie van een geavanceerd Cas9-gereedschap terwijl het minder onbedoelde DNA-breuken door het genoom veroorzaakte, wat suggereert dat het zorgvuldig versoepelen van deze scharnieren IscB zowel krachtiger als preciezer kan maken.
Waarom dit belangrijk is voor toekomstige gentherapieën
Gezamenlijk laten deze bevindingen zien hoe een compact genbewerkingsenzym veilig vergrendeld kan blijven totdat het een bijna perfecte DNA-match tegenkomt, en zich vervolgens snel herordent om op de juiste plek te knippen. Door elke stap in kaart te brengen — van RNA-deksels die de snijcentra afschermen tot de gaspedaal-achtige beweging die activering triggert en de scharnieren die de laatste knip sturen — biedt het werk een blauwdruk voor het ontwerpen van kleinere, veiligere genoomeditors. Dergelijke instrumenten zouden gemakkelijker in medische afleversystemen te passen zijn en kunnen uiteindelijk preciezere behandelingen met minder bijwerkingen mogelijk maken.
Bronvermelding: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Trefwoorden: IscB, genoombewerking, CRISPR, RNA-gestuurde nuclease, structurele biologie