Clear Sky Science · de
Strukturelle Einblicke in IscBs RNA-Lid-basierten Inaktivierungsmechanismus
Kleinere Gen-Schere mit eingebauter Sicherheitsverriegelung
Werkzeuge zur Genbearbeitung wie CRISPR–Cas9 haben die Biologie revolutioniert, doch ihre große Größe erschwert eine sichere Lieferung in menschliches Gewebe. Diese Studie untersucht IscB, einen deutlich kleineren Verwandten von Cas9, um zu verstehen, wie er zuverlässig ausgeschaltet bleibt, bis er genau die passende DNA-Sequenz trifft. Indem die Autoren IscB‑s winzige bewegliche Teile in nahezu atomarer Detailauflösung beobachteten, zeigen sie, wie das Protein versehentliche Schnitte verhindert und wie seine Eigenschaften für zukünftige medizinische Anwendungen feinjustiert werden können. 
Ein winziger Vorfahre des CRISPR-Arbeitspferds
IscB stammt aus alten mobilen genetischen Elementen und gilt als evolutionärer Vorläufer von Cas9. Wie Cas9 nutzt es eine RNA‑Leitsequenz, um die passende DNA zu erkennen und dann zu zerschneiden, ist dabei aber weniger als halb so groß wie das in Laboren übliche Cas9. Diese Kompaktheit ist für Therapien attraktiv, die auf virale Vektoren angewiesen sind, welche strikte Ladekapazitätsgrenzen haben. Bislang hatten Forscher jedoch nur eine einzige Momentaufnahme von IscB in gebundener DNA‑Form gesehen. Entscheidend fehlten Erkenntnisse darüber, wie das Protein im Ruhezustand aussieht, wie es potenzielle Ziele prüft und wie es vom harmlosen Beobachter in einen aktiven Schneider umschaltet.
Das Protein in Aktion einfangen
Um dieses Bild zu vervollständigen, erzeugte das Team eine leicht modifizierte, stabilere Version von IscB und untersuchte sie mittels Kryo-Elektronenmikroskopie. Sie erfassten vier unterschiedliche Zustände: eine ruhende Form ohne DNA, zwei Zwischenzustände, in denen die RNA‑Leitsequenz nur 6 bzw. 10 DNA‑Basenpaare bildet, und einen einsatzbereiten Zustand, in dem 16 Basenpaare geordnet sind und die DNA zum Schnitt bereitsteht. Diese hochauflösenden Bilder zeichnen einen kontinuierlichen Weg vom vollständig ausgeschalteten bis zum vollständig aktiven Zustand nach. Sie zeigen, dass IscBs zwei Schnittzentren ungewöhnlich dicht beieinander liegen und durch kurze „Scharniere“ statt durch lange, flexible Verbindungen verbunden sind, was erklärt, wie ein so kleines Protein eine komplexe Aufgabe ausführen kann.
RNA‑Lids und ein molekulares Gaspedal
Die Strukturen zeigen, dass IscB ein elegantes Doppelverriegelungssystem aus seiner eigenen RNA nutzt. Ein Teil der RNA klappt wie ein Deckel über das erste Schnittzentrum, während ein anderer Abschnitt über das zweite gebogen ist und den Zugang zu fremden DNA‑Strängen blockiert. Während die Leit‑RNA allmählich mit einer korrekten DNA‑Sequenz paaren, bewegt sie sich nicht auf einen Schlag; stattdessen verschiebt sie sich in Stufen, ähnlich dem langsamen Durchdrücken eines Gaspedals. Wenn etwa 11 übereinstimmende Basenpaare gebildet sind, drückt diese Bewegung schließlich die RNA‑Deckel beiseite und formt einen entscheidenden Bereich, die HNH‑Domäne, um, die sich um etwa 90 Grad in eine aktive Position schwenkt. Diese Schwelle stellt sicher, dass IscB nur auf stark passende Sequenzen reagiert und dadurch Nebenschnitte begrenzt.
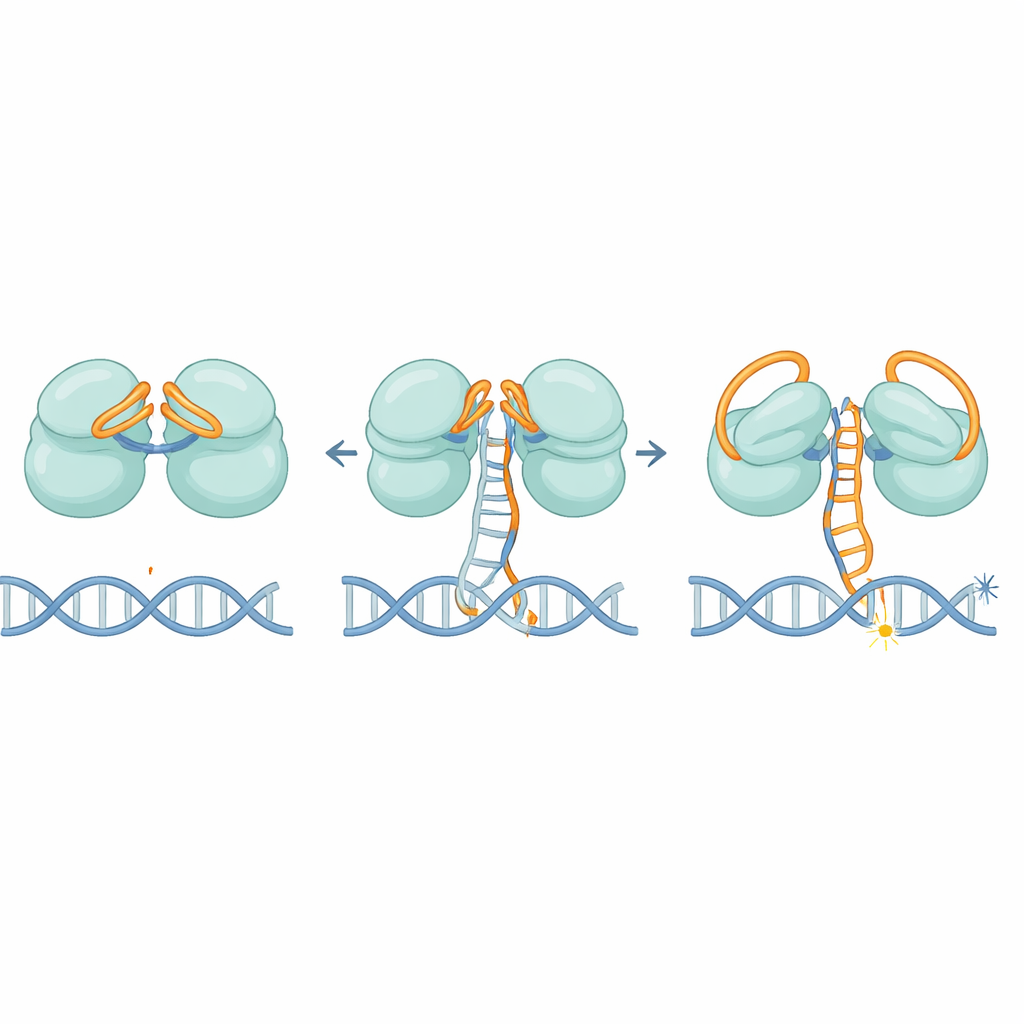
Wie IscB DNA aufklappt und stabil hält
Einmal aktiviert, muss IscB die beiden Stränge der DNA‑Doppelhelix trennen und sie lange genug auseinanderhalten, um zu schneiden. Die Autoren identifizieren eine kleine Schleife im Protein, die sich in die DNA zwängt und die Stränge in dem Bereich auseinanderdrängt, in dem RNA und DNA ein Hybridgerüst bilden. Positiv geladene Flächen entlang der Scharniere greifen dann den verdrängten Strang und stabilisieren diese blasenartige „R‑Schleife“. Mutationen, die diese Keilstruktur oder das geladene Band abschwächen, verringern die DNA‑Schneideaktivität stark und bestätigen, dass sie sowohl für das Aufklappen als auch für das Fixieren der DNA essenziell sind.
Scharniere feinjustieren, um bessere Editoren zu bauen
Da die Scharniere steuern, wie leicht die HNH‑Domäne in Aktion schwenken kann, prüften die Forscher, ob subtile Änderungen dort die Leistung verbessern könnten. Durch den Ersatz bestimmter sperriger Aminosäuren durch kleinere, flexiblere Residuen erzeugten sie IscB‑Varianten, deren Scharniere freier beweglich sind. In menschlichen Zellen zeigten zwei dieser konstruierten Varianten, genannt Hig1 und Hig2, deutlich höhere Editieraktivität. Eine Variante erreichte fast die Effizienz eines fortgeschrittenen Cas9‑Werkzeugs, verursachte dabei jedoch weniger unbeabsichtigte DNA‑Brüche im gesamten Genom, was darauf hindeutet, dass ein gezieltes Lockern dieser Scharniere IscB sowohl leistungsfähiger als auch präziser machen kann.
Warum das für zukünftige Gentherapien wichtig ist
Zusammen zeigen diese Befunde, wie ein kompakter Geneditierungsenzym sicher verriegelt bleiben kann, bis es auf eine fast perfekte DNA‑Übereinstimmung trifft, und sich dann schnell umstrukturieren kann, um an der richtigen Stelle zu schneiden. Indem jeder Schritt kartiert wird — von RNA‑Deckeln, die die Schnittzentren abschirmen, über die gaspedalähnliche Bewegung, die die Aktivierung auslöst, bis zu den Scharnieren, die den finalen Schnitt steuern — liefert die Arbeit eine Blaupause für die Entwicklung kleinerer, sichererer Genom‑Editoren. Solche Werkzeuge ließen sich leichter in medizinische Liefersysteme verpacken und könnten letztlich präzisere Behandlungen mit weniger Nebenwirkungen ermöglichen.
Zitation: Wang, F., Guo, R., Zhang, S. et al. Structural insight into IscB’s RNA-lid-based inactivation mechanism. Nat Struct Mol Biol 33, 603–614 (2026). https://doi.org/10.1038/s41594-026-01761-3
Schlüsselwörter: IscB, Genomeditierung, CRISPR, RNA-gesteuerte Nuklease, Strukturelle Biologie