Clear Sky Science · zh
UBQLN2 将蛋白毒性与神经退行性疾病中的脂质代谢联系起来
神经细胞如何耗尽能量
为何在肌萎缩侧索硬化(ALS)和额颞叶痴呆(FTD)等疾病中,某些神经细胞会死亡?这项研究表明,一种细胞内的“交通指挥官”蛋白将两个对神经元至关重要的任务联系起来:清除受损蛋白和管理脂肪与胆固醇。当这位“指挥官”出现故障时,神经细胞会以有害的方式燃烧其脂肪储备,丧失关键的膜构建成分,最终走向死亡。理解这种隐藏的能量危机,或能指向延长易损脑细胞存活时间的新方法。
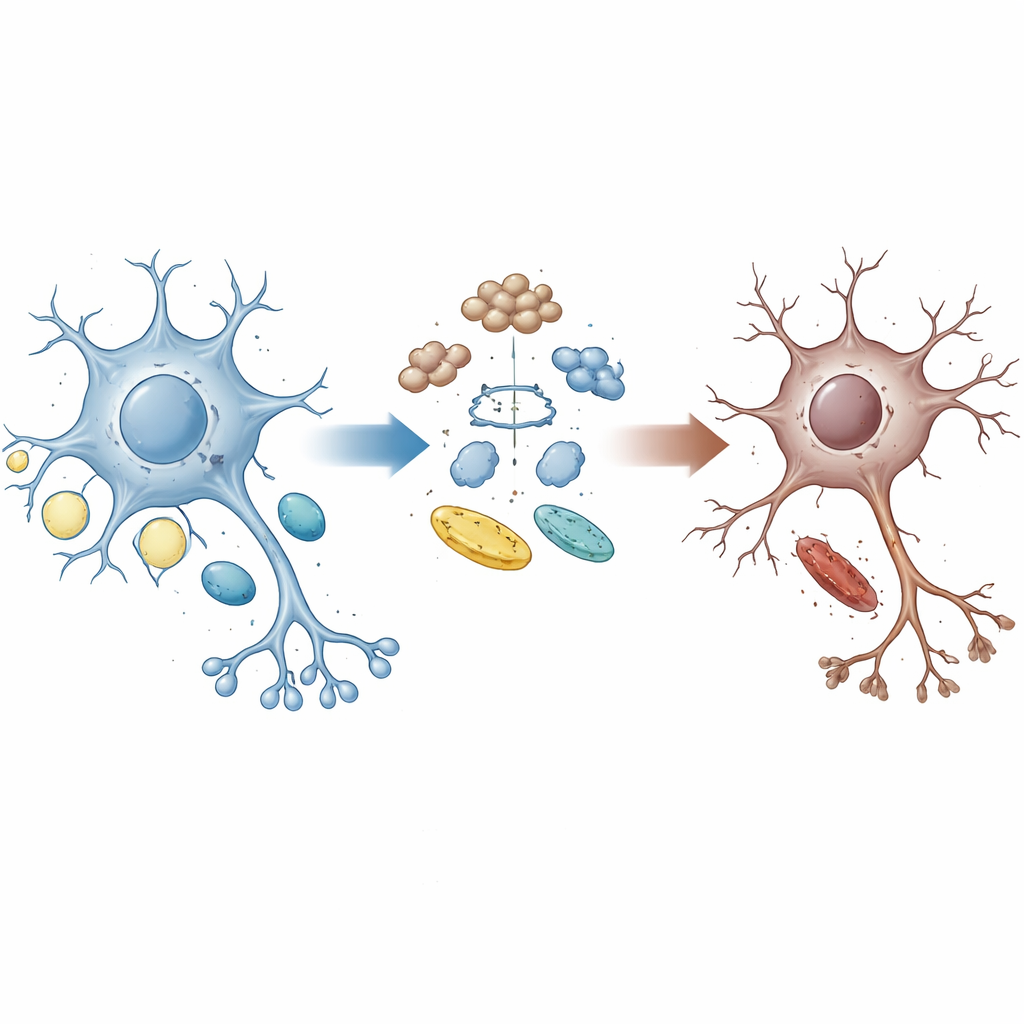
清除与能量之间的断裂环节
健康的脑细胞不断回收磨损的蛋白,并根据能量需要调整糖类和脂肪的利用。蛋白 UBQLN2 像一辆穿梭车,将受损或不需要的蛋白引导至细胞的降解机制。有家族携带特定 UBQLN2 突变会发生 ALS 和 FTD,这表明清除系统的失败可能助推疾病发展。作者使用携带患者样本 UBQLN2 突变的人源干细胞来源运动神经元、脑类器官和小鼠模型,研究该蛋白如何影响蛋白质质量控制与能量代谢之间的平衡。
当葡萄糖不足时,脂肪燃烧失控
由于 ALS 和 FTD 脑组织常显示葡萄糖利用不良,研究团队通过去除葡萄糖给运动神经元施加应激,迫使细胞更多依赖脂肪。结合蛋白质组学、脂质组学和 RNA 测序,他们发现 UBQLN2 突变放慢了数千种蛋白的周转,并显著改变了与代谢相关的通路。在能量应激下,突变神经元在线粒体中增强了长链脂肪酸氧化,并表现出脂滴——微小脂肪储备——与富含胆固醇的脂类显著减少。突触囊泡(在神经细胞间释放化学信号的小囊)变得脆弱,神经元存活率下降。补充适量胆固醇有助于恢复囊泡完整性并保护突变神经元和脑类器官,突出了胆固醇丧失为问题关键的一部分。
两种酶决定天平倾向
深入研究时,研究者询问 UBQLN2 通常控制哪些特定蛋白以维持脂质代谢的平衡。他们鉴定出两种酶——ILVBL 和 ALDH3A2,参与将某些脂类分子转化为可在线粒体中燃烧的形式。在健康细胞中,UBQLN2 与这些酶结合并在应激期间引导其被降解,从而限制脂肪过度进入线粒体。在 UBQLN2 突变的神经元中,ILVBL 和 ALDH3A2 停留时间更长,并在脂滴与线粒体的接触部位积累。这推动了过度的脂肪燃烧,激活了抑制胆固醇生成的能量感应通路,耗尽了维持稳健神经膜与突触所需的脂类。
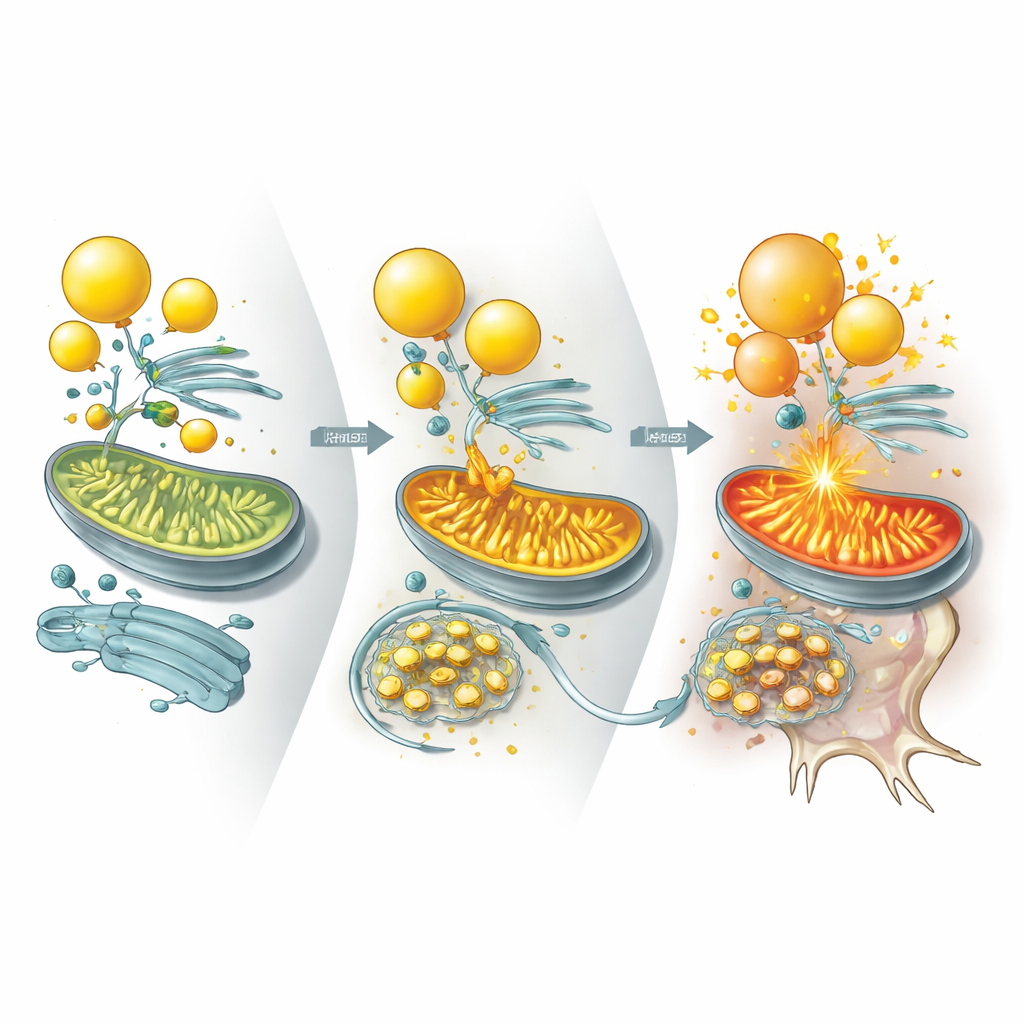
来自迷你大脑、小鼠与患者组织的证据
这一模式在多种系统中重复出现。UBQLN2 突变的脑类器官在能量应激下形成更少的脂滴并出现更多神经元死亡,这一现象同样可通过补充胆固醇得到缓解。在工程化表达疾病相关 UBQLN2 变体的小鼠中,神经元积累了 ILVBL 和 ALDH3A2,丧失脂滴并发生退化,导致运动与记忆障碍。重要的是,在这些小鼠中降低 ILVBL 或 ALDH3A2 水平可恢复脂质储备,改善神经元存活并部分挽救运动功能。作者还检查了携带 TDP‑43 蛋白聚集的散发性 ALS 患者的脊髓组织。在这些样本中,UBQLN2 被困于 TDP‑43 包涵体中,ILVBL 与 ALDH3A2 堆积,脂滴被耗尽,与胆固醇相关的脂类减少——与实验模型相呼应。
将恶性循环转为靶向方向
对非专业读者而言,关键信息是某些形式的 ALS 与 FTD 不仅反映有毒蛋白团块,还反映神经元燃料与膜结构经济的缓慢崩溃。UBQLN2 通常将脂质处理酶拴在短链上,使脂肪燃烧成为支持而非破坏细胞健康的过程。当 UBQLN2 突变或被 TDP‑43 聚集体 sequestrate(俘获)时,这些酶失去控制,脂滴缩小、胆固醇生成下降、突触减弱——形成以神经退行性为终点的恶性循环。通过明确 UBQLN2–ILVBL/ALDH3A2 轴,并表明降低这些酶活性或恢复胆固醇可发挥保护作用,该研究为减缓或预防 ALS、FTD 及相关疾病中的神经细胞丧失开辟了新的治疗思路。
引用: Liu, Y., Huang, Z., Hsu, YW. et al. UBQLN2 links proteotoxicity with lipid metabolism in neurodegeneration. Nat Neurosci 29, 782–795 (2026). https://doi.org/10.1038/s41593-026-02226-y
关键词: ALS, 额颞叶痴呆, 脂质代谢, 蛋白质稳态, 神经退行性疾病