Clear Sky Science · ru
UBQLN2 связывает протеотоксичность с липидным метаболизмом при нейродегенерации
Как нервные клетки остаются без топлива
Почему одни нервные клетки погибают при таких заболеваниях, как боковой амиотрофический склероз (БАС) и лобно‑височная деменция (ЛВД)? В этом исследовании показано, что один клеточный «регулировщик движения» связывает две жизненно важные функции нейронов: утилизацию повреждённых белков и управление жирами и холестерином. Когда этот регулятор выходит из строя, нервные клетки вредоносно расходуют свои жировые запасы, теряют ключевые строительные компоненты мембран и в конечном счёте погибают. Понимание этого скрытого энергетического кризиса может указать пути для продления жизни уязвимых клеток мозга.
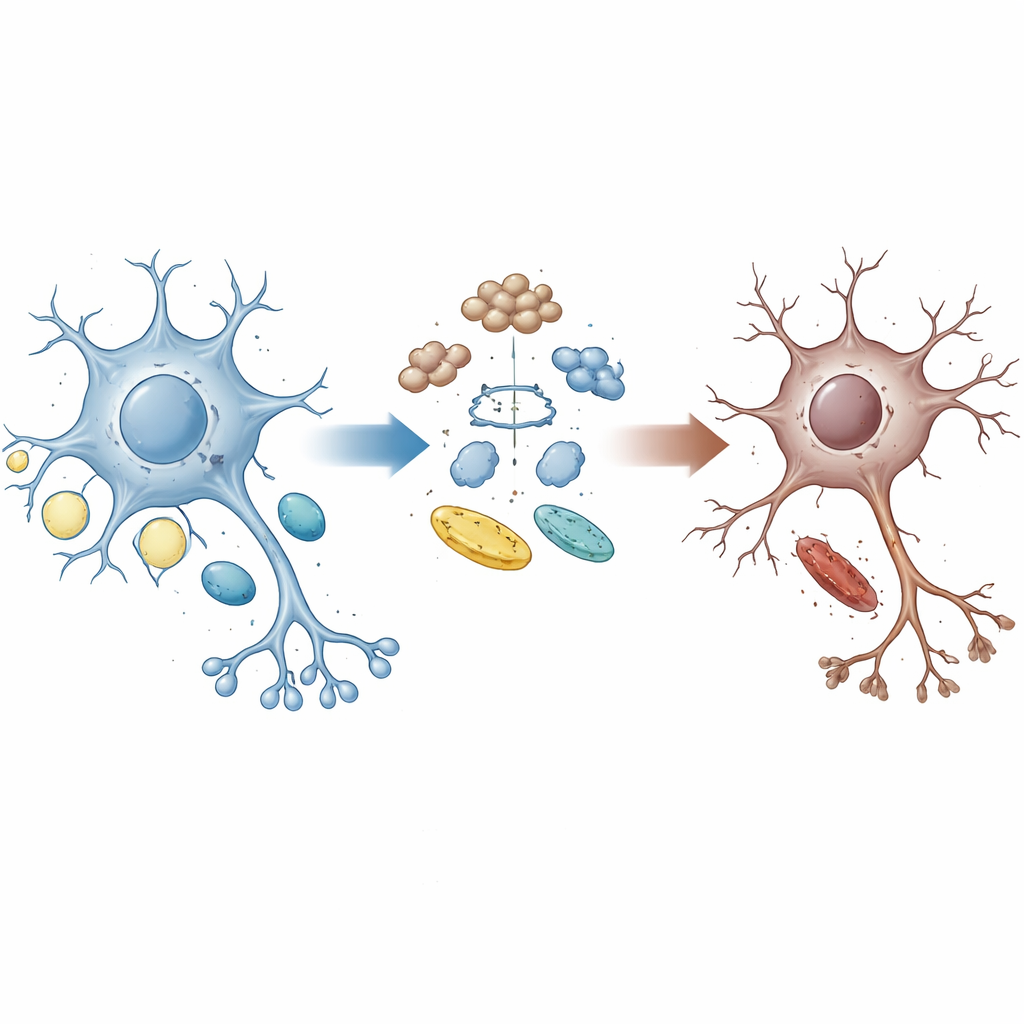
Разорванная связь между уборкой и энергией
Здоровые клетки мозга постоянно утилизируют изношенные белки и подстраивают использование сахаров и жиров под свои энергетические потребности. Белок UBQLN2 действует как «шаттл», направляющий повреждённые или ненужные белки к механизмам утилизации клетки. У семей с определёнными мутациями UBQLN2 развиваются БАС и ЛВД, что указывает на то, что сбои в этой системе очистки могут способствовать болезни. Авторы использовали моторные нейроны, полученные из человеческих стволовых клеток с пациентоподобными мутациями UBQLN2, а также мозговые органоиды и мышиные модели, чтобы выяснить, как этот белок управляет балансом между контролем качества белков и энергетическим обменом.
Когда глюкоза иссякает, сжигание жира выходит из‑под контроля
Поскольку в мозге при БАС и ЛВД часто наблюдается плохое использование глюкозы, команда подвергла моторные нейроны стрессу, убрав глюкозу и заставив клетки больше полагаться на жиры. С помощью сочетания протеомики, липидомики и РНК‑секвенирования они обнаружили, что мутации UBQLN2 замедляют оборот тысяч белков и существенно меняют метаболические пути. При энергетическом стрессе мутантные нейроны усиливали окисление длинноцепочечных жирных кислот в митохондриях и демонстрировали заметную потерю липидных капель — крошечных резервуаров жира — и липидов, богатых холестерином. Синаптические везикулы, маленькие мешочки, выпускающие химические сигналы между нервными клетками, становились хрупкими, а выживаемость нейронов падала. Добавление умеренных количеств холестерина помогало восстановить целостность везикул и защитить мутантные нейроны и органоиды, подчёркивая потерю холестерина как ключевой компонент проблемы.
Две ферменты переключают баланс
Углубляясь, исследователи выясняли, какие конкретные белки UBQLN2 обычно контролирует, чтобы сдерживать липидный метаболизм. Они идентифицировали две ферменты, ILVBL и ALDH3A2, которые помогают превращать определённые молекулы жиров в формы, готовые к окислению в митохондриях. В здоровых клетках UBQLN2 связывается с этими ферментами и направляет их на деградацию, особенно при стрессе, ограничивая чрезмерную подачу жиров в митохондрии. В нейронах с мутантным UBQLN2 ILVBL и ALDH3A2 задерживаются дольше и накапливаются в местах контакта между липидными каплями и митохондриями. Это приводит к избыточному сжиганию жира, активации энергетического сенсорного пути, подавляющего синтез холестерина, и истощению липидов, необходимых для поддержания прочных мембран и синапсов нейронов.
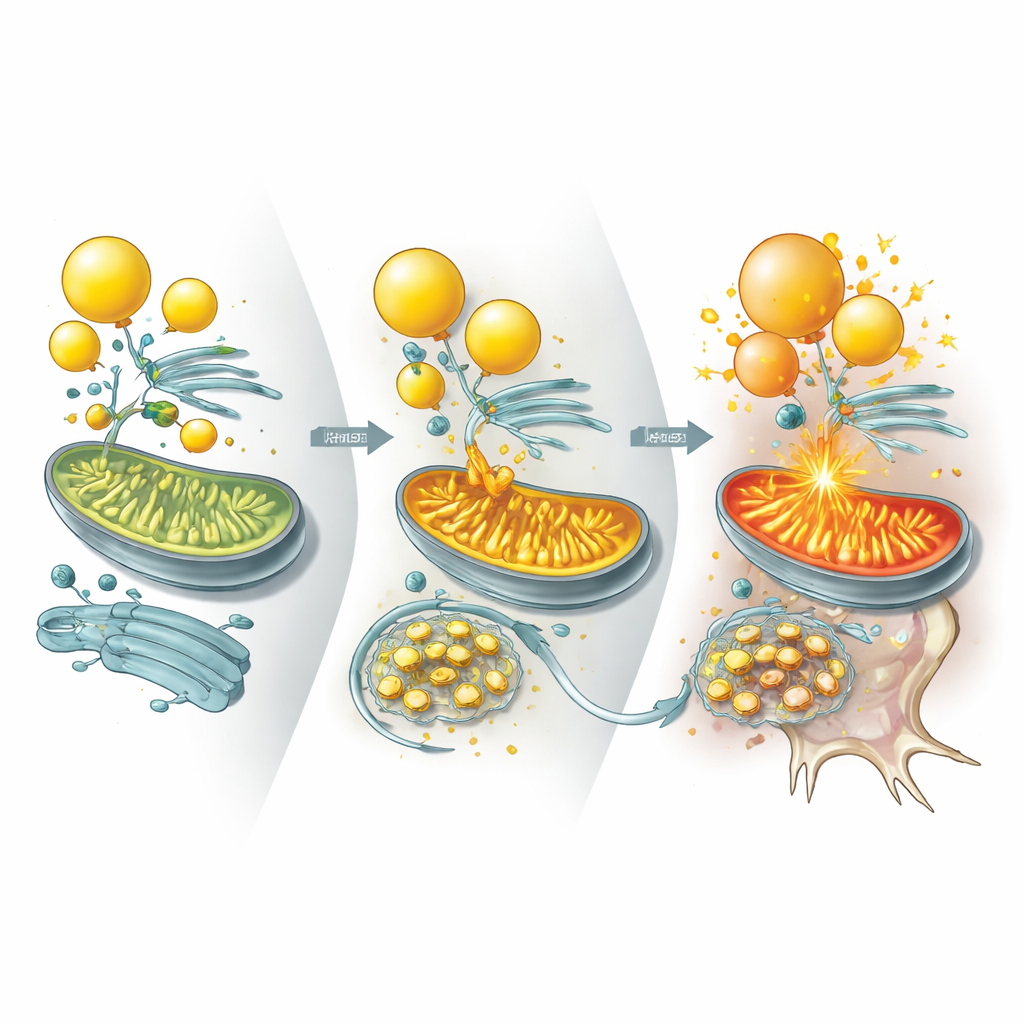
Данные из мини‑мозгов, мышей и тканей пациентов
Та же картина проявлялась в разных системах. У мозговых органоидов с мутантным UBQLN2 образовывалось меньше липидных капель и при энергетическом стрессе наблюдалась большая гибель нейронов, что вновь можно было смягчить добавлением холестерина. У мышей, генетически модифицированных для экспрессии варианта UBQLN2, связанного с болезнью, нейроны накапливали ILVBL и ALDH3A2, теряли липидные капли и дегенерировали, что приводило к нарушениям моторики и памяти. Важно, что снижение уровней ILVBL или ALDH3A2 у этих мышей восстанавливало запасы липидов, улучшало выживаемость нейронов и частично возвращало подвижность. Авторы также изучали спинномозговую ткань людей с спорадическим БАС, отмеченным агрегатами белка TDP‑43. В этих образцах UBQLN2 оказался захвачен в TDP‑43‑включениях, ILVBL и ALDH3A2 накапливались, липидные капли истощались, а липиды, связанные с холестерином, были уменьшены — что отражает экспериментальные модели.
Превращение порочного круга в терапевтическую мишень
Для неспециалистов ключевая мысль в том, что некоторые формы БАС и ЛВД отражают не только токсические белковые сгустки, но и постепенный крах энергетической и мембранной экономики нейрона. UBQLN2 обычно держит ферменты обработки липидов на коротком поводке, чтобы сжигание жира поддерживало, а не подрывало здоровье клетки. Когда UBQLN2 мутирован или захвачен агрегатами TDP‑43, эти ферменты работают без контроля, липидные капли сокращаются, производство холестерина падает, и синапсы ослабевают — порочный круг, приводящий к нейродегенерации. Указав на ось UBQLN2–ILVBL/ALDH3A2 и показав, что либо подавление этих ферментов, либо восстановление холестерина может быть защитным, исследование открывает новые терапевтические направления для замедления или предотвращения потери нервных клеток при БАС, ЛВД и родственных заболеваниях.
Цитирование: Liu, Y., Huang, Z., Hsu, YW. et al. UBQLN2 links proteotoxicity with lipid metabolism in neurodegeneration. Nat Neurosci 29, 782–795 (2026). https://doi.org/10.1038/s41593-026-02226-y
Ключевые слова: БАС, лобно‑височная деменция, липидный метаболизм, гомеостаз белков, нейродегенерация