Clear Sky Science · nl
UBQLN2 brengt proteotoxiciteit in verband met vetstoffwisseling bij neurodegeneratie
Hoe zenuwcellen zonder brandstof komen te zitten
Waarom sterven sommige zenuwcellen in aandoeningen zoals amyotrofische laterale sclerose (ALS) en frontotemporale dementie (FTD)? Deze studie laat zien dat één cellulair "verkeersagent"-eiwit twee cruciale taken in onze neuronen met elkaar verbindt: het opruimen van beschadigde eiwitten en het beheer van vetten en cholesterol. Wanneer deze verkeersagent faalt, verbranden zenuwcellen hun vetreserves op schadelijke wijze, verliezen ze belangrijke membraanbouwstenen en sterven ze uiteindelijk. Inzicht in deze verborgen energiecrisis kan wijzen op nieuwe manieren om kwetsbare hersencellen langer in leven te houden.
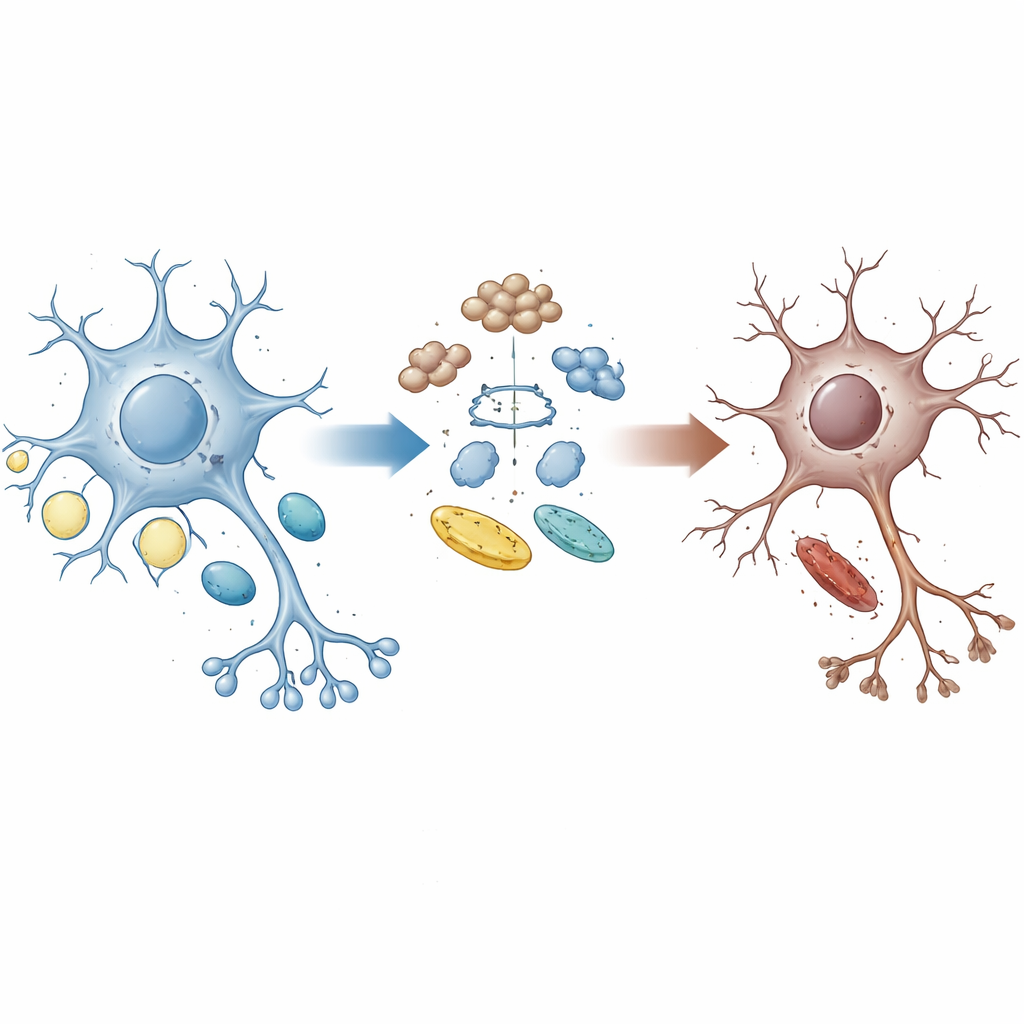
Een verbroken schakel tussen opruimen en energie
Gezonde hersencellen recyclen voortdurend versleten eiwitten en passen hun gebruik van suikers en vetten aan om aan hun energiebehoefte te voldoen. Het eiwit UBQLN2 fungeert als een pendel die beschadigde of overbodige eiwitten naar het cellulaire afvalmachinerie begeleidt. Families met bepaalde UBQLN2-mutaties kunnen ALS en FTD ontwikkelen, wat suggereert dat fouten in dit opruimsysteem de ziekte kunnen aansturen. De auteurs gebruikten uit menselijke stamcellen afgeleide motorneuronen met patiëntachtige UBQLN2-mutaties, samen met hersenorganoïden en muismodellen, om te onderzoeken hoe dit eiwit het evenwicht tussen eiwitkwaliteitscontrole en energiemetabolisme bepaalt.
Als glucose opraakt, ontspoort vetverbranding
Aangezien bij ALS- en FTD-hersenen vaak een slecht glucosengebruik wordt gezien, zetten de onderzoekers hun motorneuronen onder stress door glucose te verwijderen, waardoor de cellen meer op vetten moesten vertrouwen. Met een combinatie van proteomica, lipidomica en RNA-sequencing vonden ze dat UBQLN2-mutaties de turnover van duizenden eiwitten vertragen en sterk de routes beïnvloeden die gerelateerd zijn aan metabolisme. Bij energiestress verhoogden de gemuteerde neuronen de oxidatie van langeketenvetzuren in mitochondriën en vertoonden ze een duidelijke afname van lipidedruppels—kleine vetreserves—en cholesterolrijke lipiden. Synaptische blaasjes, de kleine zakjes die chemische signalen tussen zenuwcellen vrijgeven, werden fragiel en het overleven van neuronen daalde. Het toevoegen van bescheiden hoeveelheden cholesterol hielp de integriteit van blaasjes te herstellen en beschermde gemuteerde neuronen en hersenorganoïden, wat het verlies van cholesterol als een kernprobleem benadrukt.
Twee enzymen kantelen het evenwicht
Dieper gravend vroegen de onderzoekers welke specifieke eiwitten UBQLN2 normaal reguleert om de vetstoffwisseling in toom te houden. Ze identificeerden twee enzymen, ILVBL en ALDH3A2, die helpen bepaalde vetmoleculen om te zetten in vormen die gereed zijn om in mitochondriën verbrand te worden. In gezonde cellen bindt UBQLN2 deze enzymen en stuurt ze naar degradatie, vooral tijdens stress, waardoor wordt beperkt hoe agressief vetten de mitochondriën binnenstromen. In UBQLN2-gemuteerde neuronen blijven ILVBL en ALDH3A2 echter veel langer aanwezig en hopen ze zich op op contactplaatsen tussen lipidedruppels en mitochondriën. Dit drijft overmatige vetverbranding aan, activeert een energiesensor-pad dat de cholesterolproductie dempt, en put de lipiden uit die nodig zijn om robuuste neuronale membranen en synapsen te onderhouden.
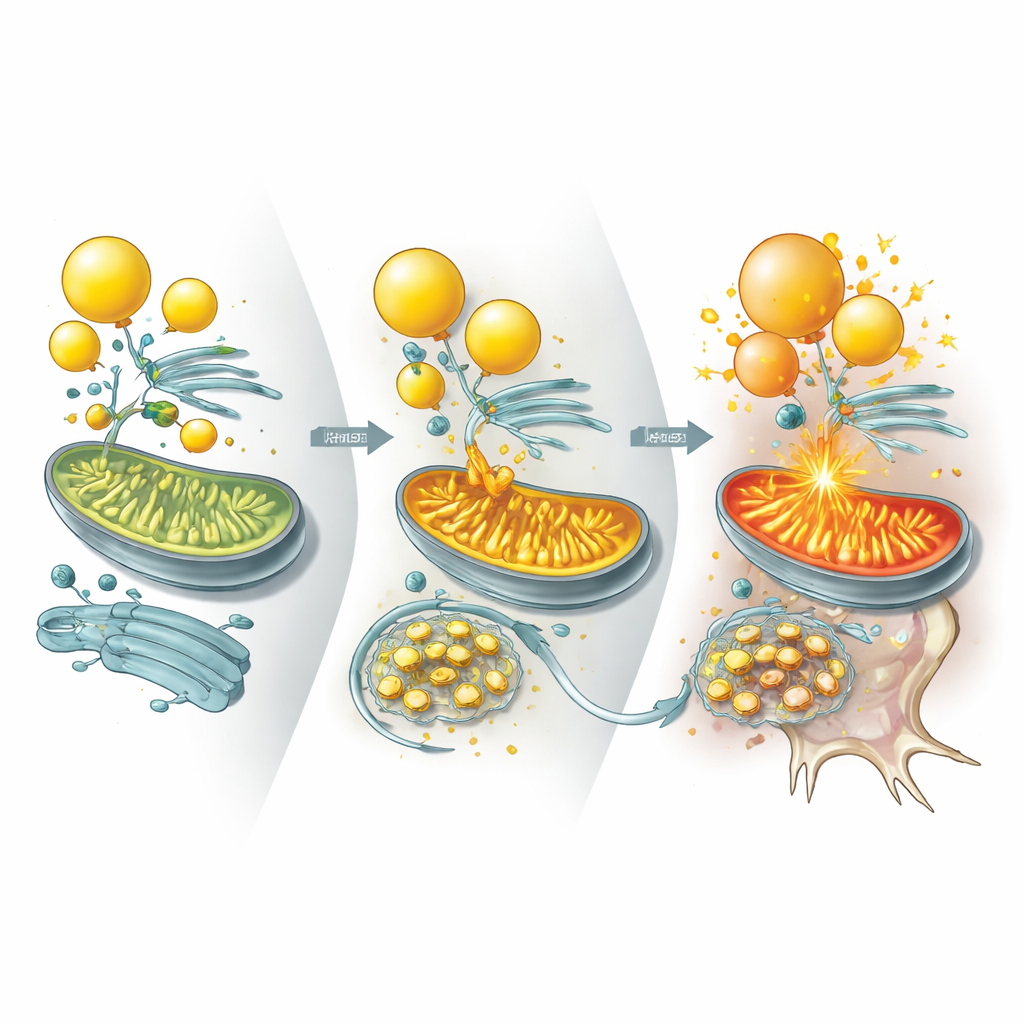
Bewijs uit mini-hersenen, muizen en patiëntweefsels
Hetzelfde patroon kwam naar voren in meerdere systemen. UBQLN2-gemuteerde hersenorganoïden ontwikkelden minder lipidedruppels en toonden meer neuronale sterfte onder energiestress, wat opnieuw verlicht kon worden door cholesteroltoevoeging. In muizen die zo waren geconstrueerd dat ze een ziektegerelateerde UBQLN2-variant tot expressie brachten, hopen neuronen ILVBL en ALDH3A2 op, verloren ze lipidedruppels en degenereren ze, wat leidde tot motorische en geheugenproblemen. Belangrijk is dat het verlagen van ILVBL- of ALDH3A2-niveaus in deze muizen de vetvoorraden herstelde, het overleven van neuronen verbeterde en de beweging gedeeltelijk redde. De auteurs onderzochten ook menselijk ruggenmergweefsel van patiënten met sporadische ALS gekenmerkt door TDP-43-eiwitaggregaten. In deze monsters zat UBQLN2 gevangen in TDP-43-inclusies, stapelden ILVBL en ALDH3A2 zich op, waren lipidedruppels uitgeput en waren cholesterolgerelateerde lipiden verminderd—een weerspiegeling van de experimentele modellen.
Een vicieuze cirkel aanpakken als therapeutisch doel
Voor niet-specialisten is de kernboodschap dat sommige vormen van ALS en FTD mogelijk niet alleen toxische eiwitklonten weerspiegelen, maar ook een langzaam instorten van de brandstof- en membraaneconomie van de neuron. UBQLN2 houdt normaal gesproken vetverwerkende enzymen kort zodat vetverbranding de celgezondheid ondersteunt in plaats van saboteert. Wanneer UBQLN2 gemuteerd is of wordt opgeslokt door TDP-43-aggregaten, lopen deze enzymen onbeheerst door, krimpen lipidedruppels, daalt de cholesterolproductie en verzwakken synapsen—een vicieuze cirkel die eindigt in neurodegeneratie. Door deze UBQLN2–ILVBL/ALDH3A2-as te identificeren en te laten zien dat het verlagen van deze enzymen of het herstellen van cholesterol beschermend kan zijn, opent de studie nieuwe therapeutische invalshoeken om het verlies van zenuwcellen bij ALS, FTD en verwante ziekten te vertragen of te voorkomen.
Bronvermelding: Liu, Y., Huang, Z., Hsu, YW. et al. UBQLN2 links proteotoxicity with lipid metabolism in neurodegeneration. Nat Neurosci 29, 782–795 (2026). https://doi.org/10.1038/s41593-026-02226-y
Trefwoorden: ALS, frontotemporale dementie, vetstoffwisseling, eiwit-homeostase, neurodegeneratie