Clear Sky Science · tr
UBQLN2 proteotoksisiteyi nörodejenerasyonda lipid metabolizmasıyla ilişkilendiriyor
Sinir Hücreleri Yakıtın Nasıl Tükeniyor
Amyotrofik lateral skleroz (ALS) ve frontotemporal demans (FTD) gibi hastalıklarda neden bazı sinir hücreleri ölür? Bu çalışma, tek bir hücresel “trafik polisi” proteininin nöronlarımız içinde iki hayati işlemi — hasarlı proteinlerin temizlenmesini ve yağ ile kolesterol yönetimini — birbirine bağlamaya yardımcı olduğunu gösteriyor. Bu trafik polisi bozulduğunda, sinir hücreleri yağ depolarını zararlı bir şekilde yakıyor, önemli zar yapıcı bileşenleri kaybediyor ve sonunda ölüyor. Bu gizli enerji krizinin anlaşılması, hassas beyin hücrelerini daha uzun süre canlı tutmaya yönelik yeni yolların işaretçisi olabilir.
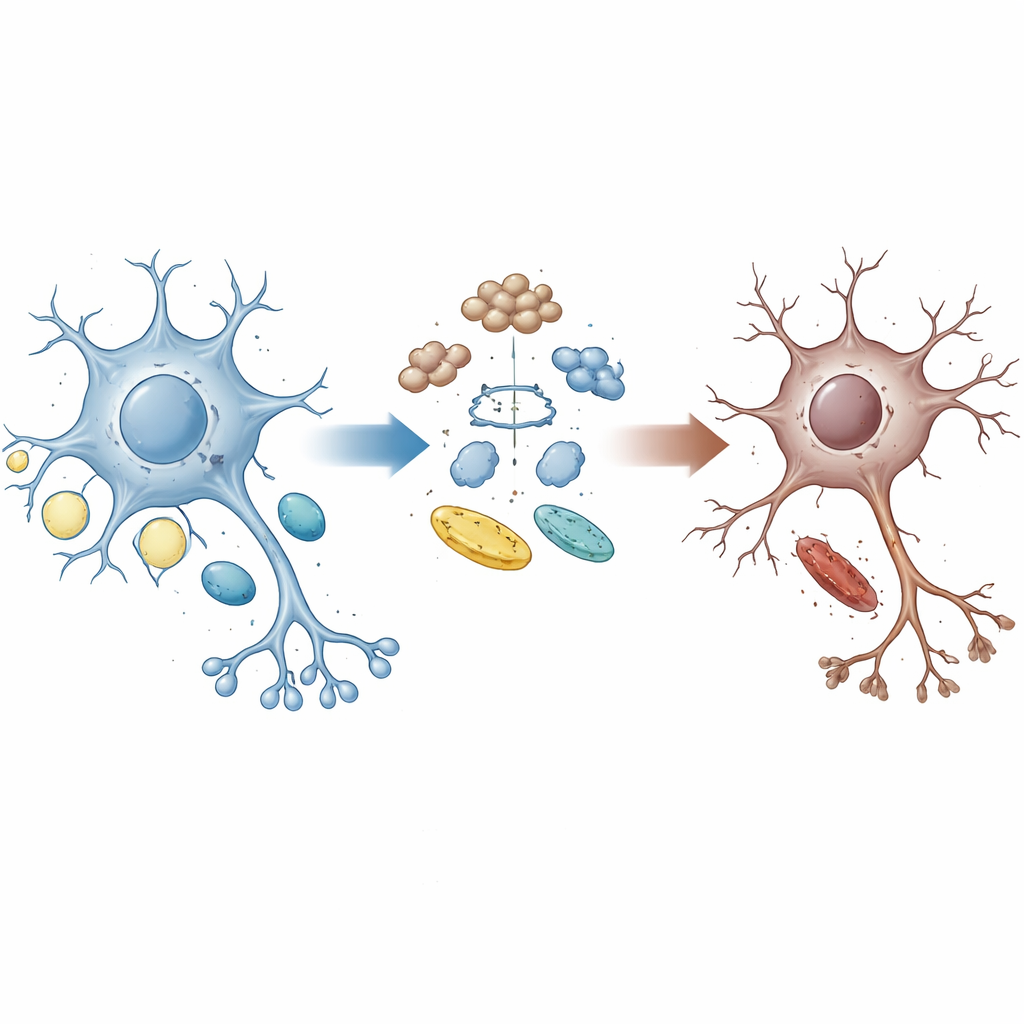
Temizlik ile Enerji Arasındaki Kırık Bağ
Sağlıklı beyin hücreleri sürekli olarak yıpranan proteinleri geri dönüştürür ve enerji ihtiyaçlarını karşılamak için şeker ile yağ kullanımını ayarlar. UBQLN2 proteini, hasarlı veya gereksiz proteinleri hücrenin imha makinelerine yönlendiren bir taşıyıcı görevi görür. Belirli UBQLN2 mutasyonlarına sahip ailelerde ALS ve FTD gelişebiliyor; bu da bu temizlik sistemindeki aksaklıkların hastalığı tetiklemiş olabileceğini düşündürüyor. Yazarlar, bu proteinin protein kalite kontrolü ile enerji metabolizması arasındaki dengeyi nasıl şekillendirdiğini görmek için hasta benzeri UBQLN2 mutasyonları taşıyan insan kök hücre kaynaklı motor nöronlar, beyin organoidleri ve fare modelleri kullandılar.
Glukoz Azalınca Yağ Yakımı Kontrolden Çıkıyor
ALS ve FTD beyinlerinde genellikle glukoz kullanımında bozukluk görüldüğü için ekip, motor nöronlarını glukozu ortamdan kaldırarak strese soktu ve hücreleri daha çok yağlara dayanmak zorunda bıraktı. Proteomik, lipidomik ve RNA dizilemenin kombinasyonunu kullanarak, UBQLN2 mutasyonlarının binlerce proteinin dönüşüm hızını yavaşlattığını ve metabolizmayla ilgili yolları güçlü biçimde değiştirdiğini buldular. Enerji stresi altında, mutan nöronlar mitokondride uzun zincirli yağ asidi oksidasyonunu artırdı ve küçük yağ rezervleri olan lipid damlacıklarında ile kolesterolden zengin lipitlerde belirgin kayıp gösterdi. Sinaptik veziküller — sinir hücreleri arasındaki kimyasal sinyalleri salan küçük kesecikler — kırılgan hale geldi ve nöron sağkalımı düştü. Mütevazı miktarda kolesterol eklemek, vezikül bütünlüğünü yeniden sağlamaya ve mutan nöronları ile beyin organoidlerini korumaya yardımcı oldu; bu da kolesterol kaybının sorunun kilit bir parçası olduğunu vurguladı.
İki Enzim Dengeyi Değiştiriyor
Daha derine inerek araştırmacılar, UBQLN2’nin lipid metabolizmasını kontrol altında tutmak için normalde hangi spesifik proteinleri denetlediğini sordular. Mitokondride yakılmaya hazır formlara dönüştürmeye yardım eden ILVBL ve ALDH3A2 adlı iki enzimi tanımladılar. Sağlıklı hücrelerde UBQLN2 bu enzimlere bağlanır ve özellikle stres sırasında bunları degradasyona yönlendirerek yağların mitokondrilere çok agresif biçimde verilmesini sınırlar. Ancak UBQLN2‑mutant nöronlarda ILVBL ve ALDH3A2 çok daha uzun süre kalıyor ve lipid damlacıkları ile mitokondri arasındaki temas bölgelerinde birikiyordu. Bu durum aşırı yağ yakımını tetikliyor, kolesterol üretimini baskılayan bir enerji algılama yolunu aktive ediyor ve sağlam nöronal zarlar ile sinapsları sürdürmek için gereken lipidleri tüketiyordu.
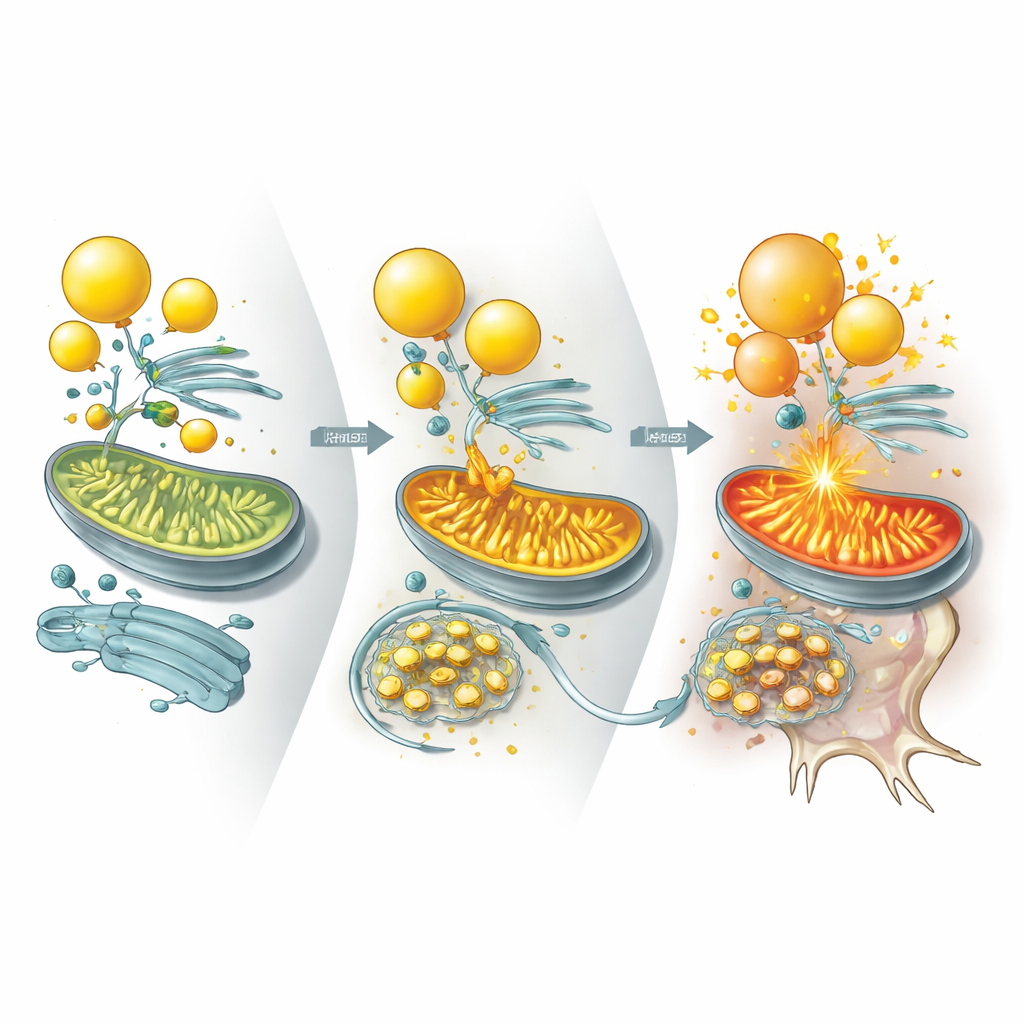
Mini‑Beyinler, Fareler ve Hasta Dokularından Kanıt
Aynı desen birden çok sistemde ortaya çıktı. UBQLN2‑mutant beyin organoidleri enerji stresi altında daha az lipid damlacığı geliştirdi ve daha fazla nöron ölümü gösterdi; bu durum yeniden kolesterol takviyesi ile hafifletilebildi. Hastalıkla ilişkili bir UBQLN2 varyantını eksprese edecek şekilde tasarlanmış farelerde nöronlar ILVBL ve ALDH3A2 biriktirdi, lipid damlacıklarını kaybetti ve dejenerasyon görüldü; bunun sonucunda motor ve hafıza sorunları gelişti. Önemli olarak, bu farelerde ILVBL veya ALDH3A2 düzeylerini düşürmek lipid depolarını geri getirdi, nöron sağkalımını iyileştirdi ve hareketi kısmen kurtardı. Yazarlar ayrıca TDP‑43 protein kümeleriyle işaretli sporadik ALS’li hastalardan alınmış insan omurilik dokusunu incelediler. Bu örneklerde UBQLN2 TDP‑43 inklüzyonlarında sıkışmış, ILVBL ve ALDH3A2 birikmiş, lipid damlacıkları tükenmiş ve kolesterolle ilişkili lipitler azalmıştı — deneysel modelleri yansıtan bulgular.
Kötü Döngüyü Hedefe Çevirmek
Uzman olmayanlar için ana mesaj, bazı ALS ve FTD formlarının yalnızca toksik protein kümelerinden ibaret olmayıp aynı zamanda nöronun yakıt ve zar ekonomisinin yavaş çöküşünü de yansıtabileceğidir. UBQLN2 normalde lipid işlemleyici enzimleri kısa bir tasma üzerinde tutar, böylece yağ yakımı hücre sağlığını destekler, sabote etmez. UBQLN2 mutasyona uğradığında veya TDP‑43 kümeleri tarafından hapsedildiğinde bu enzimler kontrolsüz çalışır, lipid damlacıkları küçülür, kolesterol üretimi düşer ve sinapslar zayıflar — nörodejenerasyonla sonuçlanan bir kısır döngü. UBQLN2–ILVBL/ALDH3A2 eksenini belirleyerek ve bu enzimlerin azaltılmasının ya da kolesterolün yeniden sağlanmasının koruyucu olabileceğini göstererek çalışma, ALS, FTD ve ilişkili hastalıklarda sinir hücresi kaybını yavaşlatmaya veya önlemeye yönelik yeni tedavi yaklaşımlarına kapı aralıyor.
Atıf: Liu, Y., Huang, Z., Hsu, YW. et al. UBQLN2 links proteotoxicity with lipid metabolism in neurodegeneration. Nat Neurosci 29, 782–795 (2026). https://doi.org/10.1038/s41593-026-02226-y
Anahtar kelimeler: ALS, frontotemporal demans, lipid metabolizması, protein homeostazı, nörodejenerasyon