Clear Sky Science · he
UBQLN2 מקשר בין רעילות חלבונית לתמטול שומנים בניורודגנרציה
כיצד תאי עצב מסיימים את המאמץ
מדוע כמה תאי עצב מתים במחלות כמו טרשת נוירונים מוטורית על שם לוא גריג (ALS) ודמנציה פרונטו‑טמפורטלית (FTD)? המחקר הזה מראה כי חלבון יחיד שעובד כ"שוטר תנועה" בתוך התא מקשר בין שתי משימות חיוניות בתאים שלנו: סילוק חלבונים פגומים וניהול של שומנים וכלורוסטרול. כאשר אותו שוטר התנועה מתקלקל, תאי עצב שורפים את מאגרי השומן שלהם באופן מזיק, מאבדים רכיבים מרכזיים לבניית ממברנות ובסופו של דבר מתים. הבנה של משבר האנרגיה החבוי הזה יכולה להצביע על דרכים חדשות לשמור על תאי מוח פגיעים חיים לאורך זמן רב יותר.
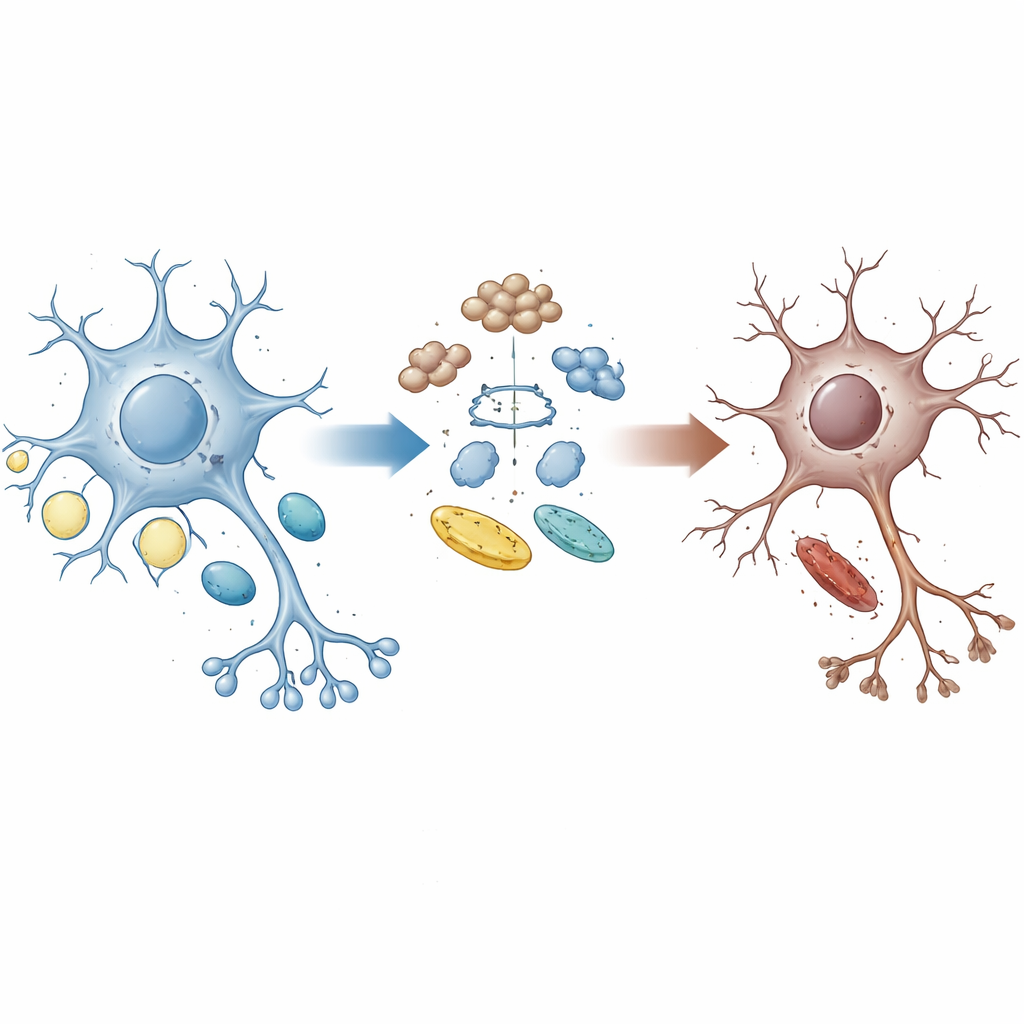
קשר שבור בין ניקיון לאנרגיה
תאי מוח בריאים ממחזרים כל העת חלבונים בלויים ומתאימים את השימוש בסוכרים ושומנים כדי לענות על צרכי האנרגיה שלהם. החלבון UBQLN2 מתפקד כשאטל שמנחה חלבונים פגומים או מיותרים אל מכניזם ההשמדה של התא. משפחות עם מוטציות מסוימות ב‑UBQLN2 עלולות לפתח ALS ו‑FTD, מה שמרמז כי כשלים במערכת הניקיון הזו עשויים לתרום למחלה. החוקרים השתמשו בניורונים מוטוריים נגזרים מתאים גזע אנושיים הנושאים מוטציות דומות לאלו של חולים, יחד עם אורגאיד (מיני‑מוח) ועכברים, כדי לבחון כיצד חלבון זה מעצב את האיזון בין בקרה על איכות חלבונים לבין מטבוליזם אנרגטי.
כשגלוקוז נחלש, שריפת שומנים יוצאת משליטה
מכיוון שבמוחי חולי ALS ו‑FTD בדרך כלל יש שימוש לקוי בגלוקוז, הצוות לחץ על נוירוניהם על‑ידי הסרת גלוקוז, וכפה על התאים להסתמך יותר על שומנים. בשילוב של פרוטאומיקה, ליפידומיקה וריצוף RNA הם מצאו שמוטציות ב‑UBQLN2 מאטות את מחזור החיים של אלפי חלבונים ומשנות בחוזקה מסלולים הקשורים למטבוליזם. תחת מאמץ אנרגטי, נוירונים מוטנטים הגבירו את חמצון חומצות השומן ארוכות‑שרשרת במיטוכונדריה והראו אובדן משמעותי של טיפות שומן—מאגרי שומן זעירים—ושומנים עשירים כלורוסטרול. וזיקולות סינפטיות, השקיות הקטנות שמשחררות איתותים כימיים בין תאי עצב, הפכו לשבריריות והישרדות הנוירונים ירדה. הוספה של כמויות מתונות של כלורוסטרול סייעה לשחזר את שלמות הוזיקולות והגנה על הנוירונים המוטנטים והאורגאידים, ודגשה את אובדן הכלורוסטרול כחלק מרכזי בבעיה.
שני אנזימים מזיזים את האיזון
בהעמקה, החוקרים שאלו אילו חלבונים ספציפיים UBQLN2 בדרך כלל שולט בהם כדי לרסן את מטבוליזם השומנים. הם זיהו שני אנזימים, ILVBL ו‑ALDH3A2, המסייעים להמיר מולקולות שומן מסוימות לצורות המוכנות להישרף במיטוכונדריה. בתאים בריאים UBQLN2 נקשר לאנזימים אלה ומנחה אותם לעבר פירוק, במיוחד בזמן סטרס, ומגביל עד כמה שומנים מוזנים למיטוכונדריה. בנוירונים מוטנטיים עם UBQLN2, לעומת זאת, ILVBL ו‑ALDH3A2 נשארים זמן רב יותר ומצטברים באתרים של מגע בין טיפות השומן למיטוכונדריה. זה מדרבן שריפת שומן מופרזת, מפעיל מסלול חישה של אנרגיה שמדכא ייצור כלורוסטרול ומייבש את השומנים הדרושים לתחזוקת ממברנות וסינפסות חזקות של הנוירון.
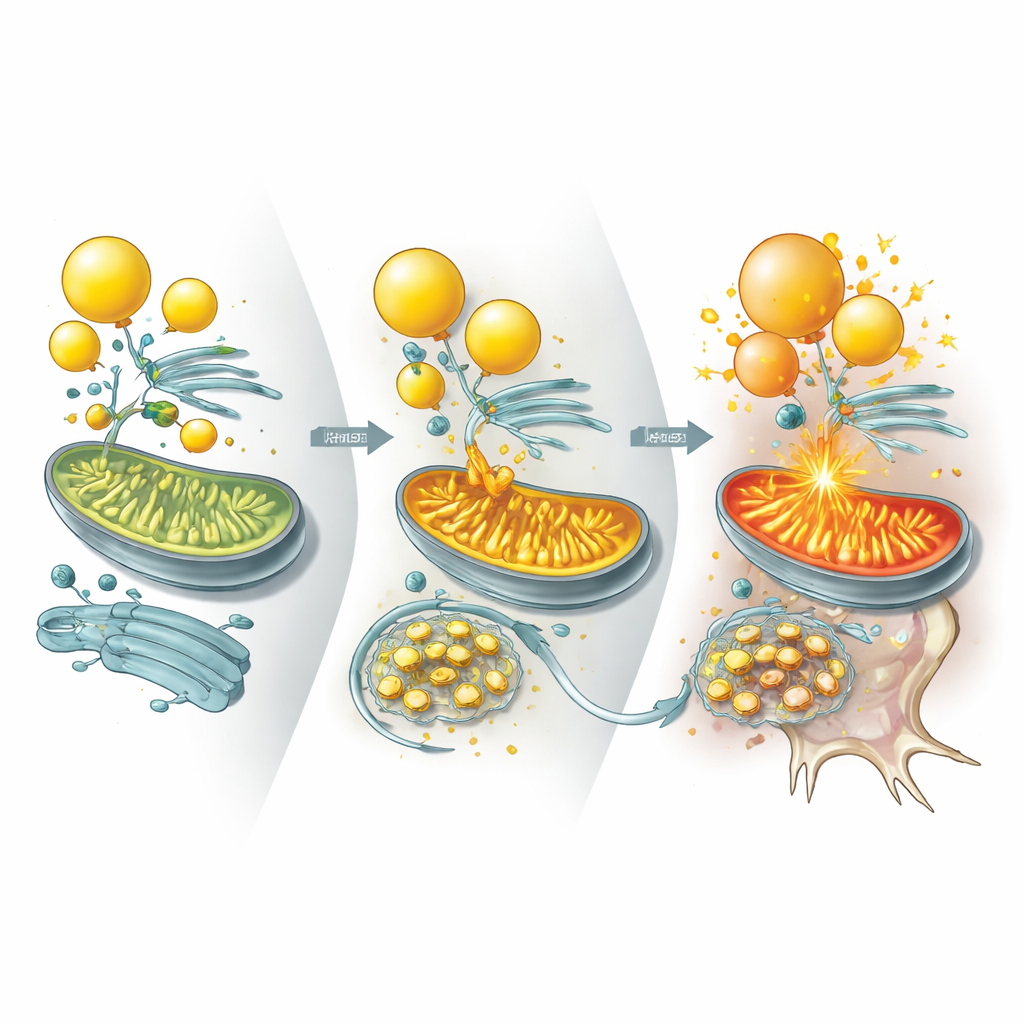
ראיות ממיני‑מוח, עכברים ורקמות חולים
אותו דפוס הופיע במערכות מרובות. אורגאידים מוחיים עם מוטציות ב‑UBQLN2 פיתחו פחות טיפות שומן והראו יותר מוות נוירוני תחת סטרס אנרגטי, שניתן היה להקל עליו שוב בתוספת כלורוסטרול. בעכברים מהונדסים לבטא וריאנט UBQLN2 הקשור למחלה, נוירונים צברו ILVBL ו‑ALDH3A2, איבדו טיפות שומן ודגרדו, מה שהוביל לבעיות מוטוריות וזכרון. באופן חשוב, הורדת רמות ILVBL או ALDH3A2 בעכברים אלה שיחזרה מאגרי שומן, שיפרה הישרדות נוירונים והצילה חלקית תפקוד תנועה. המחברים גם בחנו רקמות חוט השדרה אנושיות של חולים עם ALS ספונטני המסומן באגרגטים של חלבון TDP‑43. בדגימות אלה, UBQLN2 הוגרר לתוך כלוליות TDP‑43, ILVBL ו‑ALDH3A2 הצטברו, טיפות השומן התרוקנו ושומנים הקשורים לכלורוסטרול הופחתו—מה שמשקף את המודלים הניסויים.
להפוך מעגל רע לתכלית טיפולית
ללא‑מומחים, המסר המרכזי הוא שבצורות מסוימות של ALS ו‑FTD הבעיה אינה רק צמתי חלבון רעילים אלא גם קריסה איטית של כלכלת הדלק והממברנה של הנוירון. UBQLN2 בדרך כלל שומר על אנזימי עיבוד השומנים על רצועה קצרה כך ששריפת שומן תתמוך בבריאות התא במקום לסבית אותה. כאשר UBQLN2 מוטנטי או נלכד על‑ידי אגרגטים של TDP‑43, אנזימים אלה פועלים ללא בקרה, טיפות השומן מצטמקות, ייצור הכלורוסטרול יורד והסינפסות נחלשות—מעגל רע שמסתיים בניורודגנרציה. על‑ידי זיהוי ציר ה‑UBQLN2–ILVBL/ALDH3A2 והדגמה כי או דיכוי של אנזימים אלה או שיקום הכלורוסטרול יכול להגן, המחקר פותח כיווני טיפול חדשים להאטה או מניעה של אובדן תאי עצב ב‑ALS, FTD ומחלות קרובות.
ציטוט: Liu, Y., Huang, Z., Hsu, YW. et al. UBQLN2 links proteotoxicity with lipid metabolism in neurodegeneration. Nat Neurosci 29, 782–795 (2026). https://doi.org/10.1038/s41593-026-02226-y
מילות מפתח: אימוטורופית לטרלית (ALS), דמנציה פרונטו‑טמפורטלית, מטבוליזם שומנים, הומיאוסטזיס של חלבונים, ניורודגנרציה