Clear Sky Science · zh
TGF-β介导的先天抗病毒反应和SIV储存库大小的表观遗传控制
这项研究对艾滋病患者的重要性
即便有如今强效的抗HIV药物,一小部分病毒仍会静默地藏在免疫细胞内,一旦停药就可能重新点燃感染。本研究在猕猴体内探讨了一种通过重新训练机体第一道防线——先天免疫系统——来缩减这一隐匿储存库的新方法,而不仅仅聚焦于传统的抗病毒T细胞和抗体。该研究也有助于解释为什么少数被称为“精英控制者”的人能在不服药的情况下控制HIV。
免疫细胞内的拉锯战
研究者以一个重要的临床问题为出发点:当抗逆转录病毒治疗暂停时,HIV通常会从那些寿命较长的被感染细胞中回弹。先前的工作表明,联合两种阻断免疫抑制分子IL-10和PD-1的抗体药物,能帮助大多数被感染的猕猴控制病毒回弹,其中一部分动物甚至表现出其CD4 T细胞内隐匿病毒DNA量明显下降。本文的研究团队询问了那些储存库缩小的动物与储存库保持较大动物之间的区别,重点考察了淋巴结和血液中先天免疫细胞与辅助T细胞的行为及其“编程”。
唤醒机体的天然抗病毒警报
通过广泛的基因活性谱与单细胞分析,科学家们发现储存库缩小的动物在治疗中断前就已启动了强大的抗病毒回路。通常由干扰素触发的基因——机体的抗病毒报警分子——在多种免疫细胞类型中高度活跃,包括单核细胞、树突状细胞以及多类T细胞亚群。这些基因编码的“限制因子”在病毒生命周期的不同阶段阻断病毒。用人类CD4 T细胞的体外实验显示,干扰素预处理不仅使直接暴露的细胞更抗感染,其邻近细胞也变得更难被HIV侵染,强调了被激活的先天免疫如何在病毒重新出现时保护旁观细胞。
一条镇静信号如何产生反效果
形成鲜明对比的是,那些病毒储存库依然很大的动物血液中TGF-β这种免疫抑制分子水平较高。详尽的通路分析将TGF-β与SMAD蛋白的激活及一系列酶,尤其是某些组蛋白去乙酰化酶(HDACs),联系起来,这些酶促使细胞内DNA包装更加紧密。这种表观遗传上的紧缩使得关键的抗病毒基因更难被访问和激活。当人类记忆性CD4 T细胞暴露于富含TGF-β的血浆或TGF-β本身时,它们上调了HDAC11,对干扰素信号的响应变差,并在体外更容易被HIV感染。阻断TGF-β或抑制HDAC可逆转这些效应,重新开放对抗病毒基因的访问并降低感染率。
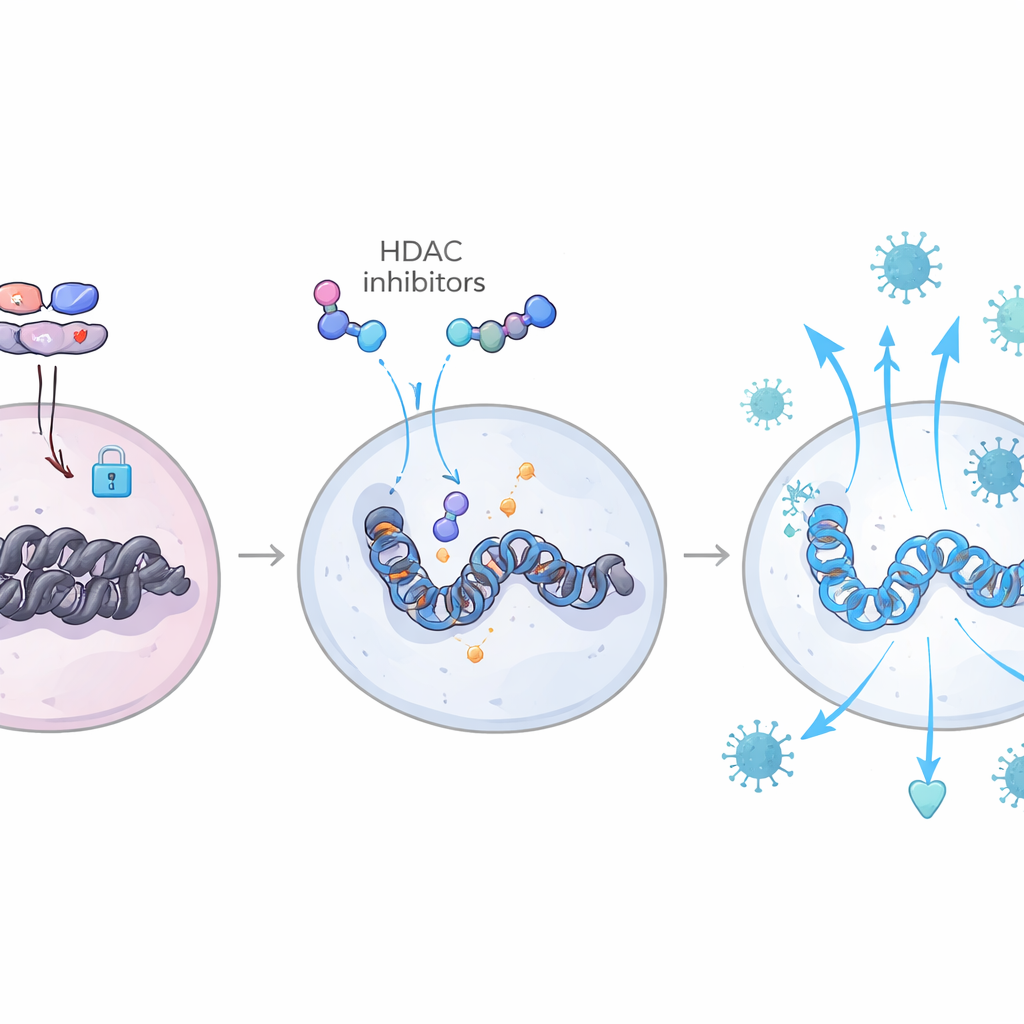
通过表观遗传重写免疫“剧本”
通过将基因活性测量与单细胞染色质开放性图谱相结合,研究团队可以在基因组层面直接看到这些拉锯力量。在储存库缩小的动物中,干扰素相关转录因子(如IRF和STAT家族)的结合位点在T细胞和髓系细胞中更易接近,而与TGF-β相关的AP-1和SMAD复合体使用的结合位点则相对关闭。这些动物还显示出涉及IL-6和转录因子C/EBP-β的通路活性增强,该通路进一步放大干扰素反应并有助于将TGF-β维持在受抑制的非活性形式。共同作用下,这创造了一种持久的“训练性”抗病毒状态,在停药时限制了新的感染循环。重要的是,许多相同的基因特征也出现在人类HIV精英控制者的血细胞中,将猕猴的发现与一种自然发生的病毒控制形式联系起来。
这对未来HIV治愈策略的意义
对非专业读者来说,主要信息是隐匿的HIV储存库大小并非固定不变——它受先天免疫细胞在DNA包装层面如何被“接线”的强烈影响。当TGF-β占主导时,它招募表观遗传酶锁住抗病毒基因,使细胞变得脆弱,储存库得以存续。当干扰素驱动的程序和IL-6介导的放大机制占优时,许多潜在靶细胞变得更难被感染,储存库随之缩小。鉴于阻断PD-1和HDAC的药物,以及增强干扰素通路的制剂已在癌症和其他领域存在,这些结果指向了可能的组合疗法路径:重新编程先天免疫、抑制TGF-β的免疫抑制影响,并逐步侵蚀HIV在机体内的最后堡垒。
引用: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
关键词: HIV储存库, 先天免疫, 干扰素信号, TGF-beta, 表观遗传重编程