Clear Sky Science · pt
TGF-β media o controle epigenético das respostas antivirais inatas e o tamanho do reservatório de SIV
Por que esta pesquisa importa para pessoas vivendo com HIV
Mesmo com os medicamentos antirretrovirais potentes de hoje, um pequeno reservatório de vírus permanece oculto silenciosamente dentro de células do sistema imune e pode reativar a infecção se o tratamento for interrompido. Este estudo em macacos rhesus explora uma nova forma de reduzir esse reservatório oculto, reconfigurando a primeira linha de defesa do corpo — o sistema imune inato — em vez de focar apenas nas células T e anticorpos clássicos que combatem vírus. O trabalho também ajuda a explicar por que uma pequena fração de pessoas, conhecidas como controladores de elite, consegue manter o HIV sob controle sem remédios.
Uma disputa dentro das células imunes
Os pesquisadores partiram de um problema clínico importante: quando a terapia antirretroviral é interrompida, o HIV geralmente ressurge a partir de células infectadas de longa duração. Trabalhos anteriores mostraram que combinar dois anticorpos que bloqueiam os freios imunes IL-10 e PD-1 ajudou a maioria dos macacos infectados a controlar a reemergência viral, e um subconjunto mostrou até uma queda marcada na quantidade de DNA viral escondido em suas células T CD4. Neste artigo, a equipe investigou o que distinguiu os animais cujos reservatórios encolheram daqueles cujos reservatórios permaneceram grandes, focando no comportamento e na “programação” de células imunes inatas e células T helper em gânglios linfáticos e sangue.
Ativando o alarme antiviral natural do corpo
Usando perfis amplos de atividade gênica e análise em célula única, os cientistas descobriram que os animais com reservatórios em redução haviam ligado circuitos antivirais potentes bem antes da interrupção da terapia. Genes tipicamente ativados por interferons — as moléculas de alarme antiviral do corpo — estavam muito ativos em muitos tipos de células imunes, incluindo monócitos, células dendríticas e múltiplos subconjuntos de células T. Esses genes codificam “fatores de restrição” que bloqueiam vírus em diferentes etapas do seu ciclo de vida. Experimentos de laboratório com células CD4 humanas mostraram que o pré-tratamento com interferon tornava tanto as células diretamente expostas quanto suas vizinhas muito mais resistentes à infecção por HIV, ressaltando como uma resposta inata primada pode proteger células ao redor quando o vírus reaparece.
Como um sinal de acalmia pode sair pela culatra
Em nítido contraste, os animais cujos reservatórios virais permaneceram grandes apresentavam altos níveis sanguíneos da molécula imunossupressora TGF-β. Análises detalhadas de vias ligaram TGF-β à ativação de proteínas SMAD e a um conjunto de enzimas, especialmente certas histona deacetilases (HDACs), que apertam a compactação do DNA dentro das células. Esse fechamento epigenético tornou mais difícil o acesso e a ativação de genes antivirais-chave. Quando células CD4 de memória humanas foram expostas a plasma rico em TGF-β, ou ao próprio TGF-β, aumentaram a expressão de HDAC11, ficaram piores em responder a sinais de interferon e foram mais facilmente infectadas pelo HIV in vitro. Bloquear TGF-β ou inibir HDACs reverteu esses efeitos, reabrindo o acesso a genes antivirais e reduzindo a infecção.
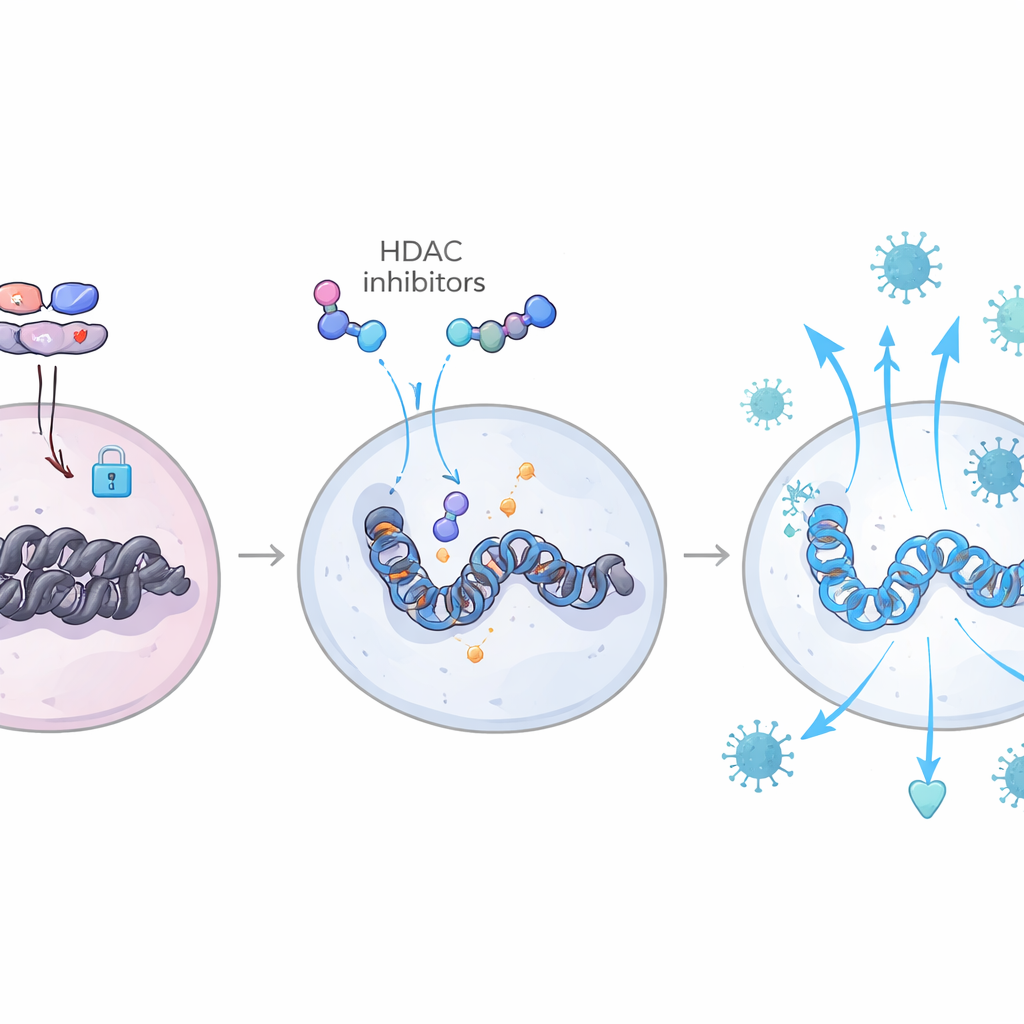
Reescrevendo o manual imune via epigenética
Ao combinar medidas de atividade gênica com mapas de abertura da cromatina em células individuais, a equipe pôde observar essas forças em disputa diretamente no genoma. Em animais com reservatórios em redução, sítios de ligação para fatores de transcrição ligados a interferon, como as famílias IRF e STAT, estavam mais acessíveis em células T e células mieloides, enquanto sítios de ligação usados por complexos associados a TGF-β — AP-1 e SMAD — estavam relativamente fechados. Esses animais também mostraram aumento da atividade de uma via envolvendo IL-6 e o fator C/EBP-β, que amplifica ainda mais as respostas a interferon e ajuda a manter o TGF-β em uma forma contida e inativa. Juntas, essas mudanças criaram um estado antiviral duradouro e “treinado” que limitou novas rodadas de infecção quando os medicamentos foram suspensos. Importante, muitas das mesmas assinaturas gênicas apareceram em células sanguíneas de controladores de elite humanos com HIV, ligando as descobertas nos macacos a uma forma natural de controle viral.
O que isso significa para estratégias futuras de cura do HIV
Para um não especialista, a mensagem principal é que o tamanho do reservatório oculto de HIV não é fixo — ele é fortemente influenciado por como as células imunes inatas são organizadas ao nível do empacotamento do DNA. Quando o TGF-β domina, ele recruta enzimas epigenéticas que trancam genes antivirais, deixando as células vulneráveis e permitindo que o reservatório viral persista. Quando programas dirigidos por interferon e a amplificação mediada por IL-6 prevalecem, muitas células potenciais-alvo tornam-se mais difíceis de infectar e o reservatório diminui. Como já existem drogas que bloqueiam PD-1 e HDACs, e agentes que estimulam vias de interferon em câncer e outras áreas, esses resultados apontam para terapias combinadas que poderiam reprogramar a imunidade inata, reduzir a influência supressora do TGF-β e, gradualmente, erodir os últimos redutos do HIV no corpo.
Citação: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Palavras-chave: Reservatório de HIV, imunidade inata, sinalização de interferon, TGF-beta, reprogramação epigenética