Clear Sky Science · sv
TGF-β medierar epigenetisk kontroll av medfödda antivirala svar och SIV-reservoarens storlek
Varför denna forskning är viktig för personer som lever med hiv
Även med dagens kraftfulla hivläkemedel finns en liten pool virus som gömmer sig tyst inne i immunceller och som kan återuppväcka infektion om behandlingen avbryts. Denna studie hos rhesusmakaker undersöker ett nytt sätt att minska den dolda reservoaren genom att ominstruera kroppens första försvarslinje — det medfödda immunsystemet — snarare än att enbart fokusera på de klassiska virusbekämpande T‑cellerna och antikropparna. Arbetet hjälper också till att förklara varför en liten grupp människor, kända som elite controllers, kan hålla hiv i schack utan läkemedel.
Dragkamp inne i immuncellerna
Forskarna utgick från ett viktigt kliniskt problem: när antiretroviral terapi pausas återkommer hiv normalt från långlivade infekterade celler. Tidigare arbeten visade att kombinationen av två antikroppsläkemedel som blockerar immunsuppressionen IL‑10 och PD‑1 hjälpte de flesta infekterade makaker att kontrollera virusåterkomst, och en del visade även en markant minskning av mängden viral DNA som gömdes i deras CD4‑T‑celler. I denna artikel undersökte teamet vad som skilde de djur vars reservoarer krympte från dem vars reservoarer förblev stora, med fokus på beteendet och ”programmeringen” av medfödda immunceller och hjälpar‑T‑celler i lymfnoder och blod.
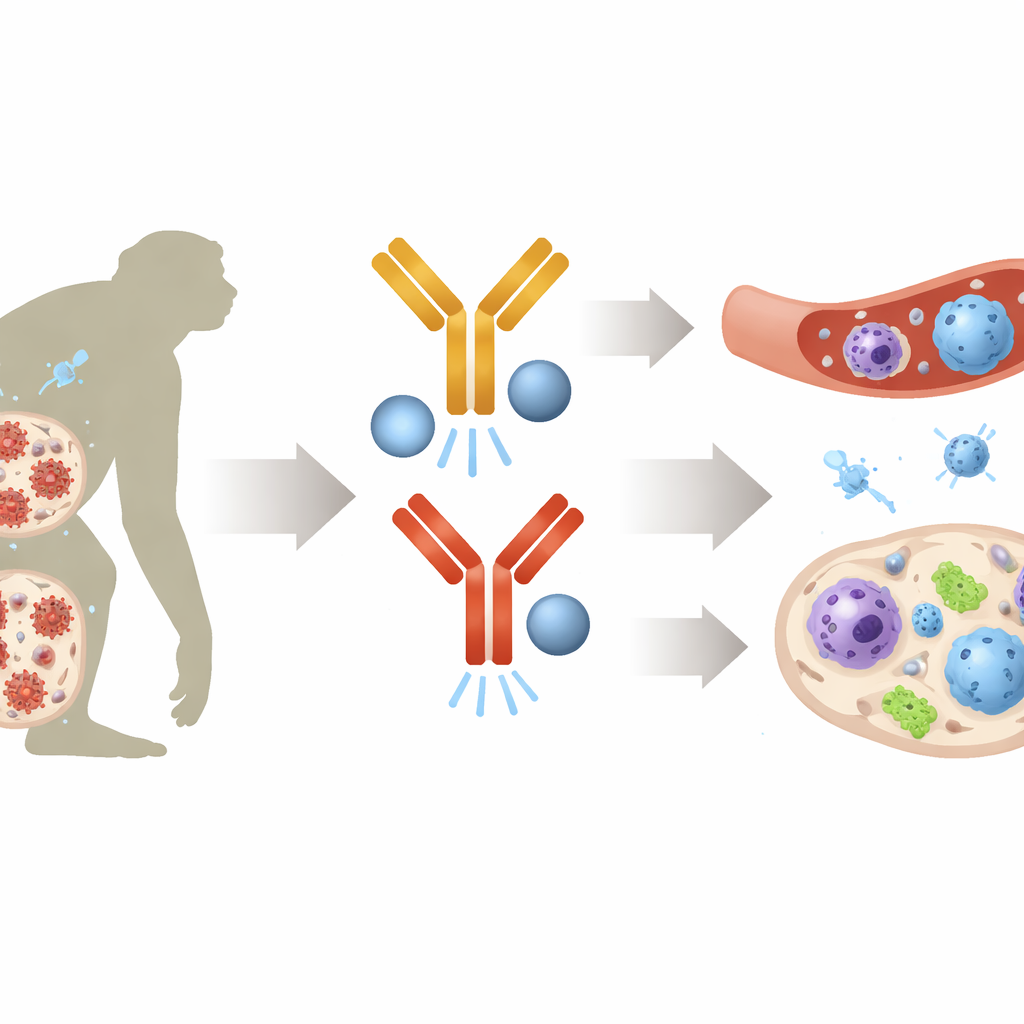
Att skruva upp kroppens naturliga antivirala alarm
Genom bred profilering av genaktivitet och analys på enskilda celler fann forskarna att djur med krympande reservoarer hade aktiverat kraftfulla antivirala kretsar långt innan behandlingen avbröts. Gener som vanligtvis triggas av interferoner — kroppens antivirala larmmolekyler — var mycket aktiva i många immuncelltyper, inklusive monocyter, dendritiska celler och flera T‑cellsundergrupper. Dessa gener kodar för ”restriktionsfaktorer” som blockerar virus i olika steg av deras livscykel. Laboratorieexperiment med humana CD4‑T‑celler visade att förbehandling med interferon gjorde både direkt utsatta celler och deras grannar mycket mer resistenta mot hivinfektion, vilket understryker hur ett förberett medfött svar kan skydda intilliggande celler när viruset återkommer.
Hur en dämpande signal kan slå tillbaka
I skarp kontrast hade djur vars virala reservoarer förblev stora höga blodnivåer av den immundämpande molekylen TGF‑β. Detaljerad vägandsanalys kopplade TGF‑β till aktivering av SMAD‑proteiner och en rad enzymer, särskilt vissa histondeacetylaser (HDACs), som stramar åt DNA‑packningen inuti cellerna. Denna epigenetiska åtstramning gjorde viktiga antivirala gener svårare att komma åt och att aktivera. När humana minnes‑CD4‑T‑celler exponerades för plasma rikt på TGF‑β, eller för TGF‑β i sig, ökade de uttrycket av HDAC11, blev sämre på att svara på interferonsignaler och infekterades lättare av hiv in vitro. Blockering av TGF‑β eller hämning av HDACs vände dessa effekter, öppnade åter tillgången till antivirala gener och minskade infektion.
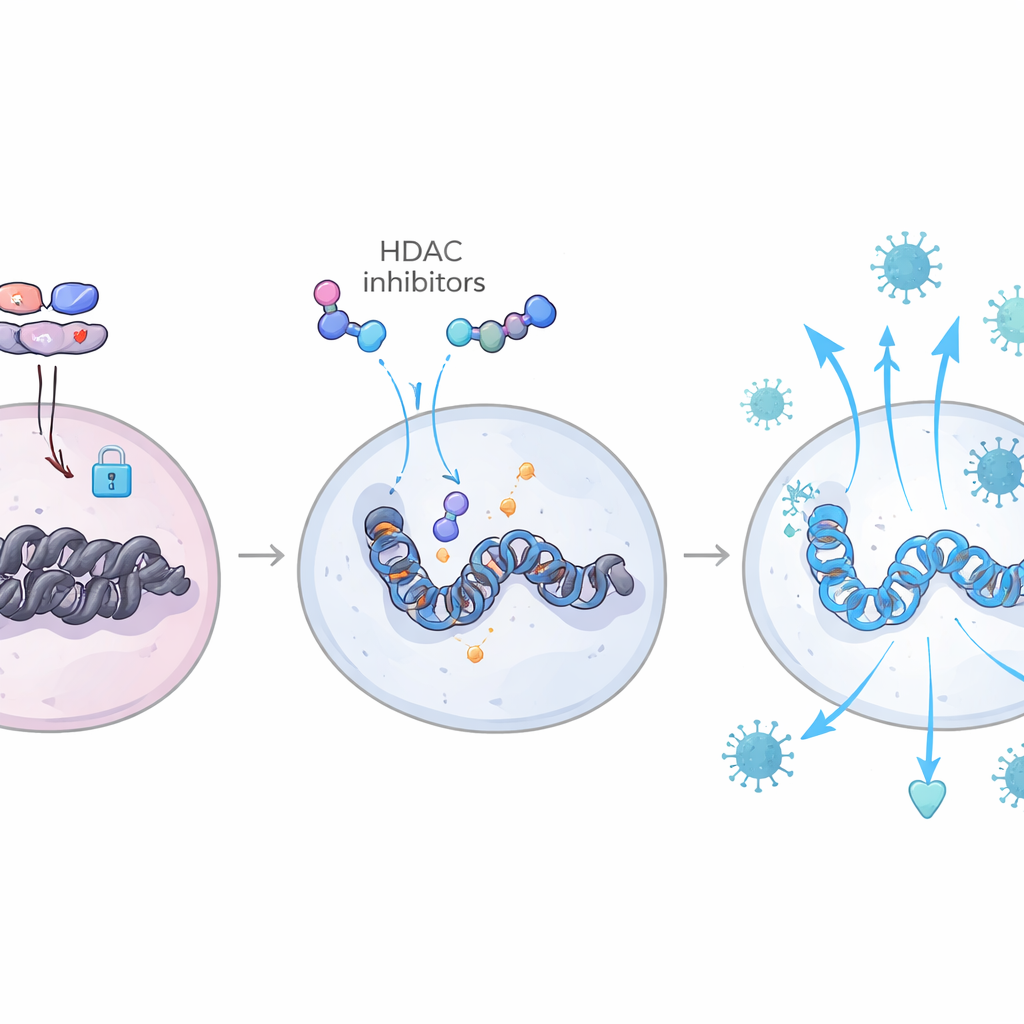
Ominskrivning av immunsystemets spelbok via epigenetik
Genom att kombinera mätningar av genaktivitet med kartor över kromatinöppenhet i enskilda celler kunde teamet se dessa dragkampskrafter direkt i genomet. Hos djur med krympande reservoarer var bindningsställen för interferon‑kopplade transkriptionsfaktorer som IRF‑ och STAT‑familjerna mer åtkomliga över T‑celler och myeloida celler, medan bindningsställen som används av TGF‑β‑associerade AP‑1‑ och SMAD‑komplex var relativt stängda. Dessa djur visade också ökad aktivitet i en väg som involverar IL‑6 och faktorn C/EBP‑β, vilket ytterligare förstärker interferonsvar och hjälper till att hålla TGF‑β i en begränsad, inaktiv form. Tillsammans skapade detta ett varaktigt, ”tränat” antiviralt tillstånd som begränsade nya infektionsomgångar när läkemedel stoppades. Viktigt är att många av samma genprofiler också framträdde i blodceller från mänskliga hiv‑elite controllers, vilket knyter makakstudierna till en naturligt förekommande form av viruskontroll.
Vad detta betyder för framtida hiv‑kurstrategier
För en icke‑specialist är huvudbudskapet att storleken på den dolda hiv‑reservoaren inte är fast — den påverkas starkt av hur medfödda immunceller är kopplade på nivån av deras DNA‑packning. När TGF‑β dominerar rekryterar det epigenetiska enzymer som låser ner antivirala gener, vilket lämnar celler sårbara och gör att den virala reservoaren kan bestå. När interferon‑drivna program och IL‑6‑medierad förstärkning dominerar blir många potentiella målceller svårare att infektera, och reservoaren krymper. Eftersom läkemedel som blockerar PD‑1 och HDACs, samt medel som stärker interferonvägar, redan finns inom cancer och andra områden, pekar dessa resultat mot kombinationsterapier som skulle kunna ominprogrammera medfödd immunitet, dämpa TGF‑β:s undertryckande inflytande och gradvis erodera hiv:s sista tillflyktsorter i kroppen.
Citering: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Nyckelord: HIV-reservoar, medfödd immunitet, interferonsignalering, TGF-beta, epigenetisk ominprogrammering