Clear Sky Science · tr
TGF-β, doğuştan gelen antiviral yanıtların epigenetik kontrolünü ve SIV rezervuar büyüklüğünü düzenliyor
Bu araştırma HIV ile yaşayan insanlar için neden önemli
Günümüzün güçlü HIV ilaçlarına rağmen, virüsün küçük bir havuzu bağışıklık hücrelerinin içinde sessizce saklanır ve tedavi durduğunda enfeksiyonu yeniden alevlendirebilir. Bu rhesus makaklarında yapılan çalışma, saklı rezervuarı küçültmenin yeni bir yolunu; klasik virüsle savaşan T hücreleri ve antikorlara odaklanmak yerine, vücudun ilk savunma hattı olan doğuştan gelen bağışıklık sistemini yeniden eğitmenin mümkün olabileceğini araştırıyor. Çalışma ayrıca, ilaç kullanmadan HIV’i kontrol altında tutabilen ‘elit kontrolör’ olarak bilinen küçük bir insan kesimini neden farklı kıldığını açıklamaya yardımcı oluyor.
Bağışıklık hücreleri içinde bir çekişme
Araştırmacılar önemli bir klinik sorundan yola çıktı: antiretroviral tedavi kesildiğinde HIV genellikle uzun ömürlü enfekte hücrelerden geri döner. Önceki çalışmalar, IL-10 ve PD-1 bağışıklık frenlerini engelleyen iki antikorun kombinasyonunun çoğu enfekte makakta viral geri dönüşü kontrol etmesine yardımcı olduğunu ve bazı hayvanlarda CD4 T hücrelerindeki gizli viral DNA miktarında belirgin bir azalma olduğunu göstermişti. Bu makalede ekip, rezervuarları küçülen hayvanları rezervuarı büyük kalan hayvanlardan ayıran özellikleri, lenf düğümleri ve kanda doğuştan gelen bağışıklık hücreleri ile yardımcı T hücrelerin davranışı ve “programlanması” açısından inceledi.
Vücudun doğal antiviral alarmını yükseltmek
Geniş kapsamlı gen aktivite profillemesi ve tek hücre analizleri kullanarak, rezervuarları küçülen hayvanlarda tedavi kesilmeden çok önce güçlü antiviral devrelerin açıldığını buldular. Interferonlar—vücudun antiviral alarm molekülleri—tarafından tipik olarak tetiklenen genler, monositler, dendritik hücreler ve birden fazla T hücresi alt grubu dahil olmak üzere birçok bağışıklık hücresi tipinde yüksek düzeyde aktiftir. Bu genler virüsleri yaşam döngülerinin farklı adımlarında engelleyen “kısıtlama faktörlerini” kodlar. İnsan CD4 T hücreleriyle yapılan laboratuvar deneyleri, interferonla ön işlem görmenin hem doğrudan maruz kalan hücreleri hem de komşu hücreleri HIV enfeksiyonuna karşı çok daha dirençli hale getirdiğini gösterdi; bu da virüs yeniden ortaya çıktığında primlenmiş bir doğuştan yanıtın çevredeki hücreleri nasıl koruyabileceğini vurguluyor.
Sakinleştirici bir sinyalin ters tepmesi
Buna keskin bir karşıtlık olarak, viral rezervuarları büyük kalan hayvanlarda kanda bağışıklığı baskılayan molekül TGF-β yüksek düzeyde bulundu. Ayrıntılı yol analizi TGF-β’yi SMAD proteinlerinin aktivasyonu ve özellikle belirli histon deasetilazlar (HDAC’lar) olmak üzere DNA paketlenmesini sıkılaştıran bir dizi enzimle ilişkilendirdi. Bu epigenetik sıkışma, önemli antiviral genlerin erişimini ve aktive edilmesini zorlaştırdı. İnsan bellek CD4 T hücreleri, TGF-β bakımından zengin plazmaya veya doğrudan TGF-β’ye maruz kaldığında HDAC11’i artırdı, interferon sinyallerine yanıt verme yeteneği azaldı ve in vitro ortamda HIV’e daha kolay enfekte oldu. TGF-β’nin engellenmesi veya HDAC’ların inhibisyonu bu etkileri tersine çevirerek antiviral genlere erişimi yeniden açtı ve enfeksiyonu azalttı.
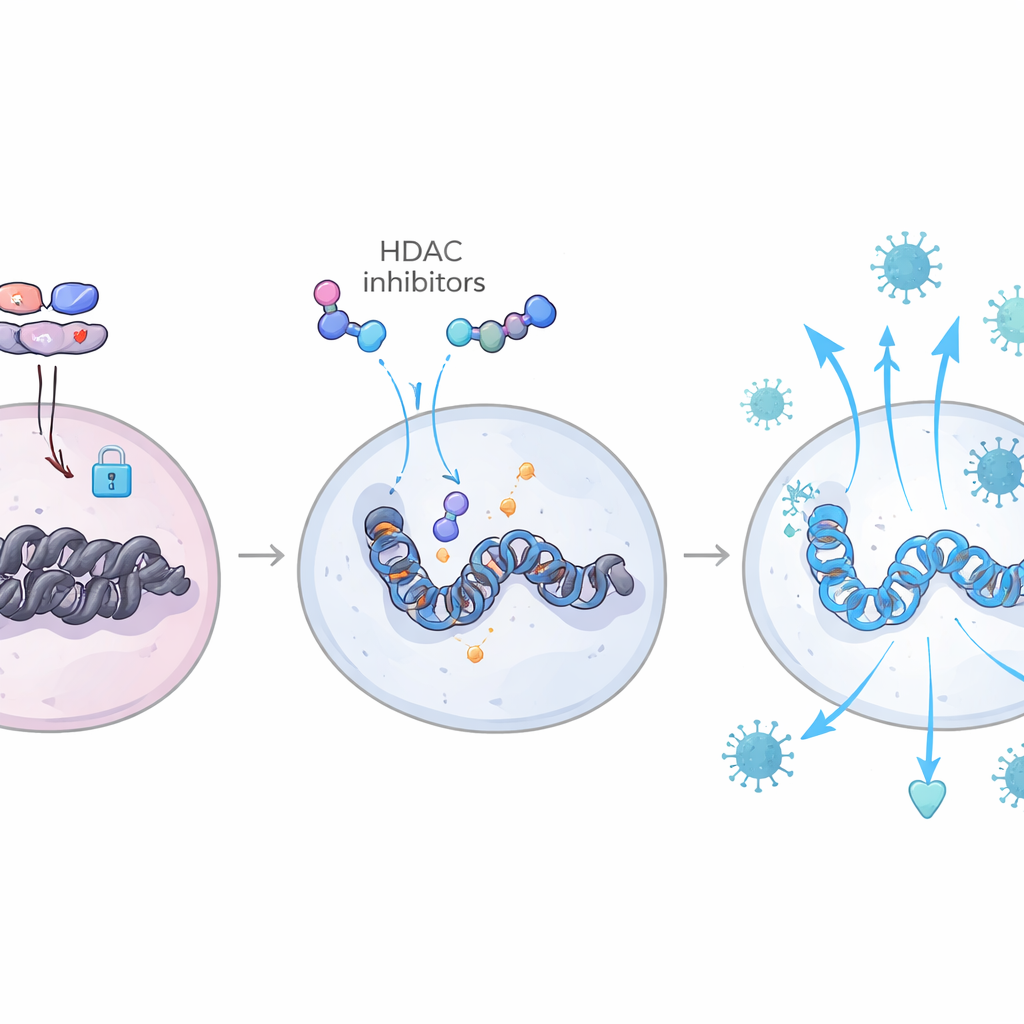
Epigenetik yoluyla bağışıklık oyun kitabını yeniden yazmak
Gen aktivitesi ölçümlerini bireysel hücrelerde kromatin açıklığı haritalarıyla birleştirerek, ekip bu çekişme güçlerini doğrudan genomda görebildi. Rezervuarları küçülen hayvanlarda IRF ve STAT aileleri gibi interferonla ilişkili transkripsiyon faktörlerinin bağlanma bölgeleri T hücreleri ve miyeloid hücreler genelinde daha erişilebilirdi; oysa TGF-β ile ilişkili AP-1 ve SMAD komplekslerinin kullandığı bağlanma bölgeleri nispeten kapalıydı. Bu hayvanlar ayrıca interferon yanıtlarını daha da güçlendiren ve TGF-β’yi sınırlı, inaktif bir biçimde tutmaya yardımcı olan IL-6 ve C/EBP-β faktörünü içeren bir yolun artmış aktivitesini gösterdi. Birlikte, bu durum ilaçlar kesildiğinde yeni enfeksiyon turlarını sınırlayan dayanıklı, “eğitilmiş” antiviral bir durum yarattı. Önemli olarak, aynı gen imzalarının birçoğu insan HIV elit kontrolörlerinin kan hücrelerinde de görüldü; bu da makak bulgularını doğal olarak oluşan bir viral kontrol biçimiyle ilişkilendiriyor.
Gelecekteki HIV kür stratejileri için anlamı
Bir uzman olmayan kişi için temel mesaj şudur: gizli HIV rezervuarının büyüklüğü sabit değildir—DNA paketlenme düzeyinde doğuştan gelen bağışıklık hücrelerinin nasıl kablolandığından güçlü şekilde etkilenir. TGF-β hakim olduğunda, antiviral genleri kilitleyen epigenetik enzimleri göreve çağırır, hücreleri savunmasız bırakır ve viral rezervuarın sürmesine izin verir. Interferon yönlendirmeli programlar ve IL-6 aracılı amplifikasyon öne geçtiğinde ise birçok potansiyel hedef hücre enfekte olmaya daha dirençli hale gelir ve rezervuar küçülür. PD-1 ve HDAC’ları bloke eden ilaçlar ile interferon yollarını güçlendiren ajanlar kanser ve diğer alanlarda zaten mevcut olduğundan, bu sonuçlar doğuştan gelen bağışıklığı yeniden programlayabilecek, TGF-β’nin baskılayıcı etkisini sınırlayabilecek ve zaman içinde HIV’in vücuttaki son kalesini eritmeye yardımcı olabilecek kombinasyon tedavilerine işaret ediyor.
Atıf: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Anahtar kelimeler: HIV rezervuarı, doğuştan gelen bağışıklık, interferon sinyallemesi, TGF-beta, epigenetik yeniden programlama