Clear Sky Science · fr
TGF-β médie le contrôle épigénétique des réponses antivirales innées et la taille du réservoir SIV
Pourquoi cette recherche compte pour les personnes vivant avec le VIH
Même avec les traitements antirétroviraux puissants d’aujourd’hui, une petite réserve de virus reste silencieusement cachée à l’intérieur des cellules immunitaires et peut réamorcer l’infection si le traitement est interrompu. Cette étude chez des macaques rhésus explore une nouvelle façon de réduire ce réservoir caché en rééduquant la première ligne de défense de l’organisme — le système immunitaire inné — plutôt qu’en se concentrant uniquement sur les lymphocytes T et les anticorps classiques. Ce travail aide aussi à expliquer pourquoi une infime fraction de personnes, appelées contrôleurs d’élite, parviennent à contenir le VIH sans médicaments.
Une lutte interne au sein des cellules immunitaires
Les chercheurs sont partis d’un problème clinique important : lorsque la thérapie antirétrovirale est arrêtée, le VIH reprend généralement sa vigueur à partir de cellules infectées de longue durée. Des travaux antérieurs avaient montré que la combinaison de deux anticorps bloquant les freins immunitaires IL-10 et PD-1 aidait la plupart des macaques infectés à contrôler la reprise virale, et qu’un sous-groupe présentait même une baisse marquée de l’ADN viral caché dans leurs cellules T CD4. Dans cet article, l’équipe a cherché à savoir ce qui distinguait les animaux dont les réservoirs ont diminué de ceux dont les réservoirs restaient importants, en se concentrant sur le comportement et la « programmation » des cellules immunitaires innées et des cellules T auxiliaires dans les ganglions lymphatiques et le sang.
Renforcer l’alarme antivirale naturelle de l’organisme
Grâce à un profilage large de l’activité génique et à des analyses en cellule unique, les scientifiques ont constaté que les animaux dont les réservoirs diminuaient avaient activé de puissants circuits antiviraux bien avant l’interruption du traitement. Les gènes typiquement déclenchés par les interférons — les molécules d’alarme antivirale de l’organisme — étaient fortement actifs dans de nombreux types cellulaires immunitaires, y compris les monocytes, les cellules dendritiques et plusieurs sous-ensembles de lymphocytes T. Ces gènes codent des « facteurs de restriction » qui bloquent les virus à différentes étapes de leur cycle de vie. Des expériences en laboratoire sur des cellules T CD4 humaines ont montré que le prétraitement par l’interféron rendait à la fois les cellules directement exposées et leurs voisines beaucoup plus résistantes à l’infection par le VIH, soulignant comment une réponse innée amorcée peut protéger les cellules voisines quand le virus réapparaît.
Comment un signal calmant peut se retourner contre l’hôte
En net contraste, les animaux dont les réservoirs viraux restaient importants présentaient des taux sanguins élevés de la molécule immunosuppressive TGF-β. Une analyse détaillée des voies a relié le TGF-β à l’activation des protéines SMAD et à une série d’enzymes, en particulier certaines histone désacétylases (HDAC), qui renforcent le compactage de l’ADN à l’intérieur des cellules. Cet enroulement épigénétique rendait l’accès et l’activation des gènes antiviraux plus difficiles. Lorsque des cellules T CD4 mémoires humaines ont été exposées au plasma riche en TGF-β, ou au TGF-β lui-même, elles ont augmenté l’expression de HDAC11, sont devenues moins aptes à répondre aux signaux d’interféron et ont été plus facilement infectées par le VIH in vitro. Bloquer le TGF-β ou inhiber les HDAC a inversé ces effets, rouvrant l’accès aux gènes antiviraux et réduisant l’infection.
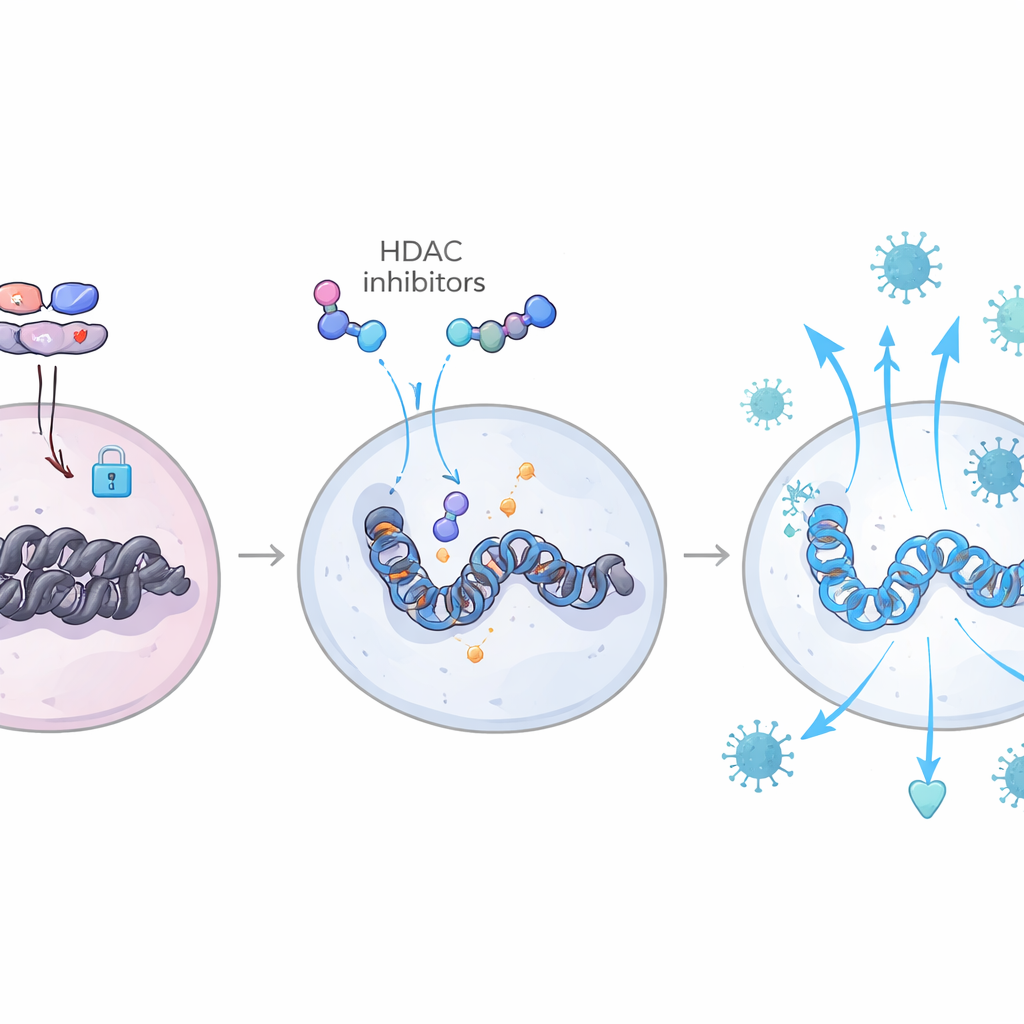
Réécrire le manuel immunitaire par l’épigénétique
En combinant des mesures de l’activité génique avec des cartographies de l’ouverture de la chromatine dans des cellules individuelles, l’équipe a pu observer ces forces antagonistes directement au niveau du génome. Chez les animaux dont les réservoirs diminuaient, les sites de liaison des facteurs de transcription liés aux interférons, tels que les familles IRF et STAT, étaient plus accessibles dans les lymphocytes T et les cellules myéloïdes, tandis que les sites de liaison utilisés par les complexes associés au TGF-β comme AP-1 et SMAD étaient relativement fermés. Ces animaux présentaient également une activité accrue d’une voie impliquant IL-6 et le facteur C/EBP-β, qui amplifie encore les réponses aux interférons et aide à maintenir le TGF-β sous une forme inactive et contenue. Ensemble, cela créait un état antiviral durable et « entraîné » qui limitait de nouvelles vagues d’infection lorsque les médicaments étaient arrêtés. Fait important, de nombreux mêmes profils géniques apparaissaient dans les cellules sanguines de contrôleurs d’élite humains, reliant les observations chez le macaque à une forme naturelle de contrôle viral.
Ce que cela signifie pour les futures stratégies de guérison du VIH
Pour un non-spécialiste, le message principal est que la taille du réservoir caché du VIH n’est pas fixe — elle est fortement influencée par la manière dont les cellules immunitaires innées sont câblées au niveau de l’emballage de leur ADN. Lorsque le TGF-β domine, il recrute des enzymes épigénétiques qui verrouillent les gènes antiviraux, laissant les cellules vulnérables et permettant au réservoir viral de persister. Lorsque les programmes pilotés par les interférons et l’amplification médiée par IL-6 l’emportent, de nombreuses cellules cibles potentielles deviennent plus difficiles à infecter et le réservoir se réduit. Parce que des médicaments bloquant PD-1 et les HDAC, ainsi que des agents stimulant les voies d’interféron, existent déjà en cancérologie et dans d’autres domaines, ces résultats ouvrent la voie à des thérapies combinées susceptibles de reprogrammer l’immunité innée, de réduire l’influence suppressive du TGF-β et d’éroder progressivement les derniers bastions du VIH dans l’organisme.
Citation: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Mots-clés: réservoir du VIH, immunité innée, signalisation de l'interféron, TGF-bêta, reprogrammation épigénétique