Clear Sky Science · nl
TGF-β bemiddelt epigenetische controle van aangeboren antivirale reacties en de grootte van het SIV-reservoir
Waarom dit onderzoek van belang is voor mensen die met hiv leven
Zelfs met de krachtige hiv-medicatie van vandaag verbergt een kleine populatie virussen zich stilletjes in immuuncellen en kan de infectie weer oplaaien als de behandeling stopt. Deze studie bij rhesusapen onderzoekt een nieuwe manier om dat verborgen reservoir te verkleinen door de eerste verdedigingslinie van het lichaam — het aangeboren immuunsysteem — opnieuw te programmeren in plaats van alleen te focussen op klassieke virusbestrijdende T-cellen en antilichamen. Het werk helpt ook verklaren waarom een klein deel van de mensen, bekend als elite controllers, hiv onder controle kan houden zonder geneesmiddelen.
Een touwtrekken binnen immuuncellen
De onderzoekers vertrokken van een belangrijk klinisch probleem: wanneer antiretrovirale therapie wordt gepauzeerd, laait hiv meestal weer op vanuit langlevende geïnfecteerde cellen. Eerder onderzoek toonde aan dat het combineren van twee antilichaamtherapieën die de immuineremmers IL-10 en PD-1 blokkeren, de meeste geïnfecteerde apen hielp om virale terugkeer te beheersen, en dat bij een subset de hoeveelheid viraal DNA verborgen in hun CD4 T-cellen opvallend daalde. In dit artikel onderzochten de onderzoekers wat dieren onderscheidde waarvan de reservoirs krimpten van dieren waarvan de reservoirs groot bleven, met de nadruk op het gedrag en de “programmering” van aangeboren immuuncellen en helper-T-cellen in lymfeklieren en bloed.
Het antivirale alarm van het lichaam aanzetten
Met brede profilering van genactiviteit en single-cell-analyse vonden de wetenschappers dat dieren met krimpende reservoirs krachtige antivirale circuits hadden aangezet ruim voordat de therapie werd onderbroken. Genen die doorgaans door interferonen — de antivirale alarmmoleculen van het lichaam — worden geactiveerd, waren sterk actief in veel immuunceltypen, waaronder monocyten, dendritische cellen en meerdere T-celsubsets. Deze genen coderen voor “restrictiefactoren” die virussen op verschillende stappen in hun levenscyclus blokkeren. Laboratoriumexperimenten met menselijke CD4 T-cellen toonden dat voorbehandeling met interferon zowel rechtstreeks blootgestelde cellen als hun buren veel resistenter maakte tegen hiv-infectie, wat benadrukt hoe een geprimede aangeboren respons voorbijlopende cellen kan beschermen wanneer het virus terugkeert.
Hoe een kalmerend signaal kan tegenwerken
In scherp contrast hadden dieren waarvan de virale reservoirs groot bleven hoge bloedspiegels van het immuundempende molecuul TGF-β. Gedetailleerde padway-analyse koppelde TGF-β aan activatie van SMAD-eiwitten en een reeks enzymen, in het bijzonder bepaalde histon-deacetylasen (HDACs), die de DNA-verpakking in cellen aanscherpen. Deze epigenetische verstrakking maakte belangrijke antivirale genen moeilijker toegankelijk en te activeren. Wanneer menselijke geheugen-CD4 T-cellen werden blootgesteld aan plasma rijk aan TGF-β, of aan TGF-β zelf, verhoogden zij HDAC11, werden ze slechter in het reageren op interferonsignalen en waren ze in vitro gemakkelijker door hiv geïnfecteerd. Het blokkeren van TGF-β of het remmen van HDACs keerde deze effecten om, heropende de toegang tot antivirale genen en verminderde infectie.
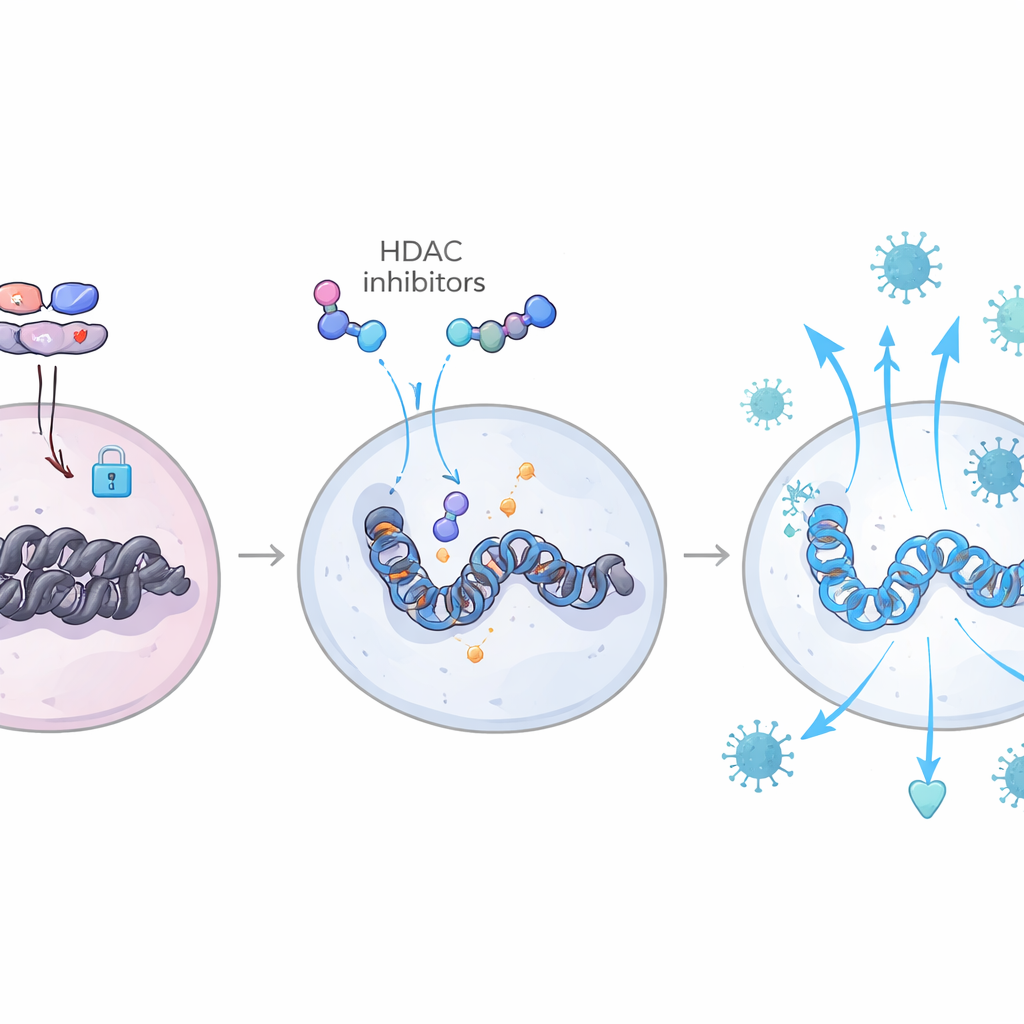
Het immuunhandboek herschrijven via epigenetica
Door metingen van genactiviteit te combineren met kaarten van chromatine-toegankelijkheid in individuele cellen, kon het team deze touwtrek-krachten rechtstreeks in het genoom zien. Bij dieren met krimpende reservoirs waren bindingsplaatsen voor interferon-gekoppelde transcriptiefactoren zoals de IRF- en STAT-families beter toegankelijk in zowel T-cellen als myeloïde cellen, terwijl bindingsplaatsen gebruikt door TGF-β–geassocieerde AP-1- en SMAD-complexen relatief gesloten waren. Deze dieren toonden ook verhoogde activiteit van een route die IL-6 en de factor C/EBP-β omvat, wat interferonresponsen verder versterkt en helpt TGF-β in een geremde, inactieve vorm te houden. Samen creëerde dit een duurzame, “getrainde” antivirale toestand die nieuwe infectierondes beperkte wanneer medicatie werd gestopt. Belangrijk is dat veel van dezelfde genhandtekeningen ook verschenen in bloedcellen van menselijke hiv-elite controllers, wat de bevindingen bij apen verbindt met een van nature voorkomende vorm van virale controle.
Wat dit betekent voor toekomstige hiv-genezingsstrategieën
Voor een niet-specialist is de kernboodschap dat de grootte van het verborgen hiv-reservoir niet vaststaat — ze wordt sterk beïnvloed door hoe aangeboren immuuncellen zijn bedraad op het niveau van hun DNA-verpakking. Wanneer TGF-β domineert, werft het epigenetische enzymen aan die antivirale genen vastzetten, waardoor cellen kwetsbaar blijven en het virale reservoir kan aanhouden. Wanneer interferon-gedreven programma’s en IL-6–gemedieerde amplificatie de overhand krijgen, worden veel potentiële doelcellen moeilijker te infecteren en krimpt het reservoir. Omdat geneesmiddelen die PD-1 en HDACs blokkeren, en middelen die interferonroutes stimuleren, al bestaan in kanker en andere vakgebieden, wijzen deze resultaten op combinatietherapieën die het aangeboren immuunsysteem kunnen herprogrammeren, de onderdrukkende invloed van TGF-β kunnen temperen en geleidelijk hiv’s laatste bolwerken in het lichaam kunnen uitputten.
Bronvermelding: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Trefwoorden: HIV-reservoir, aangeboren immuniteit, interferon-signaleringsweg, TGF-beta, epigenetische herprogrammering