Clear Sky Science · es
TGF-β media el control epigenético de las respuestas antivirales innatas y el tamaño del reservorio de SIV
Por qué esta investigación importa para las personas que viven con VIH
Incluso con los potentes medicamentos actuales contra el VIH, una pequeña reserva de virus permanece oculta de forma silente dentro de las células inmunitarias y puede reavivar la infección si el tratamiento se interrumpe. Este estudio en macacos rhesus explora una nueva forma de reducir ese reservorio oculto reentrenando la primera línea de defensa del cuerpo —el sistema inmunitario innato— en lugar de centrarse solo en las clásicas células T y anticuerpos que combaten el virus. El trabajo también ayuda a explicar por qué una pequeña fracción de personas, conocidas como controladores élite, pueden mantener el VIH bajo control sin fármacos.
Una lucha interna dentro de las células inmunitarias
Los investigadores partieron de un problema clínico importante: cuando se pausa la terapia antirretroviral, el VIH suele resurgir desde células infectadas de larga vida. Trabajos anteriores mostraron que combinar dos anticuerpos que bloquean los frenos inmunitarios IL-10 y PD-1 ayudó a la mayoría de los macacos infectados a controlar la reaparición viral, y un subconjunto incluso presentó una disminución marcada en la cantidad de ADN viral oculto en sus células CD4 T. En este artículo, el equipo se preguntó qué distinguía a los animales cuyo reservorio se redujo de los que mantuvieron reservorios grandes, centrándose en el comportamiento y la “programación” de las células inmunitarias innatas y las células T colaboradoras en los ganglios linfáticos y la sangre.
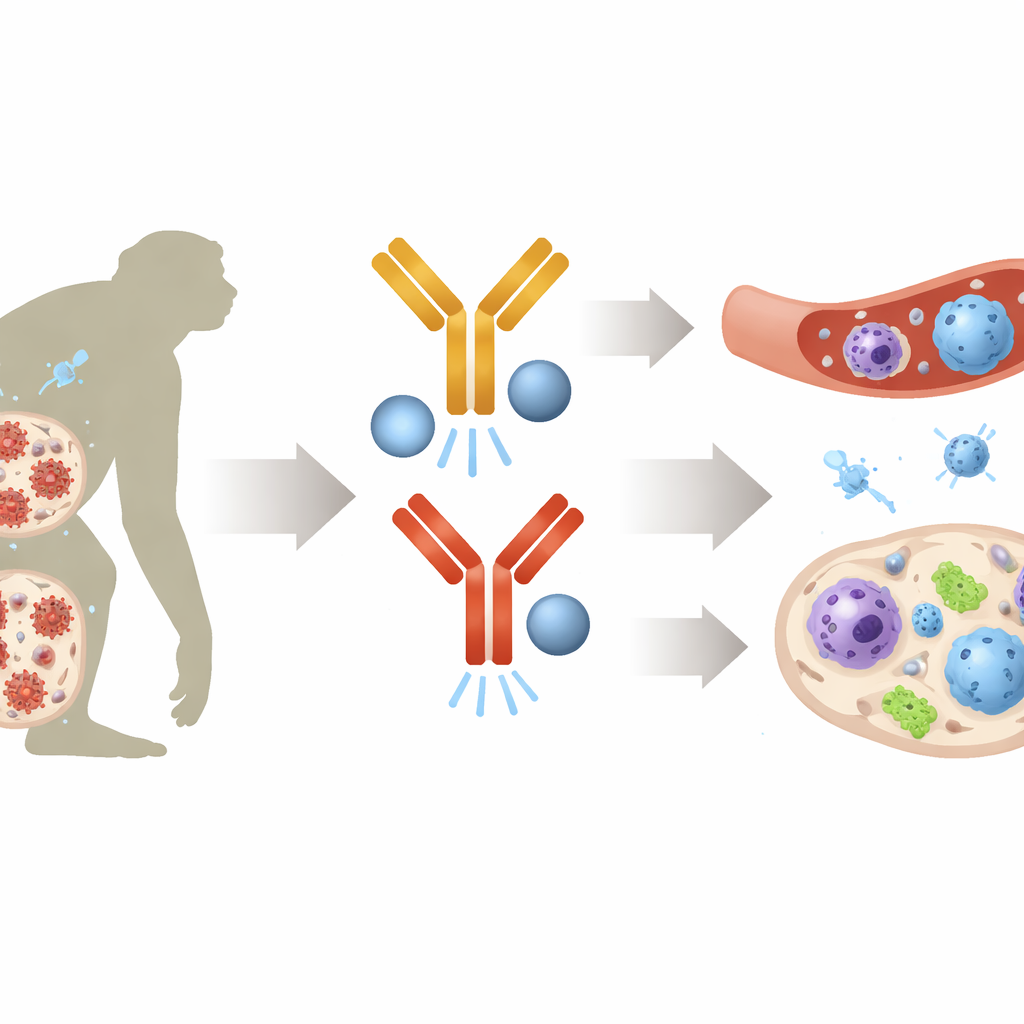
Activar la alarma antiviral natural del organismo
Mediante perfiles amplios de actividad génica y análisis unicelular, los científicos encontraron que los animales con reservorios en disminución habían activado circuitos antivirales potentes mucho antes de que se interrumpiera la terapia. Genes típicamente inducidos por interferones —las moléculas de alarma antiviral del organismo— estaban muy activos en muchos tipos de células inmunitarias, incluidos monocitos, células dendríticas y varios subconjuntos de células T. Estos genes codifican “factores de restricción” que bloquean los virus en diferentes etapas de su ciclo vital. Experimentos de laboratorio con células CD4 T humanas mostraron que el tratamiento previo con interferón hizo que tanto las células expuestas directamente como sus vecinas fueran mucho más resistentes a la infección por VIH, subrayando cómo una respuesta innata primada puede proteger a las células colaterales cuando el virus reaparece.
Cómo una señal calmante puede volverse contraproducente
En marcado contraste, los animales cuyos reservorios virales permanecieron grandes presentaban niveles sanguíneos elevados de la molécula inmunosupresora TGF-β. Un análisis detallado de vías vinculó TGF-β con la activación de proteínas SMAD y un conjunto de enzimas, especialmente determinadas histona desacetilasas (HDACs), que compactan la estructura del ADN dentro de las células. Este endurecimiento epigenético dificultó el acceso y la activación de genes antivirales clave. Cuando células CD4 T de memoria humanas se expusieron a plasma rico en TGF-β, o al propio TGF-β, aumentaron la expresión de HDAC11, respondieron peor a las señales de interferón y fueron más fácilmente infectadas por el VIH in vitro. Bloquear TGF-β o inhibir las HDAC revirtió estos efectos, reabriendo el acceso a genes antivirales y reduciendo la infección.
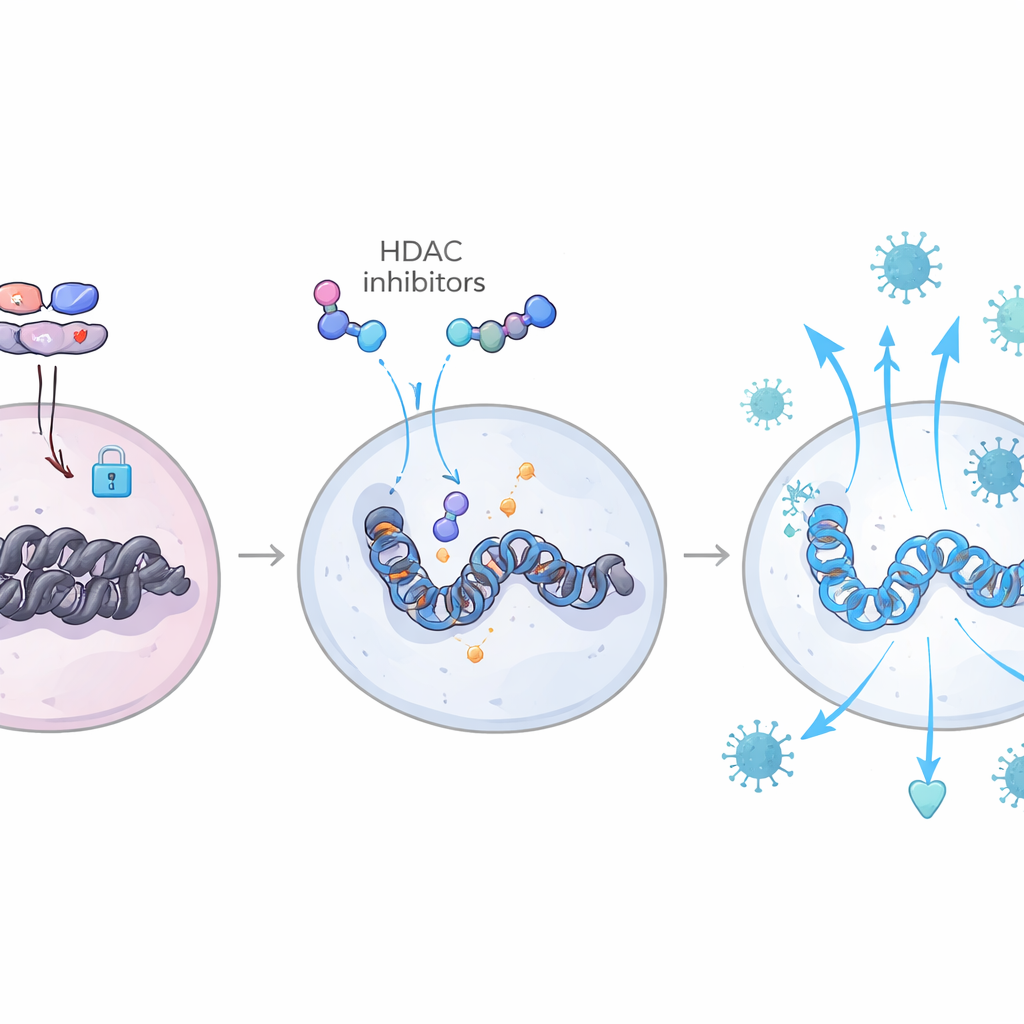
Reescribir el manual inmunitario mediante la epigenética
Al combinar mediciones de actividad génica con mapas de la accesibilidad de la cromatina en células individuales, el equipo pudo observar directamente estas fuerzas opuestas en el genoma. En animales con reservorios en reducción, los sitios de unión para factores de transcripción ligados al interferón, como las familias IRF y STAT, eran más accesibles en células T y células mieloides, mientras que los sitios de unión utilizados por complejos asociados a TGF-β —AP-1 y SMAD— estaban relativamente cerrados. Estos animales también mostraron mayor actividad de una vía que incluye IL-6 y el factor C/EBP-β, que amplifica las respuestas de interferón y ayuda a mantener al TGF-β en una forma restringida e inactiva. En conjunto, esto creó un estado antiviral duradero y “entrenado” que limitó nuevas rondas de infección cuando se interrumpieron los fármacos. De manera importante, muchas de las mismas firmas génicas aparecieron en células sanguíneas de controladores élite humanos con VIH, vinculando los hallazgos en macacos con una forma de control viral que ocurre de manera natural.
Qué significa esto para futuras estrategias de curación del VIH
Para un público no especialista, el mensaje principal es que el tamaño del reservorio oculto de VIH no está fijo: está fuertemente influido por cómo están configuradas las células inmunitarias innatas a nivel del empaquetamiento de su ADN. Cuando TGF-β domina, recluta enzimas epigenéticas que cierran los genes antivirales, dejando las células vulnerables y permitiendo que el reservorio viral persista. Cuando predominan los programas impulsados por interferón y la amplificación mediada por IL-6, muchas células diana potenciales se vuelven más difíciles de infectar y el reservorio se reduce. Dado que ya existen fármacos que bloquean PD-1 y las HDAC, y agentes que potencian las vías de interferón en oncología y otros campos, estos resultados apuntan hacia terapias combinadas que podrían reprogramar la inmunidad innata, frenar la influencia supresora de TGF-β y erosionar gradualmente los últimos refugios del VIH en el organismo.
Cita: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Palabras clave: Reservorio de VIH, inmunidad innata, señalización de interferón, TGF-beta, reprogramación epigenética