Clear Sky Science · de
TGF-β vermittelt epigenetische Kontrolle angeborener antiviraler Reaktionen und die Größe des SIV-Reservoirs
Warum diese Forschung für Menschen mit HIV wichtig ist
Auch mit den heutigen wirksamen HIV-Medikamenten verbirgt sich eine kleine Virusreserve still in Immunzellen und kann die Infektion wieder aufflammen lassen, wenn die Behandlung abgesetzt wird. Diese Studie an Rhesusaffen untersucht einen neuen Weg, dieses verborgene Reservoir zu verkleinern, indem die erste Verteidigungslinie des Körpers — das angeborene Immunsystem — umgeschult wird, anstatt sich ausschließlich auf klassische virusbekämpfende T‑Zellen und Antikörper zu konzentrieren. Die Arbeit trägt außerdem dazu bei zu erklären, warum eine kleine Gruppe von Menschen, die sogenannten Elite-Controller, HIV ohne Medikamente im Zaum halten kann.
Ein Tauziehen innerhalb der Immunzellen
Die Forschenden gingen von einem wichtigen klinischen Problem aus: Wenn die antiretrovirale Therapie unterbrochen wird, bricht HIV in der Regel aus langlebigen infizierten Zellen wieder aus. Frühere Arbeiten zeigten, dass die Kombination zweier Antikörper, die die Immunbremsen IL‑10 und PD‑1 blockieren, den meisten infizierten Makaken half, das virale Wiederauftreten zu kontrollieren, und bei einem Teil sogar die Menge an viralem DNA in ihren CD4‑T‑Zellen deutlich sank. In diesem Papier untersuchte das Team, was Tiere mit schrumpfenden Reservoirs von solchen mit großen Reservoirs unterschied, mit Fokus auf das Verhalten und die „Programmierung“ angeborener Immunzellen und Helfer‑T‑Zellen in Lymphknoten und Blut.
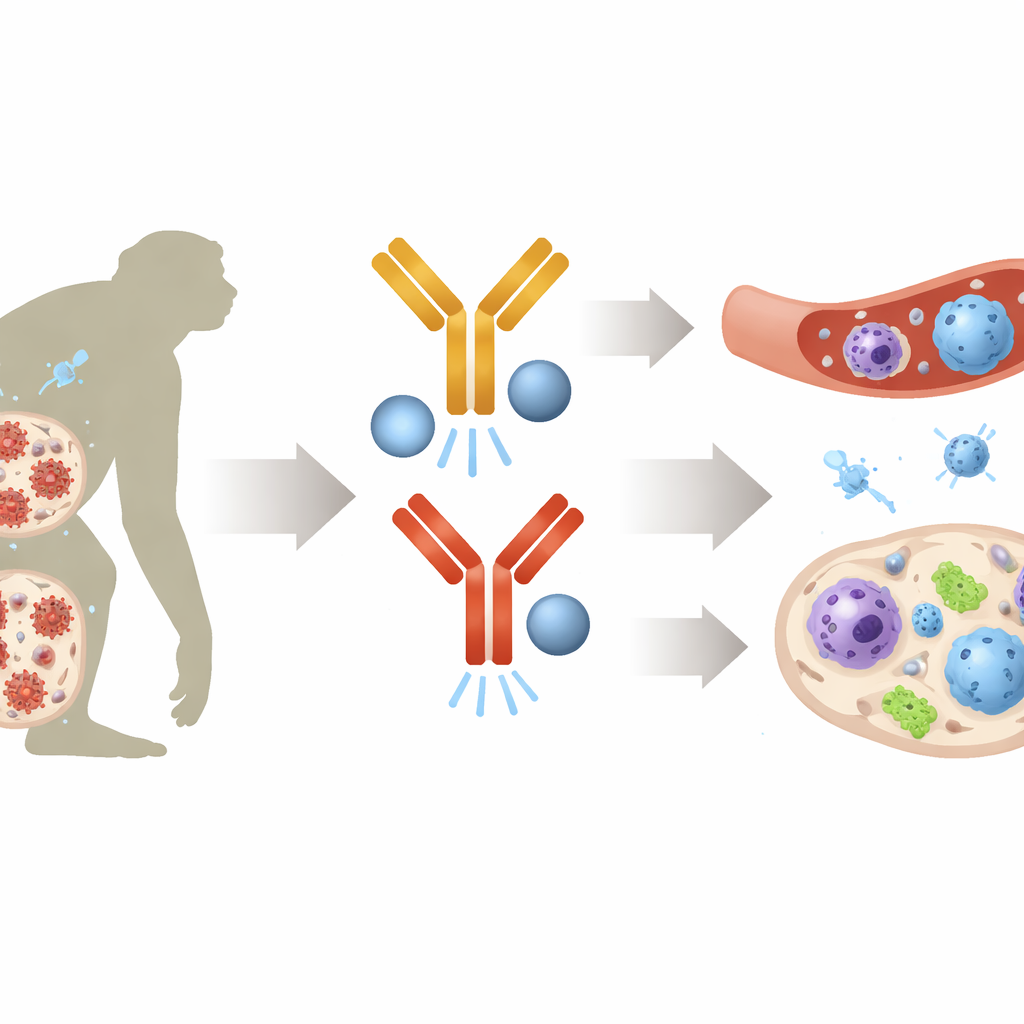
Das natürliche antivirale Alarmsystem hochfahren
Mithilfe umfassender Genaktivitätsprofile und Einzelzellanalysen fanden die Wissenschaftler, dass Tiere mit schrumpfenden Reservoirs leistungsfähige antivirale Schaltkreise bereits lange vor dem Absetzen der Therapie aktiviert hatten. Gene, die typischerweise durch Interferone — die antiviralen Alarmmoleküle des Körpers — ausgelöst werden, waren in vielen Immunzelltypen stark aktiv, darunter Monozyten, dendritische Zellen und mehrere T‑Zell‑Untergruppen. Diese Gene kodieren sogenannte „Restriktionsfaktoren“, die Viren an verschiedenen Punkten ihres Lebenszyklus blockieren. Laborversuche mit menschlichen CD4‑T‑Zellen zeigten, dass eine Vorbehandlung mit Interferon sowohl direkt exponierte Zellen als auch benachbarte Zellen deutlich resistenter gegenüber einer HIV‑Infektion machte, was unterstreicht, wie eine primed angeborene Antwort Neben‑Zellen schützen kann, wenn das Virus wieder auftaucht.
Wie ein beruhigendes Signal nach hinten losgehen kann
Im starken Gegensatz dazu hatten Tiere mit großen viralen Reservoirs hohe Blutspiegel des immundämpfenden Moleküls TGF‑β. Detaillierte Pfadanalyse verknüpfte TGF‑β mit der Aktivierung von SMAD‑Proteinen und einer Reihe von Enzymen, insbesondere bestimmten Histondeacetylasen (HDACs), die die DNA‑Verpackung innerhalb der Zellen verdichten. Diese epigenetische Verdichtung machte wichtige antivirale Gene schwerer zugänglich und damit schwerer aktivierbar. Wenn menschliche Gedächtnis‑CD4‑T‑Zellen Plasma mit hohem TGF‑β‑Gehalt oder TGF‑β selbst ausgesetzt wurden, erhöhten sie HDAC11, reagierten schlechter auf Interferon‑Signale und ließen sich in vitro leichter von HIV infizieren. Die Blockade von TGF‑β oder die Hemmung von HDACs kehrte diese Effekte um, öffnete den Zugang zu antiviralen Genen wieder und reduzierte die Infektion.
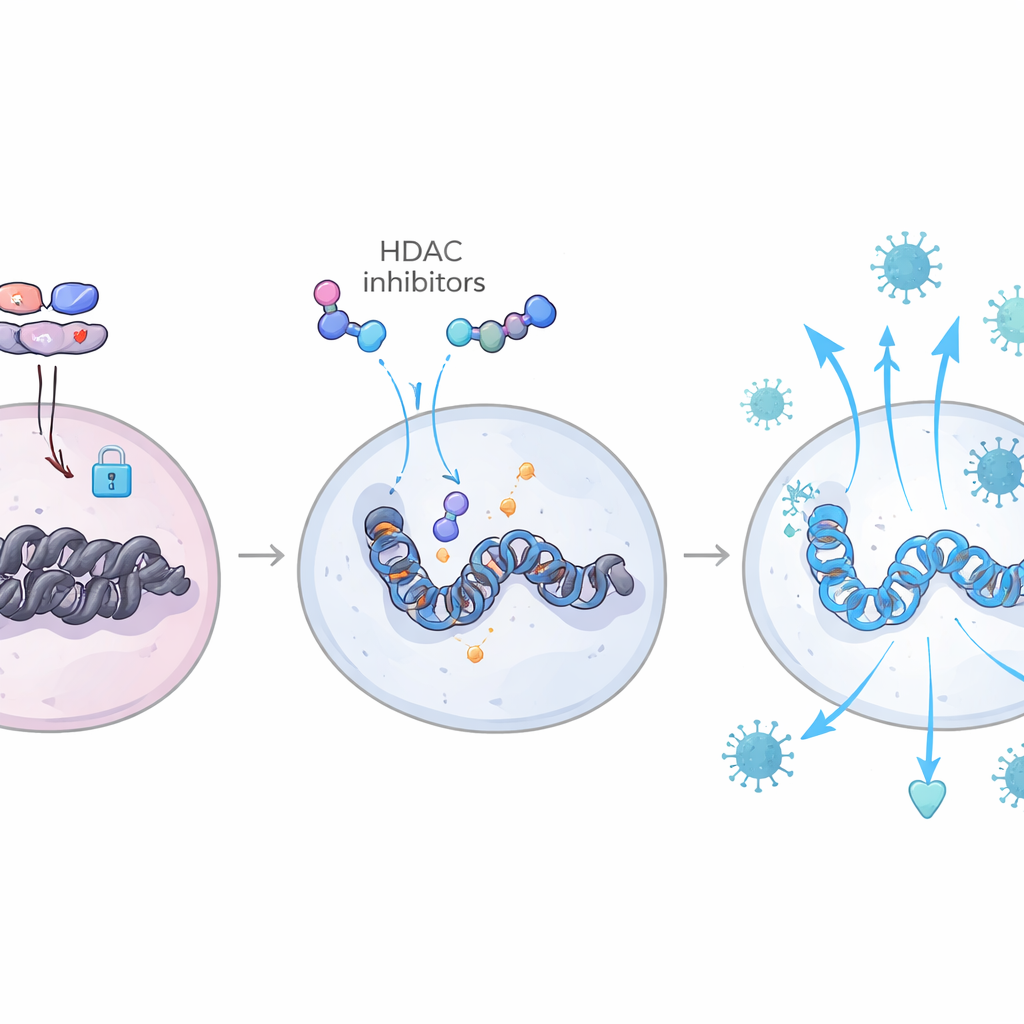
Das Immun‑Spielbuch durch Epigenetik umschreiben
Durch die Kombination von Messungen der Genaktivität mit Karten der Chromatin‑Zugänglichkeit in einzelnen Zellen konnte das Team dieses Tauziehen direkt im Genom beobachten. Bei Tieren mit schrumpfenden Reservoirs waren Bindungsstellen für interferonverknüpfte Transkriptionsfaktoren wie Mitglieder der IRF‑ und STAT‑Familien in T‑Zellen und myeloiden Zellen besser zugänglich, während Bindungsstellen, die von TGF‑β‑assoziierten AP‑1‑ und SMAD‑Komplexen genutzt werden, relativ verschlossen waren. Diese Tiere zeigten zudem eine erhöhte Aktivität eines Signalwegs, der IL‑6 und den Faktor C/EBP‑β umfasst, was Interferon‑Antworten weiter verstärkt und hilft, TGF‑β in einer zurückhaltenden, inaktiven Form zu halten. Zusammengenommen schuf dies einen dauerhaften, „trainierten“ antiviralen Zustand, der neue Infektionsrunden begrenzte, wenn Medikamente abgesetzt wurden. Wichtig ist, dass viele derselben Gen‑Signaturen auch in Blutzellen von menschlichen HIV‑Elite‑Controllern zu sehen waren, wodurch die Befunde aus Makaken mit einer natürlich vorkommenden Form der Viruskontrolle verknüpft werden.
Was das für künftige HIV‑Heilungsstrategien bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die Größe des verborgenen HIV‑Reservoirs ist nicht festgelegt — sie wird stark davon beeinflusst, wie angeborene Immunzellen auf Ebene ihrer DNA‑Verpackung verdrahtet sind. Wenn TGF‑β dominiert, rekrutiert es epigenetische Enzyme, die antivirale Gene zusperren, wodurch Zellen verwundbar bleiben und das virale Reservoir persistieren kann. Wenn interferongetriebene Programme und IL‑6‑vermittelte Verstärkung überwiegen, werden viele potenzielle Zielzellen schwerer zu infizieren und das Reservoir schrumpft. Da Medikamente, die PD‑1 und HDACs blockieren, sowie Wirkstoffe, die Interferon‑Wege stärken, bereits in der Onkologie und anderen Bereichen existieren, deuten diese Ergebnisse auf Kombinationsansätze hin, die das angeborene Immunsystem umprogrammieren, den unterdrückenden Einfluss von TGF‑β dämpfen und die letzten Zufluchtsorte von HIV im Körper schrittweise aushöhlen könnten.
Zitation: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Schlüsselwörter: HIV-Reservoir, angeborene Immunität, Interferon-Signalgebung, TGF-beta, epigenetische Umprogrammierung