Clear Sky Science · ar
يعتمد TGF-β على التحكم اللاجيني في الاستجابات الفطرية لمضادات الفيروسات وحجم مخزون SIV
لماذا تهم هذه الدراسة الأشخاص المصابين بفيروس نقص المناعة البشرية
حتى مع الأدوية الفعالة لعلاج فيروس نقص المناعة البشرية اليوم، يبقى مجموعة صغيرة من الفيروس مخفيّة بصمت داخل خلايا المناعة ويمكن أن تعيد إشعال العدوى إذا توقفت المعالجة. تستكشف هذه الدراسة في رزوس المكاك نهجًا جديدًا لتقليص ذلك المخزون الخفي من خلال إعادة تدريب خط الدفاع الأول في الجسم—المناعة الفطرية—بدلاً من التركيز فقط على خلايا T والأجسام المضادة التقليدية المقاومة للفيروسات. كما تساعد النتائج في تفسير لماذا يستطيع جزء ضئيل من الأشخاص، المعروفون بالمتحكمين النخبة، إبقاء الفيروس تحت السيطرة دون أدوية.
سحب وحسم داخل خلايا المناعة
انطلق الباحثون من مشكلة سريرية مهمة: عند إيقاف العلاج المضاد للفيروسات، عادةً ما يعود فيروس نقص المناعة البشرية من الخلايا المصابة طويلة العمر. أظهرت أبحاث سابقة أن الجمع بين عقارين مناعيَّين مضادين يثبطان كوابح المناعة IL-10 وPD-1 ساعد معظم المكاك المصابة على التحكم في عودة الفيروس، وبنسبة منهم انخفضت كمية الحمض النووي الفيروسي المختبئة في خلايا CD4 T. في هذه الورقة، سأل الفريق ماذا يميز الحيوانات التي انكمش فيها المخزون عن تلك التي بقي مخزونها كبيرًا، مع التركيز على سلوك و«برمجة» الخلايا المناعية الفطرية وخلايا T المساعدة في الغدد اللمفاوية والدم.
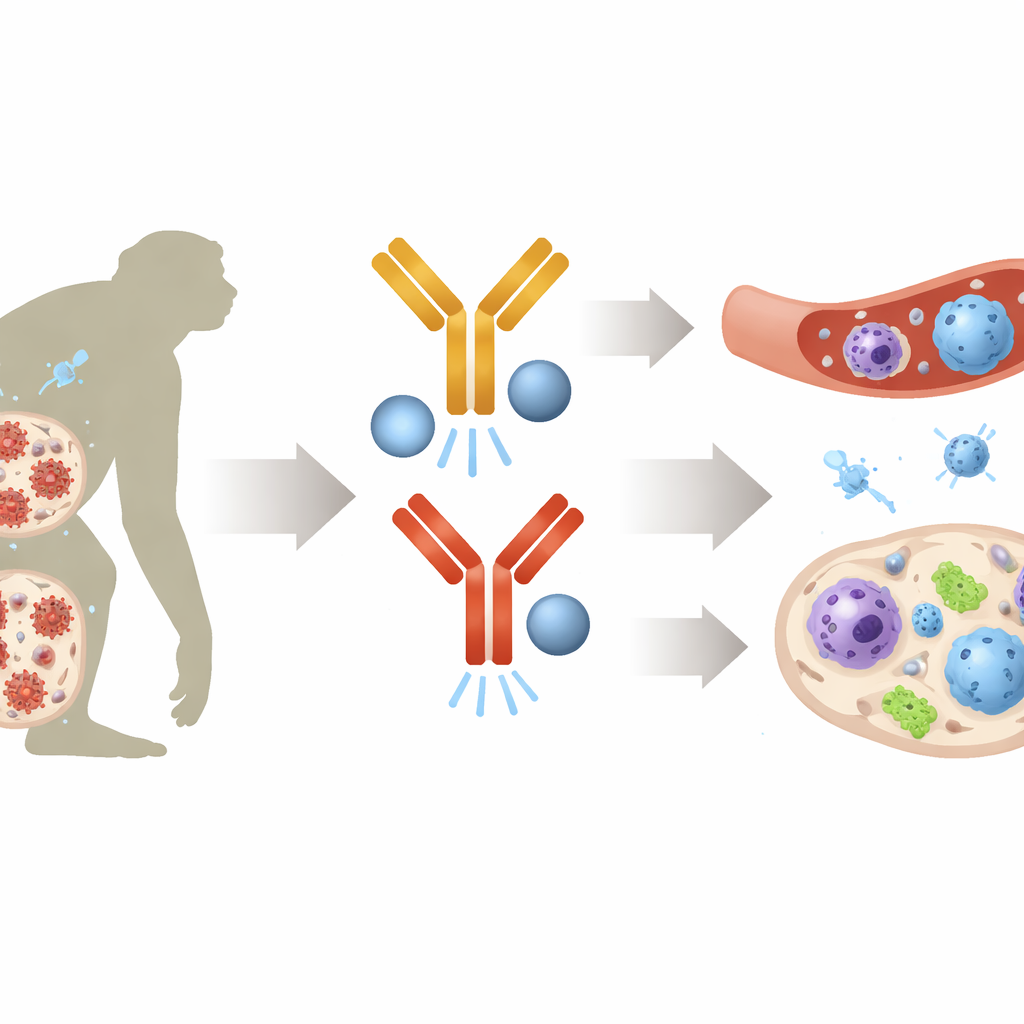
رفع إنذار الجسم الطبيعي المضاد للفيروسات
باستخدام بروفايل واسع لنشاط الجينات وتحليل على مستوى الخلية الواحدة، وجد العلماء أن الحيوانات ذات المخازن المتناقصة قد شغلت دوائر مضادة للفيروسات قوية قبل وقت طويل من وقف العلاج. كانت الجينات التي عادةً ما تنشط بواسطة الإنترفيرونات—جزيئات إنذار الجسم المضادة للفيروسات—نشطة بقوة في العديد من أنواع الخلايا المناعية، بما في ذلك الوحيدات والخلايا التغصُّنية والعديد من أصناف خلايا T. تشفر هذه الجينات عوامل «تقييد» تعترض الفيروسات في مراحل مختلفة من دورة حياتها. أظهرت تجارب مخبرية على خلايا CD4 T بشرية أن المعالجة المسبقة بالإنترفيرون جعلت الخلايا المعرضة مباشرة وجيرانها أكثر مقاومة لعدوى HIV، مما يؤكد كيف يمكن للاستجابة الفطرية المُهيأة أن تحمي الخلايا المجاورة عند عودة الفيروس.
كيف يمكن أن يعود الإشارة المهدئة بنتيجة عكسية
على النقيض التام، كانت الحيوانات التي ظل مخزونها الفيروسي كبيرًا لديها مستويات دم عالية من الجزيء المطِّبط للمناعة TGF-β. ربط تحليل المسارات التفصيلي TGF-β بتفعيل بروتينات SMAD ومجموعة من الإنزيمات، لا سيما بعض ناقلات ديستيل الأسيتيل للهستون (HDACs)، التي تُشدِّد تغليف الحمض النووي داخل الخلايا. جعل هذا الشد اللاجيني من الصعب الوصول إلى الجينات المضادة للفيروسات وتشغيلها. عندما تعرضت خلايا CD4 T الذاكرية البشرية لبلازما غنية بـTGF-β، أو لـTGF-β بمفرده، رفعت تعبير HDAC11، وأصبحت أقل استجابة لإشارات الإنترفيرون، وكان من السهل إصابتها بـHIV في المختبر. عكس حجب TGF-β أو تثبيط HDACs هذه التأثيرات، فأعاد فتح الوصول إلى الجينات المضادة للفيروسات وخفض العدوى.
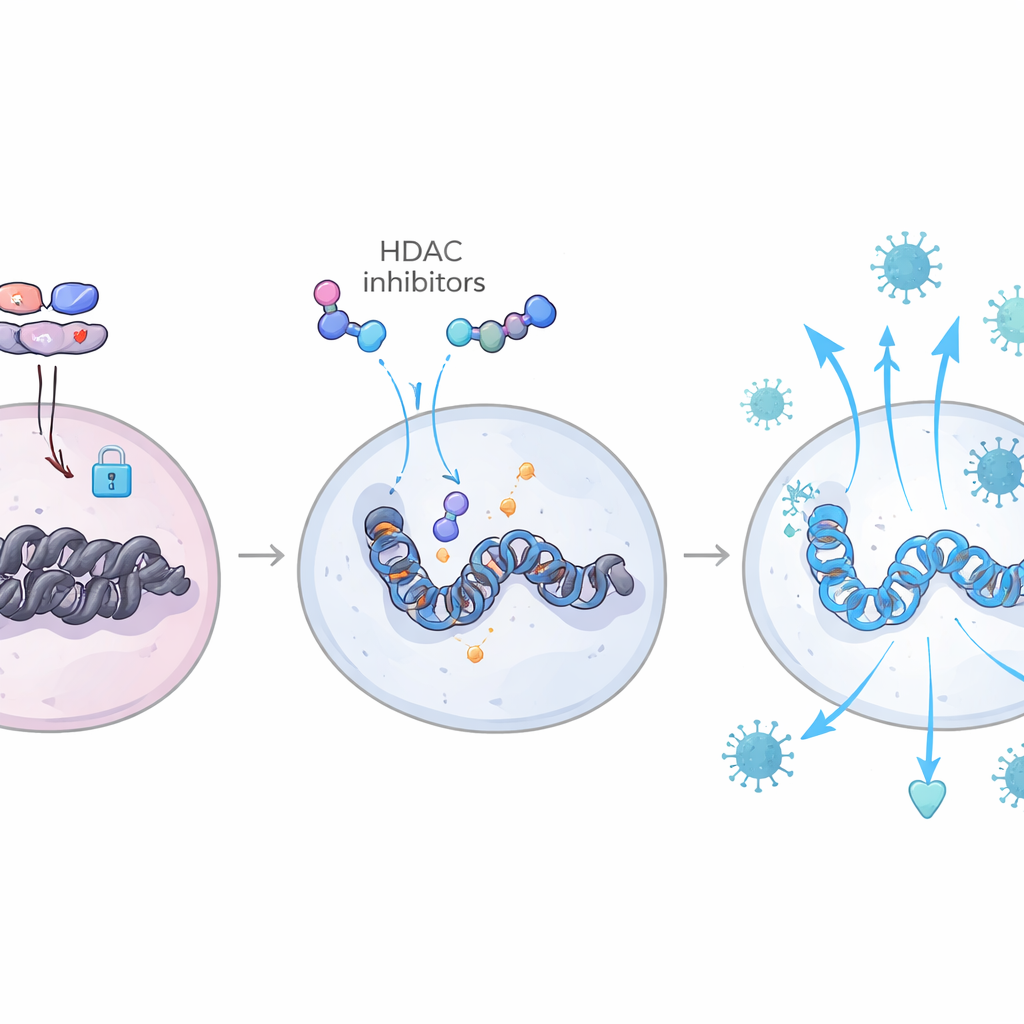
إعادة كتابة دفتر تكتيكات المناعة عبر اللاجين
من خلال الجمع بين قياسات نشاط الجينات وخرائط انفتاح الكروماتين في خلايا فردية، تمكن الفريق من رؤية قوى السحب والحسم هذه مباشرة في الجينوم. في الحيوانات التي انكمش فيها المخزون، كانت مواقع ربط عوامِل النسخ المرتبطة بالإنترفيرون مثل عائلات IRF وSTAT أكثر انفتاحًا عبر خلايا T والخلايا النخاعية، بينما كانت مواقع الربط المستخدمة من قِبل مركبات AP-1 وSMAD المرتبطة بـTGF-β مغلقة نسبيًا. كما أظهرت هذه الحيوانات نشاطًا متزايدًا لمسار يشمل IL-6 والعامل C/EBP-β، الذي يضخم المزيد من استجابات الإنترفيرون ويساعد على إبقاء TGF-β في شكل مقيد وغير نشط. معًا، خلق ذلك حالة مضادة للفيروسات «مدرَّبة» ودائمة حدّت من جولات عدوى جديدة عند وقف الأدوية. والأهم أن العديد من هذه البصمات الجينية ظهرت أيضًا في خلايا دم لمتحكمين نخبويين بشريين بفيروس HIV، ما يربط نتائج المكاك بشكل طبيعي بشكلٍ ما بنمط حدوث السيطرة الفيروسية لدى البشر.
ماذا يعني هذا لاستراتيجيات علاجية مستقبلة لهدف شفاء فيروس HIV
بالنسبة لغير المتخصصين، الرسالة الأساسية أن حجم مخزون HIV الخفي ليس ثابتًا—إنه يتأثر بشدة بكيفية توصيل خلوية المناعة الفطرية عند مستوى تغليف الحمض النووي. عندما يسود TGF-β، يجند إنزيمات لاجينية تُقفل الجينات المضادة للفيروسات، مما يترك الخلايا عرضة ويسمح للمخزون الفيروسي بالاستمرار. عندما تسود برامج مدفوعة بالإنترفيرون وتضخيم بواسطة IL-6، تصبح العديد من الخلايا المستهدفة أصعب للإصابة، وينكمش المخزون. ونظرًا لوجود أدوية تَحجب PD-1 وHDACs، وعوامل تعزز مسارات الإنترفيرون بالفعل في مجالات السرطان وغيرها، تشير هذه النتائج إلى علاجات متركبة قد تعيد برمجة المناعة الفطرية، وتقيّد تأثير TGF-β القمعي، وتؤدي تدريجيًا إلى تآكل المعاقل الأخيرة لفيروس HIV في الجسم.
الاستشهاد: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
الكلمات المفتاحية: مخزون فيروس نقص المناعة البشرية, المناعة الفطرية, إشارة الإنترفيرون, TGF-beta, إعادة برمجة ملَكِّيّة اللاجين