Clear Sky Science · it
TGF-β media il controllo epigenetico delle risposte antivirali innate e la dimensione del reservoir SIV
Perché questa ricerca è importante per chi vive con l’HIV
Anche con gli attuali farmaci antiretrovirali potenti, una piccola riserva di virus rimane nascosta silenziosamente all’interno delle cellule immunitarie e può riaccendere l’infezione se il trattamento viene interrotto. Questo studio sui macachi rhesus esplora un nuovo modo per ridurre quel reservoir nascosto rieducando la prima linea di difesa dell’organismo—il sistema immunitario innato—invece di concentrarsi soltanto sulle classiche cellule T e sugli anticorpi. Il lavoro aiuta anche a spiegare perché una piccola frazione di persone, note come elite controller, riesce a tenere l’HIV sotto controllo senza farmaci.
Una lotta interna alle cellule immunitarie
I ricercatori sono partiti da un problema clinico rilevante: quando la terapia antiretrovirale viene sospesa, l’HIV solitamente riprende vigore a partire da cellule infette a lunga persistenza. Studi precedenti avevano mostrato che combinare due farmaci anticorpali che bloccano i freni immunitari IL-10 e PD-1 aiutava la maggior parte dei macachi infetti a controllare la ripresa virale, e in un sottogruppo si osservò anche una netta riduzione della quantità di DNA virale nascosta nelle loro cellule T CD4. In questo articolo il gruppo ha chiesto cosa distinguesse gli animali il cui reservoir si era ridotto da quelli il cui reservoir era rimasto ampio, concentrandosi sul comportamento e sulla “programmazione” delle cellule immunitarie innate e delle cellule T helper nei linfonodi e nel sangue.
Accendere l’allarme antivirale naturale del corpo
Attraverso un’analisi ampia dell’attività genica e studi a singola cellula, gli scienziati hanno riscontrato che gli animali con reservoir in diminuzione avevano attivato potenti circuiti antivirali ben prima che la terapia fosse interrotta. I geni tipicamente indotti dagli interferoni—le molecole di allarme antivirale dell’organismo—erano molto attivi in molti tipi di cellule immunitarie, inclusi monociti, cellule dendritiche e diversi sottogruppi di cellule T. Questi geni codificano “fattori di restrizione” che bloccano i virus in diversi passaggi del loro ciclo vitale. Esperimenti di laboratorio con cellule T CD4 umane hanno mostrato che il pretrattamento con interferone rendeva sia le cellule direttamente esposte sia le loro vicine molto più resistenti all’infezione da HIV, sottolineando come una risposta innata pronta possa proteggere le cellule circostanti quando il virus riemerge.
Come un segnale calmante può ritorcersi contro
Al contrario netto, gli animali il cui reservoir virale rimaneva ampio avevano alti livelli ematici della molecola immunosoppressiva TGF-β. Un’analisi dettagliata dei percorsi ha collegato TGF-β all’attivazione delle proteine SMAD e a una serie di enzimi, in particolare certe deacetilasi istoniche (HDAC), che compattano il DNA all’interno delle cellule. Questo irrigidimento epigenetico rendeva più difficile l’accesso e l’attivazione di geni antivirali chiave. Quando le cellule T CD4 di memoria umane venivano esposte a plasma ricco di TGF-β, o al TGF-β stesso, aumentavano l’espressione di HDAC11, diminuivano la risposta ai segnali interferonici e risultavano più facilmente infettabili dall’HIV in vitro. Bloccare il TGF-β o inibire le HDAC invertiva questi effetti, riaprendo l’accesso ai geni antivirali e riducendo l’infezione.
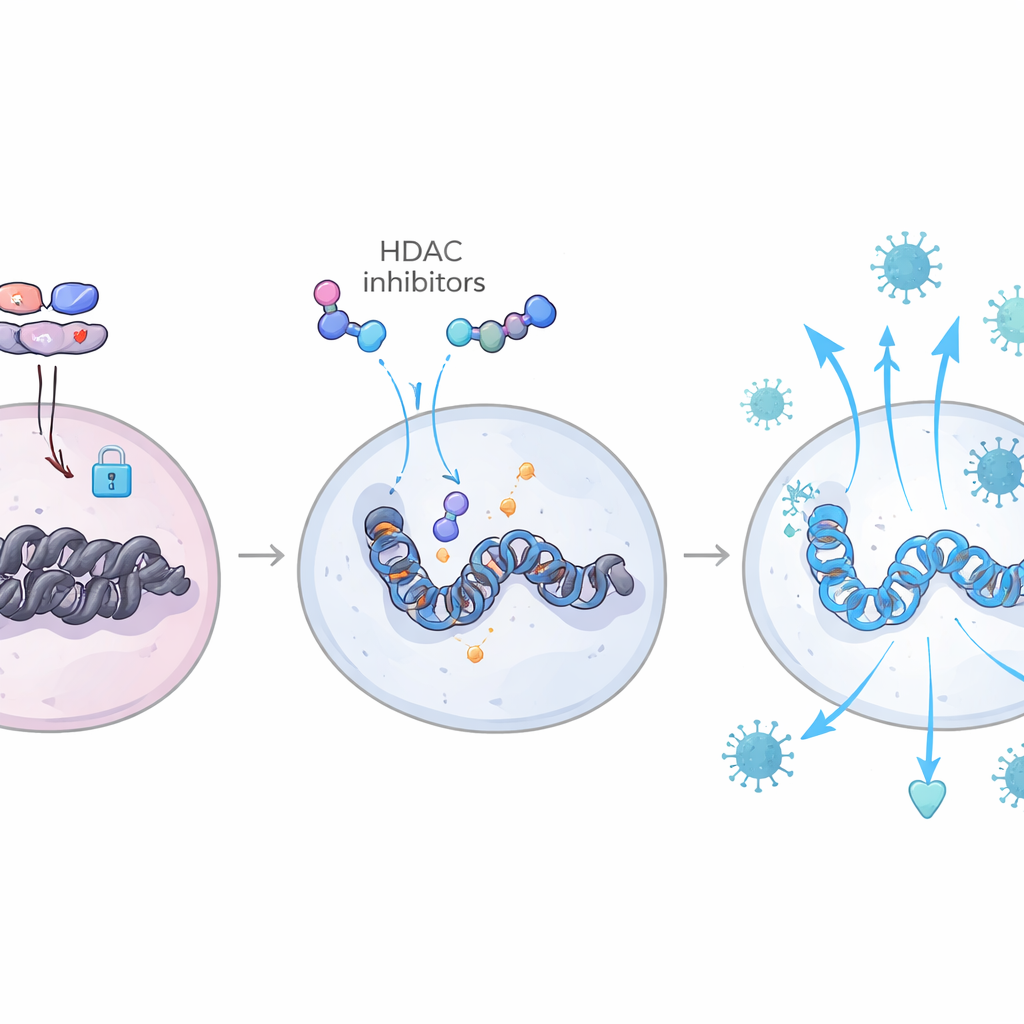
Rieditare il manuale immunitario tramite l’epigenetica
Combinando misure dell’attività genica con mappe dell’apertura della cromatina in singole cellule, il gruppo ha potuto osservare direttamente questi fattori in lotta nel genoma. Negli animali con reservoir in diminuzione, i siti di legame per fattori trascrizionali legati all’interferone, come le famiglie IRF e STAT, erano più accessibili nelle cellule T e nelle cellule mieloidi, mentre i siti di legame utilizzati dai complessi AP-1 e SMAD associati a TGF-β risultavano relativamente chiusi. Questi animali mostravano anche una maggiore attività di una via che coinvolge IL-6 e il fattore C/EBP-β, che amplifica ulteriormente le risposte agli interferoni e contribuisce a mantenere il TGF-β in una forma trattenuta e inattiva. Insieme, questo creava uno stato antivirale duraturo e “allenato” che limitava nuovi cicli d’infezione quando i farmaci venivano sospesi. È importante che molte delle stesse firme geniche siano comparse nelle cellule del sangue di elite controller umani con HIV, collegando i risultati nei macachi a una forma naturalmente presente di controllo virale.
Cosa significa per future strategie di cura dell’HIV
Per chi non è specialista, il messaggio principale è che la dimensione del reservoir nascosto dell’HIV non è fissa—è fortemente influenzata da come le cellule immunitarie innate sono cablate a livello del confezionamento del loro DNA. Quando TGF-β domina, recluta enzimi epigenetici che serrano i geni antivirali, lasciando le cellule vulnerabili e permettendo al reservoir virale di persistere. Quando prevalgono programmi guidati dagli interferoni e l’amplificazione mediata da IL-6, molte potenziali cellule bersaglio diventano più difficili da infettare e il reservoir si riduce. Poiché esistono già farmaci che bloccano PD-1 e HDAC, e agenti che potenziano le vie degli interferoni, impiegati in oncologia e altri settori, questi risultati indicano strategie combinate che potrebbero riprogrammare l’immunità innata, contenere l’influenza soppressiva del TGF-β e erodere gradualmente le ultime roccaforti dell’HIV nell’organismo.
Citazione: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Parole chiave: Reservoir HIV, immunità innata, segnalazione dell'interferone, TGF-beta, riprogrammazione epigenetica