Clear Sky Science · pl
TGF-β pośredniczy w epigenetycznej kontroli wrodzonych odpowiedzi przeciwwirusowych i wielkości rezerwuaru SIV
Dlaczego to badanie ma znaczenie dla osób żyjących z HIV
Nawet przy dzisiejszych silnych lekach przeciwretrowirusowych mała pula wirusa ukrywa się bezobjawowo w komórkach układu odpornościowego i może nawrócić zakażenie, jeśli leczenie zostanie przerwane. Badanie to na makakach rezus bada nową drogę zmniejszenia tego ukrytego rezerwuaru poprzez przeszkolenie pierwszej linii obrony organizmu — odporności wrodzonej — zamiast skupiania się wyłącznie na klasycznych komórkach T i przeciwciałach zwalczających wirusa. Praca pomaga także wyjaśnić, dlaczego niewielka grupa osób, zwana kontrolerami elity, potrafi utrzymywać HIV pod kontrolą bez leków.
Szarpanina wewnątrz komórek odpornościowych
Naukowcy wyszli od istotnego problemu klinicznego: gdy terapię antyretrowirusową przerywa się, HIV zazwyczaj odradza się z długowiecznych zainfekowanych komórek. Wcześniejsze prace wykazały, że łączenie dwóch przeciwciał blokujących hamulce odporności IL-10 i PD-1 pomogło większości zakażonych makaków kontrolować ponowny wzrost wirusa, a u części zwierząt zaobserwowano wyraźny spadek ilości DNA wirusowego ukrytego w komórkach CD4 T. W tej pracy zespół pytał, co odróżniało zwierzęta, u których rezerwuar się kurczył, od tych, u których rezerwuar pozostawał duży, koncentrując się na zachowaniu i „programowaniu” komórek odporności wrodzonej oraz pomocniczych komórek T w węzłach chłonnych i krwi.
Wzmacnianie naturalnego alarmu przeciwwirusowego organizmu
Stosując szerokie profilowanie aktywności genów i analizę pojedynczych komórek, naukowcy stwierdzili, że u zwierząt z kurczącymi się rezerwuarami przed przerwaniem terapii uruchomione zostały silne obwody przeciwwirusowe. Geny zwykle aktywowane przez interferony — molekularne alarmy przeciwwirusowe organizmu — były bardzo aktywne w wielu typach komórek odpornościowych, w tym w monocytach, komórkach dendrytycznych i różnych podtypach komórek T. Geny te kodują „czynniki ograniczające”, które blokują wirusy na różnych etapach ich cyklu życiowego. Doświadczenia laboratoryjne na ludzkich komórkach CD4 T wykazały, że przedtraktowanie interferonem uczyniło zarówno bezpośrednio eksponowane komórki, jak i ich sąsiadów znacznie bardziej opornymi na zakażenie HIV, podkreślając, jak uprzednio pobudzona odpowiedź wrodzona może chronić komórki biorące udział w pobliżu, gdy wirus nawraca.
Jak sygnał uspokajający może obrócić się przeciwko nam
W kontrastującym obrazie zwierzęta, których rezerwuar wirusa pozostał duży, miały wysokie stężenia we krwi cząsteczki tłumiącej odporność TGF-β. Szczegółowa analiza szlaków powiązała TGF-β z aktywacją białek SMAD i grupy enzymów, zwłaszcza niektórych deacetylaz histonowych (HDAC), które zaostrzają pakowanie DNA w komórkach. To epigenetyczne „zaciskanie” utrudniało dostęp do kluczowych genów przeciwwirusowych i ich aktywację. Gdy ludzkie pamięciowe komórki CD4 T eksponowano na osocze bogate w TGF-β lub na sam TGF-β, zwiększały ekspresję HDAC11, gorzej reagowały na sygnały interferonowe i były łatwiej zakażane przez HIV in vitro. Blokowanie TGF-β lub hamowanie HDAC odwracało te efekty, ponownie udostępniając geny przeciwwirusowe i zmniejszając zakażenie.
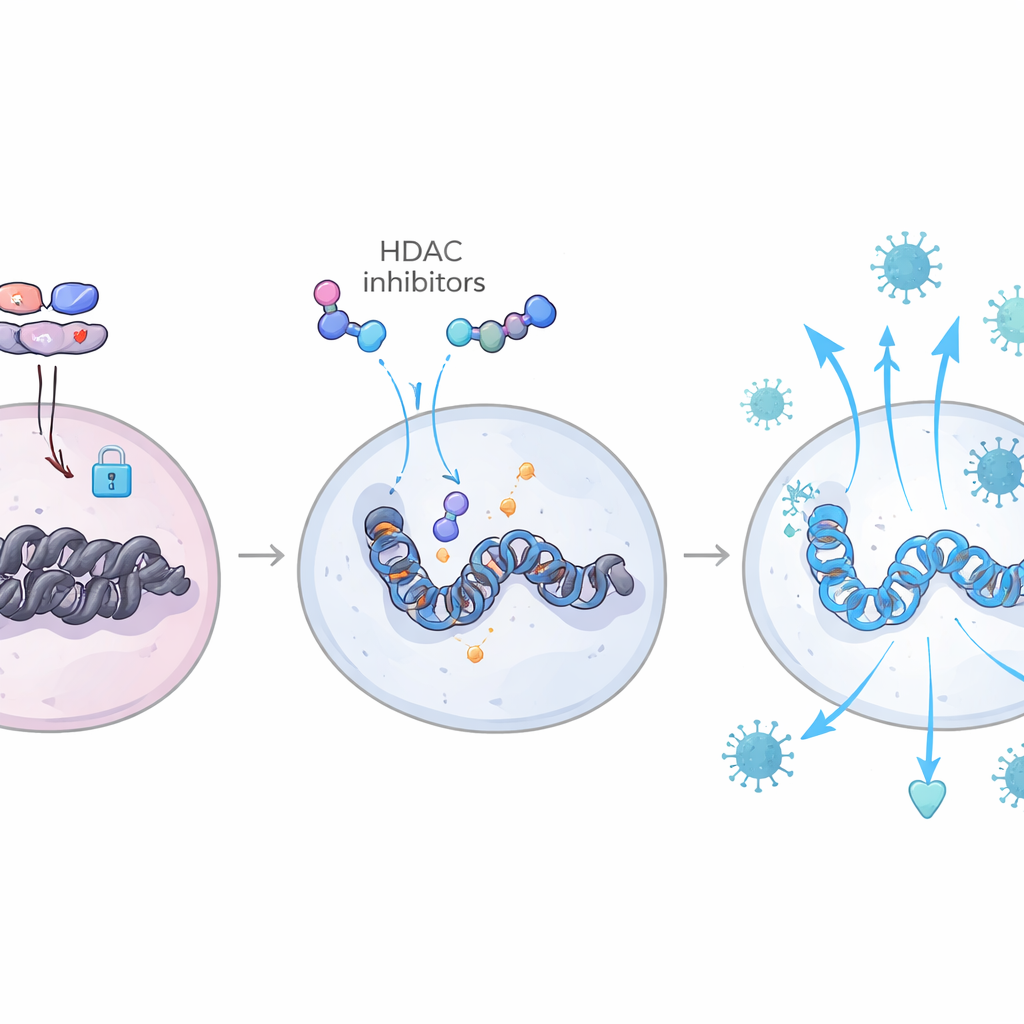
Przepisywanie podręcznika działania układu odpornościowego przez epigenetykę
Łącząc pomiary aktywności genów z mapami dostępności chromatyny w pojedynczych komórkach, zespół mógł bezpośrednio obserwować te siły w genomie. U zwierząt z kurczącymi się rezerwuarami miejsca wiązania czynników transkrypcyjnych związanych z interferonami, takich jak rodziny IRF i STAT, były bardziej dostępne w komórkach T i komórkach mieloidalnych, podczas gdy miejsca wiązania używane przez powiązane z TGF-β kompleksy AP-1 i SMAD były stosunkowo zamknięte. Te zwierzęta wykazywały także zwiększoną aktywność szlaku obejmującego IL-6 i czynnik C/EBP-β, który dodatkowo wzmacnia odpowiedzi interferonowe i pomaga utrzymać TGF-β w zrestrykowanej, nieaktywnej formie. W efekcie powstał trwały, „wytrenowany” stan przeciwwirusowy, który ograniczał nowe rundy zakażeń po zaprzestaniu leków. Co ważne, wiele tych samych sygnatur genowych pojawiało się w komórkach krwi u ludzkich elitarnych kontrolerów HIV, łącząc obserwacje u makaków z naturalnie występującą formą kontroli wirusa.
Co to oznacza dla przyszłych strategii leczenia HIV
Dla osoby niebędącej specjalistą główny przekaz jest taki, że wielkość ukrytego rezerwuaru HIV nie jest stała — jest silnie zależna od tego, jak komórki odporności wrodzonej są „okablowane” na poziomie pakowania ich DNA. Gdy TGF-β dominuje, rekrutuje enzymy epigenetyczne blokujące geny przeciwwirusowe, pozostawiając komórki podatne i umożliwiając utrzymanie rezerwuaru wirusa. Gdy zwycięża program napędzany interferonami i wzmocniony przez IL-6, wiele potencjalnych komórek docelowych staje się trudniejszych do zakażenia, a rezerwuar się kurczy. Ponieważ leki blokujące PD-1 i HDAC oraz środki pobudzające szlaki interferonowe są już stosowane w onkologii i innych dziedzinach, wyniki te wskazują na terapie kombinowane, które mogłyby przeprogramować odporność wrodzoną, ograniczyć tłumiący wpływ TGF-β i stopniowo wytrzeć ostatnie kryjówki HIV w organizmie.
Cytowanie: Ghneim, K., ten-Caten, F., Santana, A.C. et al. TGF-β mediates epigenetic control of innate antiviral responses and SIV reservoir size. Nat Immunol 27, 686–699 (2026). https://doi.org/10.1038/s41590-026-02458-x
Słowa kluczowe: rezerwuar HIV, odporność wrodzona, sygnalizacja interferonowa, TGF-beta, reprogramowanie epigenetyczne