Clear Sky Science · zh
独特来源与生态位决定中枢神经系统巨噬细胞在再生后的细胞反应性
为何脑边界守卫至关重要
我们的大脑不仅由神经元构成。免疫细胞也在组织深处或位于边界处巡逻,那些边界是大脑与保护性膜层和血管相接的地方。本研究考察了这些不同群体的免疫哨兵如何消失并再生,结果表明它们被替代的方式会改变大脑对炎症和卒中的反应。理解这种再生机制为在不扰动大脑其他部分的情况下调整边界免疫细胞的疗法提供了可能。
不同街区,不同的脑哨兵
被称为巨噬细胞的免疫细胞在中枢神经系统占据不同“街区”。小胶质细胞生活在脑组织内部,而所谓的边界巨噬细胞位于大脑表面和血管周围。在这些边界细胞中,皮下(subdural)巨噬细胞紧贴脑组织表面和血管周围间隙,而另一类则定居在坚韧的外膜——硬脑膜(dura)中。尽管这些群体都参与监视并调节脑内的免疫反应,但它们起源和寿命不同,早期研究提示小胶质细胞可以在局部自我维持,而不依赖血源性细胞的补充。
重置系统并观察其再生
为了观察每类巨噬细胞在被清除后如何恢复,研究者在小鼠中使用了一种阻断关键生存信号的药物,暂时耗尽这些细胞。随后他们通过结合遗传“条形码”小鼠、单细胞RNA测序、染色质分析和高分辨率显微镜追踪细胞的来源和归处。脑组织内的小胶质细胞通过稀有幸存者的增殖快速几乎完全恢复,没有迹象表明循环免疫细胞迁入替代它们。相比之下,位于脑表面的皮下巨噬细胞再生缓慢且在不同区域间不均匀,提示它们可能从原有常驻细胞之外动员了额外来源。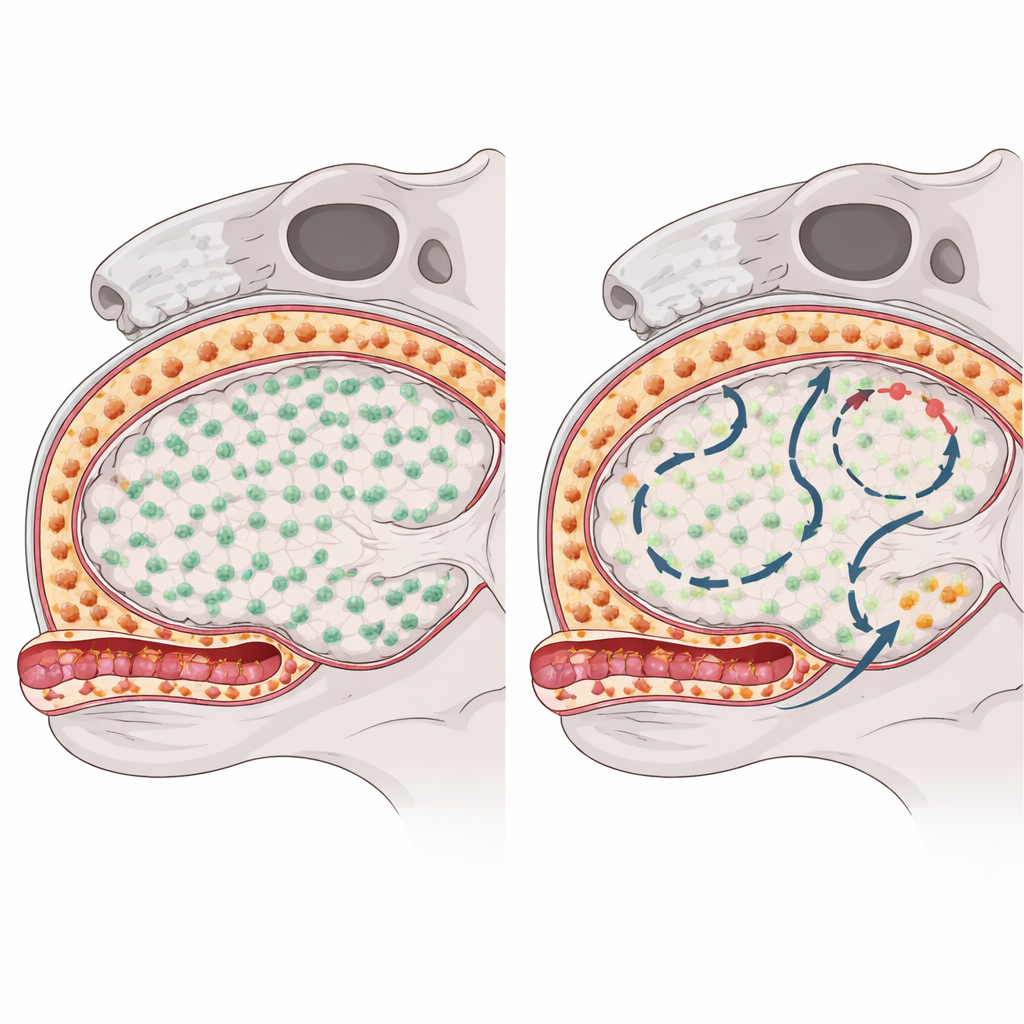
血液细胞迁入并长期驻留
命运追踪实验显示,与小胶质细胞不同,皮下巨噬细胞部分通过循环中短寿命的单核细胞补充其生态位。在耗尽后,血管和基质细胞发出的信号创造了一个短暂的窗口,使这些单核细胞能够粘附在被激活的血管壁上,在粘附分子(如ICAM‑1和VCAM‑1)的帮助下穿行并定居于血管周围和表面生态位。阻断这些粘附通路会减少入侵细胞的数量,从而证实了它们的重要性。一旦植入,来自单核细胞的边界巨噬细胞并非简单模仿原本的胚胎来源细胞:它们保持独特的基因表达和染色质图谱,在抗原呈递和细胞粘附相关分子上富集,并在初期损伤表面愈合很久之后仍作为群体的稳定组成部分存在。
对边界免疫的持久重编织
单细胞和整体测序显示,小胶质细胞在再生后大致恢复了原有的分子谱,长期变化很小。然而皮下巨噬细胞则持久地倾向于更“警觉”的亚型,表现出更高水平的免疫激活基因。通过使用遗传标记将胚胎来源细胞与单核细胞来源细胞区分开来,研究团队表明发育起源强烈塑造了这些细胞的基因活动和可及染色质区域。来自单核细胞的边界巨噬细胞带有近期分化的血细胞典型的表观遗传印记,并在感知病原体和与其它免疫细胞相互作用的基因处显示出更高的可及性。当动物遭遇细菌成分挑战时,这些新来细胞比胚胎来源的邻居产生更强的炎性和应激反应,而小胶质细胞和硬膜巨噬细胞的反应变化则小得多。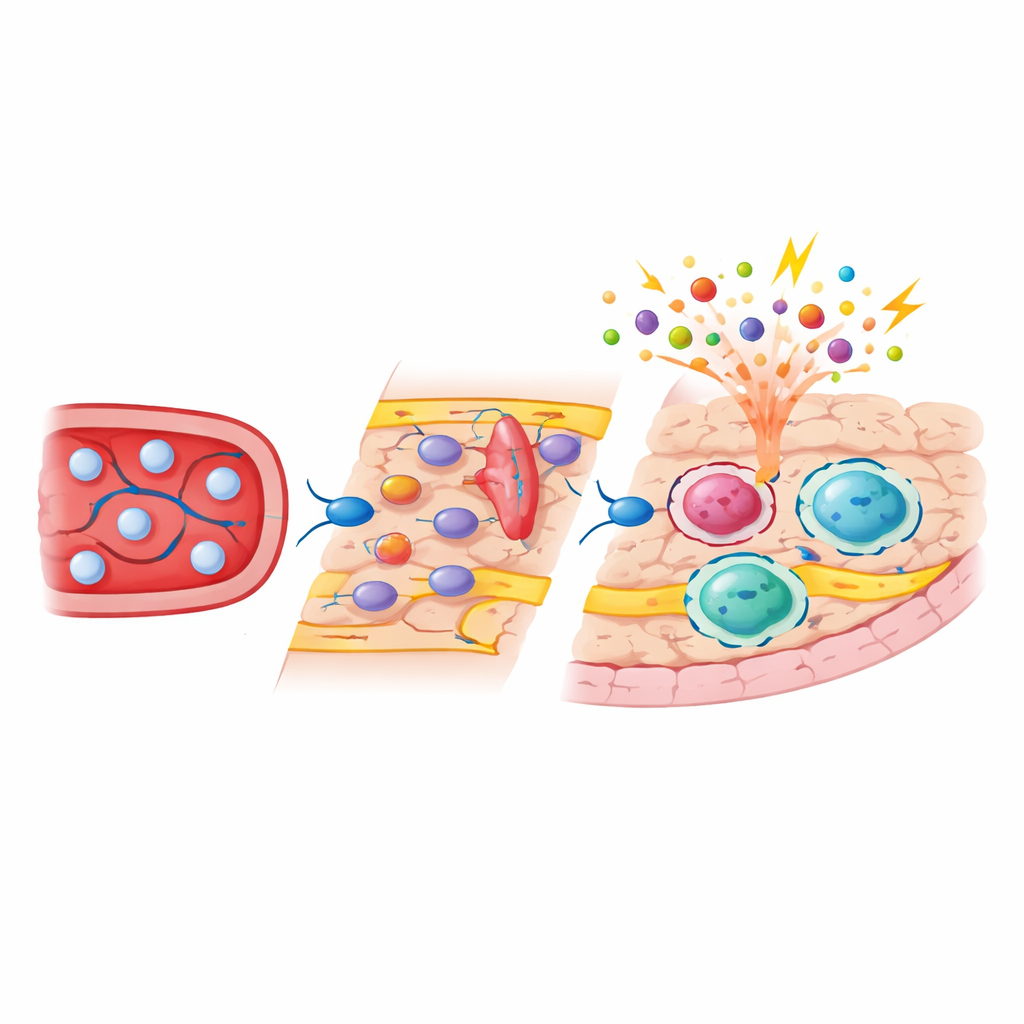
对卒中和大脑健康的影响
作者接着探讨这种隐秘的边界巨噬细胞重塑是否影响疾病。在缺血性卒中模型中,即便病变大小和血管再通与对照组相似,经皮下巨噬细胞再生的小鼠在行为测试中的表现更差。对整体组织和分离的边界巨噬细胞分析显示,再生动物中与炎症、活性氧以及血–脑屏障破坏相关基因的诱导更强。来自单核细胞的边界细胞在卒中后尤其反应性更强,产生更多趋化因子和活化标志物。血管活化成像证实,P‑选择素这一强烈血管炎症标志的信号更高,并且与较差的运动恢复相关联。
对未来治疗的意义
这项工作表明并非所有脑内巨噬细胞都相同,且替换它们并不等同于简单重置系统。小胶质细胞可以从幸存细胞悄然重建并恢复常态。相比之下,位于脑表面的边界巨噬细胞则成为胚胎来源细胞与来自血液的新来者的永久混合体,该混合群体对系统性炎症和卒中反应更为强烈。由于研究者开发出一种在保留小胶质细胞的同时选择性更换这些边界细胞的方法,他们的发现指向一种前景:未来可通过精细调控大脑免疫边界的疗法——要么抑制卒中和神经退行性疾病中有害的炎症,要么增强保护性反应——而不需全局扰动大脑内部的免疫网络。
引用: Fliegauf, M., Levard, D., Cardamone, F. et al. Distinct origins and niches determine the cellular responsiveness of CNS macrophages after repopulation. Nat Immunol 27, 961–974 (2026). https://doi.org/10.1038/s41590-026-02457-y
关键词: 脑边界巨噬细胞, 小胶质细胞再生, 单核细胞植入, 神经炎症, 缺血性卒中